Clear Sky Science · pl
Specyficzna dla ubikwityny proteaza 26 ułatwia kostnienie śródkartylaginowe poprzez stymulowanie hipertrofii chondrocytów i mineralizacji
Jak kości rosną i naprawiają się
Nasz szkielet jest w ciągłej przebudowie. Długie kości ramion i nóg najpierw formują się jako miękka chrząstka, która później przekształca się w twardą kość w procesie zwanym kostnieniem śródkartylaginowym. Ten sam program wspiera gojenie złamań — ale gdy działa nadmiernie w obrębie stawów, może też napędzać chorobę zwyrodnieniową stawów. W niniejszym badaniu odkryto kluczowy przełącznik molekularny, białko o nazwie USP26, które pomaga komórkom chrząstki rosnąć, twardnieć i reagować na siły mechaniczne, takie jak ciężar ciała i ruch. Zrozumienie tego przełącznika może otworzyć nowe możliwości wspomagania naprawy kości przy jednoczesnym spowalnianiu uszkodzeń stawów.
Droga od miękkiej chrząstki do twardej kości
W rozwijającym się zarodku i podczas gojenia się złamań wyspecjalizowane komórki chrząstki, zwane chondrocytami, najpierw się dzielą, następnie powiększają, a w końcu uczestniczą w układaniu minerałów, tworząc kość. Autorzy zaobserwowali, że USP26 staje się bardziej obfity dokładnie wtedy i tam, gdzie zachodzi ta przemiana: w środku rozwijających się kości kończyn myszy, w kostnym zrostu (callus) łączącym złamanie oraz w przerostowych obszarach chrząstki w stawach dotkniętych chorobą zwyrodnieniową. Gdy chondrocyty są w laboratorium stymulowane do dojrzewania, poziomy USP26 rosną równolegle z klasycznymi markerami hipertrofii (powiększenia komórek) i mineralizacji. Te wzorce sugerują, że USP26 działa jako przyspieszacz przejścia z chrząstki do kości. 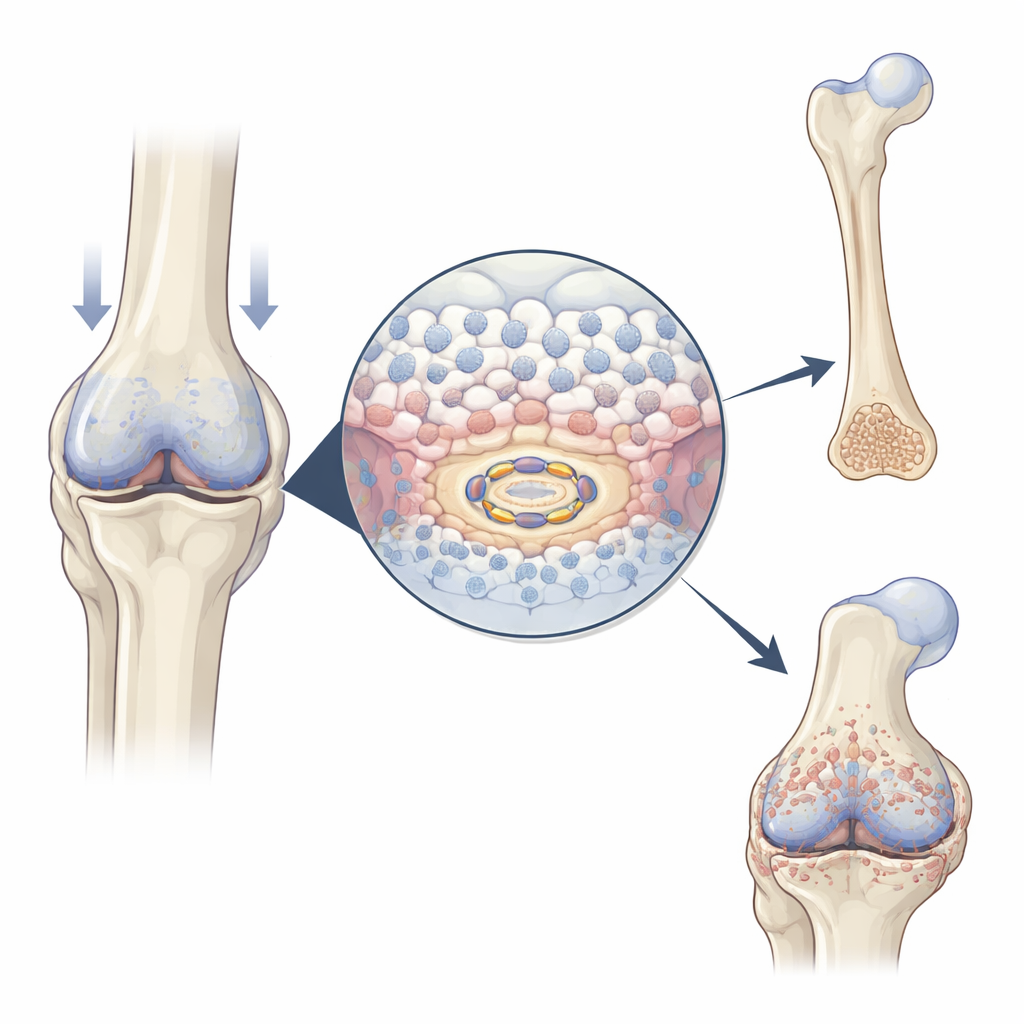
Co się dzieje, gdy brakuje USP26
Aby sprawdzić rolę USP26, zespół zaprojektował myszy, w których to białko usunięto jedynie z chondrocytów. Zwierzęta te rozwijały krótsze kończyny i kręgi, co odzwierciedla zahamowany wzrost szkieletu. Ich płytki wzrostu — strefy, gdzie normalnie powstaje nowa kość — wykazywały mniej powiększonych chondrocytów, słabiej zmineralizowaną chrząstkę oraz obniżoną ekspresję kluczowych genów napędzających tworzenie kości i naciekanie naczyń krwionośnych. Gdy te myszy z defektem USP26 doznały złamania kości udowej, ich zrost zawierał mniej chrząstki i kości, a badania obrazowe wykazały słabszą, mniej zmineralizowaną tkankę naprawczą. Jednocześnie usunięcie USP26 z chrząstki stawowej chroniło przed eksperymentalnie wywołaną chorobą zwyrodnieniową: obserwowano mniej ostrogi kostnych, gładsze powierzchnie chrząstki i niższe wskaźniki nasilenia choroby. Razem wyniki pokazują, że USP26 ma dwoistą naturę — jest potrzebny do prawidłowego wzrostu i naprawy, ale jednocześnie przyczynia się do szkodliwego przerastania kości w chorych stawach.
Zasilanie tworzenia kości przez komórkowe elektrownie
Powiększanie się chondrocytów i ich mineralizacja wymagają dużych nakładów energii. Badacze odkryli, że USP26 pomaga sprostać temu zapotrzebowaniu, utrzymując zdrowe mitochondria — komórkowe elektrownie. Bez USP26 chondrocyty pobierały mniej glukozy, wytwarzały mniej ATP (waluty energetycznej komórki) i produkowały mniej mleczanu. Ich mitochondria było mniej, były bardziej pofragmentowane i funkcjonowały gorzej, z obniżoną aktywnością oddechową oraz niższą ekspresją genów zaangażowanych w fosforylację oksydacyjną. Białko o nazwie FBP2 wyłoniło się jako kluczowe ogniwo: w braku USP26 poziomy FBP2 gwałtownie rosły. Wiadomo, że FBP2 skłania komórki od odtwarzania glukozy w kierunku hamowania biogenezy mitochondriów. Tutaj blokada FBP2 w chondrocytach pozbawionych USP26 przywróciła wykorzystanie glukozy, masę mitochondriów i produkcję energii oraz odnowiła zdolność komórek do powiększania się i mineralizacji. W modelach choroby zwyrodnieniowej hamowanie FBP2 również nasilało kostnienie chrząstki, podkreślając, jak równowaga USP26–FBP2 kształtuje wyniki związane z kością. 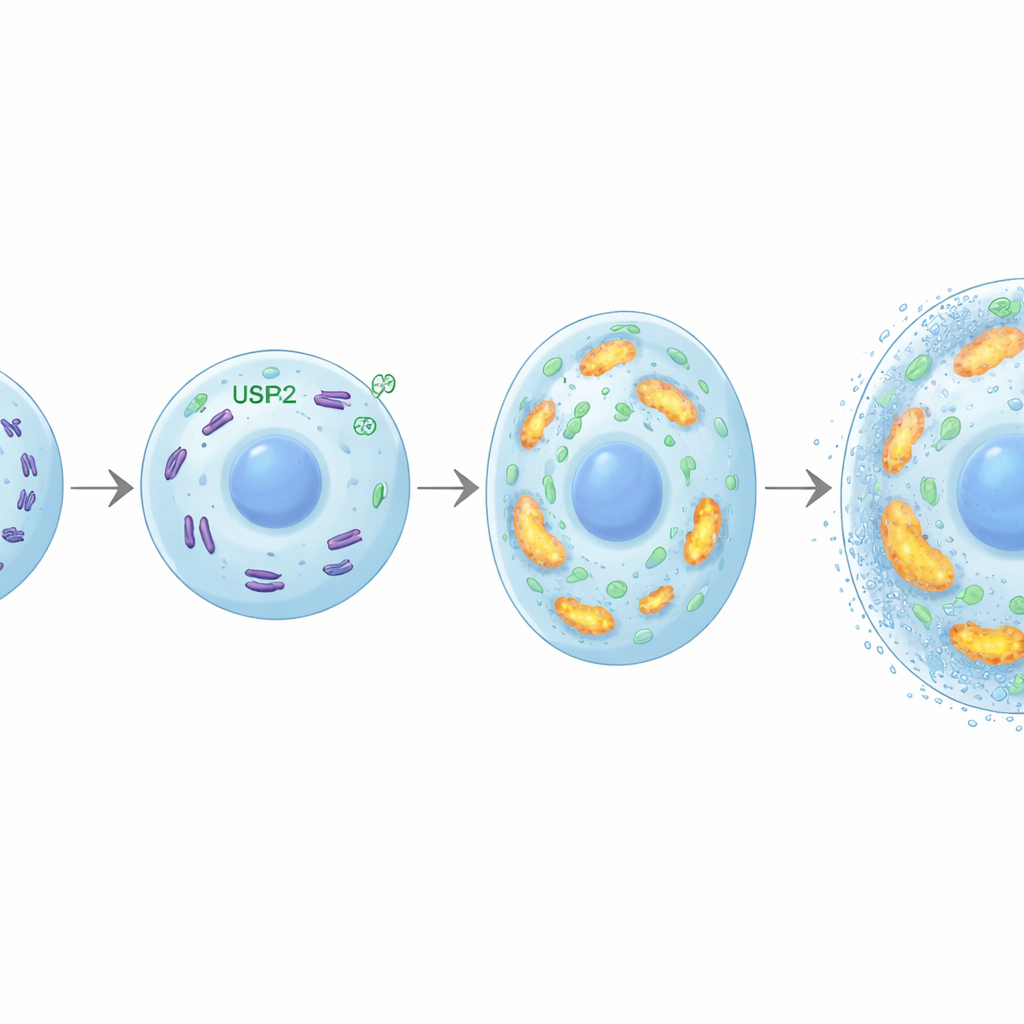
Jak siły mechaniczne włączają USP26
Układ szkieletowy nieustannie wyczuwa i dostosowuje się do sił mechanicznych. Zespół stwierdził, że obszary chrząstki pod dużym obciążeniem — na przykład strefy przenoszące ciężar w chorych kolanach — wykazują wyższe poziomy USP26. W hodowanych chondrocytach kontrolowane ściskanie zwiększało USP26 i jednocześnie uruchamiało geny napędzające hipertrofię i mineralizację. Ten sygnał mechaniczny przechodził przez receptor estrogenowy‑α (ER‑α), hormonowrażliwy czynnik transkrypcyjny. Pod uciskiem ER‑α aktywował się przez fosforylację w określonym miejscu (seryna 118) i wiązał się bezpośrednio z krótką sekwencją DNA w regionie kontrolnym genu USP26. Mutacja albo tego miejsca DNA, albo miejsca fosforylacji na ER‑α osłabiała wzrost USP26, utrzymywała wyższe poziomy FBP2 i słabiła metaboliczną oraz rozwojową zmianę w kierunku tworzenia kości. U myszy zmuszanych do biegania i przeciążających stawy kolanowe usunięcie USP26 w chondrocytach ponownie zmniejszyło przerost kostny i uszkodzenie chrząstki, potwierdzając jego rolę jako mechanicznego „czujnika‑efektora” in vivo.
Dlaczego to ma znaczenie dla kości i stawów
Mówiąc wprost, USP26 pomaga komórkom chrząstki przekształcać obciążenie mechaniczne i dostępność paliwa w aktywność budującą kość. Robi to przez obniżanie poziomu FBP2, zachowanie solidnych, produkujących energię mitochondriów oraz popychanie chondrocytów w stronę powiększenia i mineralizacji. To sprawia, że USP26 jest niezbędny dla prawidłowego wzrostu szkieletu i skutecznego zrastania złamań. Jednak u starszych lub uszkodzonych stawów, narażonych na przewlekłe przeciążenie, ta sama ścieżka wydaje się napędzać utwardzanie i przerost chrząstki charakterystyczne dla choroby zwyrodnieniowej. Celowanie w sam USP26, albo w jego efektor FBP2, może w przyszłości pozwolić selektywnie wzmocnić kostnienie śródkartylaginowe tam, gdzie potrzebujemy więcej kości — po urazie lub w zaburzeniach wzrostu — przy jednoczesnym jego przytłumieniu w stawach zagrożonych chorobą zwyrodnieniową.
Cytowanie: Li, C., Xu, Y., Zhou, L. et al. Ubiquitin-specific protease 26 facilitates endochondral ossification by driving chondrocyte hypertrophy and mineralization. Bone Res 14, 41 (2026). https://doi.org/10.1038/s41413-026-00517-5
Słowa kluczowe: kostnienie śródkartylaginowe, hipertrofia chondrocytów, metabolizm mitochondrialny, mechanotransdukcja, choroba zwyrodnieniowa stawów