Clear Sky Science · he
פרוטאז ספציפית לאוביקויטין 26 מקלה על האוסיפיקציה האנדוכרנלית על‑ידי קידום היפרטרופיה של כונדרוציטים ומינרליזציה
איך העצמות גדלות ומשתקמות
שלדינו משתנה כל הזמן. עצמות ארוכות בזרועות וברגליים נוצרות תחילה מסחוס רך, שמאוחר יותר הופך לעצם קשה בתהליך שנקרא אוסיפיקציה אנדוכרנלית. אותו מנגנון מסייע גם לריפוי עצמות שבורות—אבל כאשר הוא מופעל ביתר באזורי המפרקים, הוא עלול לתרום להתפתחות דלקת פרקים ניוונית. מחקר זה חושף מתג מולקולרי מרכזי, חלבון בשם USP26, שעוזר לתאי הסחוס לגדול, להתמקד ולרגיש לכוחות מכניים כמו משקל ותנועה. הבנת מתג זה עשויה לפתוח דרכים חדשות לשיפור ריפוי עצם תוך האטת נזק למפרקים.
המסע מסחוס רך לעצם קשה
בעוברים הגדלים ובשברים שמתקנים, תאי סחוס מתמחים הידועים ככונדרוציטים מתחילים להתרבות, אחר כך מתרחבים, ולבסוף מסייעים להטמעת מינרלים ליצירת עצם. המחברים מצאו ש‑USP26 נעשה בשפע בדיוק בזמן ובמקום שבו המעבר הזה מתרחש: במרכז עצמות הגפה בעכברים מתפתחים, בקאלוס הסחוס שמגשר על שבר מתרופף, ובאזורים של התעבות סחוס במפרקים עם דלקת פרקים ניוונית. כאשר כונדרוציטים מעודדים לבגרות במעבדה, רמות USP26 עולות במקביל לסמנים הקלאסיים של היפרטרופיה (הגדלת התאים) ומינרליזציה. דפוסים אלה מרמזים ש‑USP26 פועל כמאיץ במעבר מסחוס לעצם. 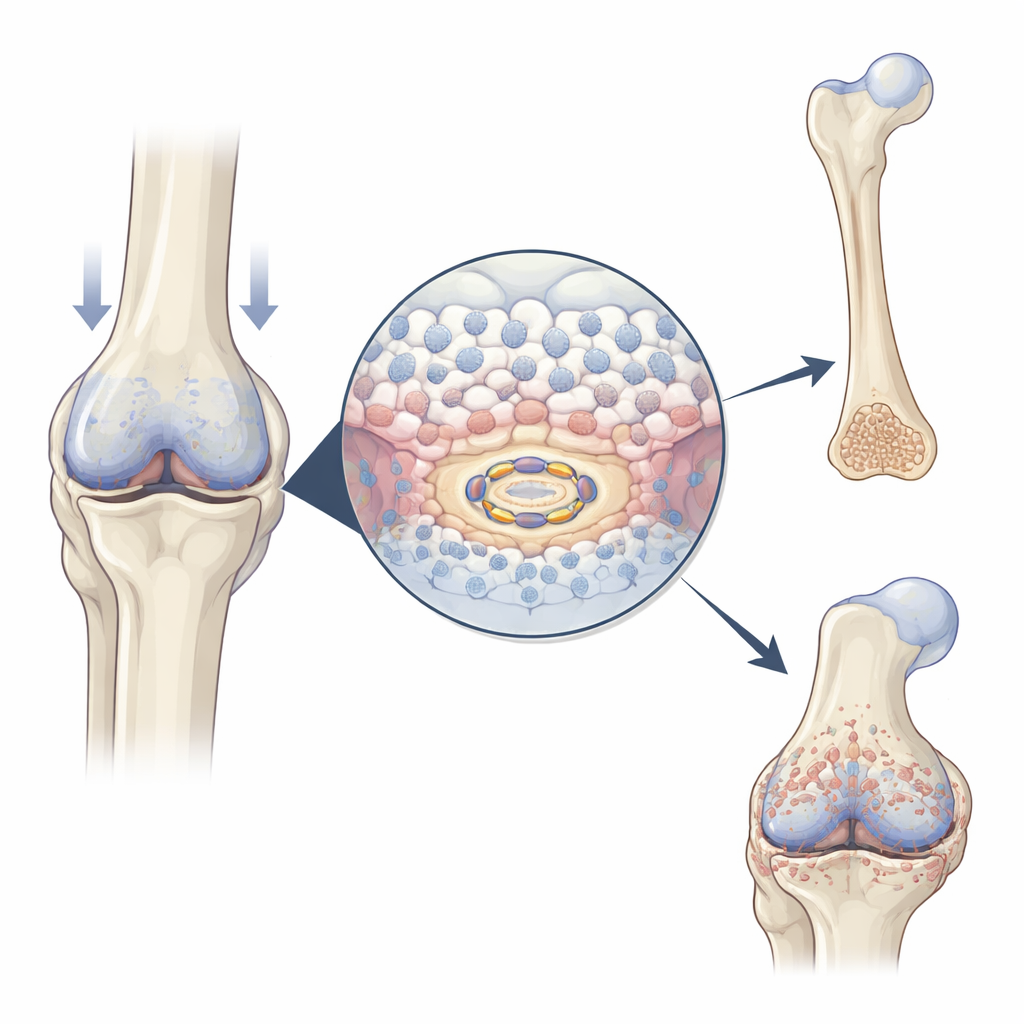
מה קורה כש‑USP26 חסר
כדי לבדוק את תפקידו של USP26, הצוות הנדס עכברים שבהם החלבון הוסר רק מתוך כונדרוציטים. בעלי חיים אלה פיתחו גפיים וחוליות קצרות יותר, תופעה המשקפת גדילה שלדית מעוכבת. צלחות הגדילה שלהם—האזור שבו בדרך כלל נוצרת עצם חדשה—הציגו פחות כונדרוציטים מורחבים, סחוס פחות ממונרל, והבעה מופחתת של גנים מפתח שמניעים יצירת עצם וחדירת כלי דם. כאשר לעכברים אלה נגרמו שברי ירך, הקאלוסים שלהם הכילו פחות סחוס ועצם, וסריקות חשפו רקמת תיקון חלשה ופחות ממונרל. במקביל, הסרת USP26 מסחוס מפרקי הגנה מפני דלקת פרקים ניסויית: נצפו פחות יבלות עצם, משטחי סחוס חלקים יותר, ונקודות חומרת מחלה נמוכות יותר. יחד, הממצאים מראים כי USP26 היא דו‑להבית—הוא נחוץ לגדילה ותיקון תקינים, אך גם תורם להתעבות עצמית מזיקה במפרקים חולים.
דלק להיווצרות עצם דרך תחנות הכוח של התא
הגדלת הכונדרוציטים והמינרליזציה דורשים כמות גדולה של אנרגיה. החוקרים גילו ש‑USP26 מסייע למלא דרישה זו על ידי שימור מיטוכונדריות בריאות, תחנות הכוח של התא. בהעדר USP26, כונדרוציטים לקחו פחות גלוקוז, ייצרו פחות ATP (מטבע האנרגיה של התא), והפיקו פחות לקטט. המיטוכונדריות שלהם היו פחותות במספר, מפורקות יותר, ותפקדו בצורה לקויה, עם פעילות נשימתית מופחתת והבעה נמוכה של גנים המעורבים בפוספורילציה אוקסידטיבית. חלבון בשם FBP2 התגלה כקישור קריטי: בהיעדר USP26, רמות FBP2 עלו באופן חזק. ידוע כי FBP2 מטה את התאים משימוש בגלוקוז ומשתיק ביוגנזה מיטוכונדריאלית. כאן, חסימת FBP2 בכונדרוציטים חסרי USP26 שיקמה את ניצול הגלוקוז, מסת המיטוכונדריות וייצור האנרגיה, והחזירה את יכולתם להתרחב ולהתמנן. במודלים של דלקת פרקים, עיכוב FBP2 גם הגבירה את אוסיפיקציית הסחוס, מה שמדגיש כיצד איזון USP26–FBP2 מעצב תוצאות קשורות לעצם. 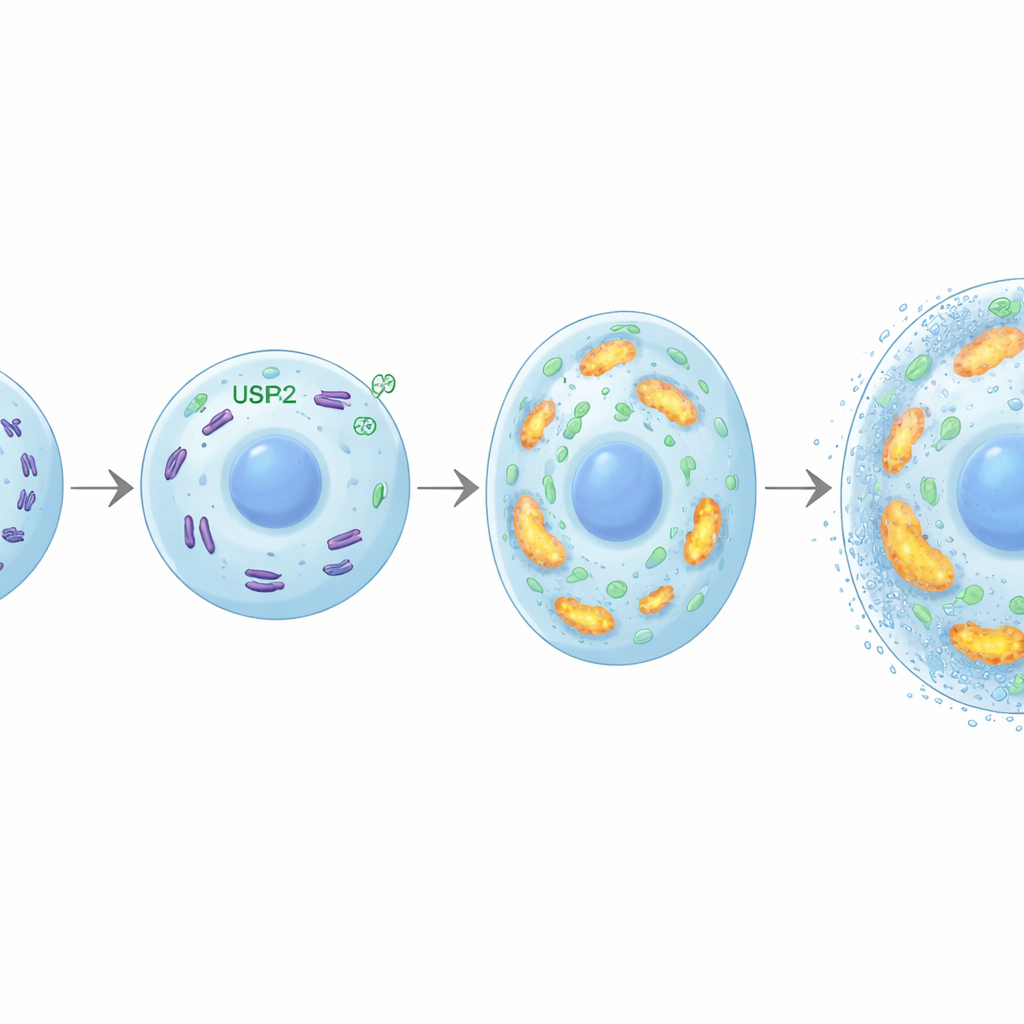
כיצד כוחות מכניים מדליקים את USP26
השלד חשים ומסתגלים כל הזמן לכוחות מכניים. הצוות מצא שאזורי סחוס שנמצאים תחת עומס כבד—כמו אזורים נשאי משקל בברכיים ארטריטיות—מציגים רמות USP26 גבוהות יותר. בכונדרוציטים בתרבית, החלה דחיסה מבוקרת שהגבירה את USP26 ובאותו הזמן הפעילה גנים שמניעים היפרטרופיה ומינרליזציה. אות מכני זה עבר דרך קולטנית האסטרוגן‑α (ER‑α), פקטור שעתוק הרגיש להורמונים. תחת דחיסה, ER‑α הופעל על‑ידי פוספורילציה באתר ספציפי (סרין 118) וקשר ישירות לרצף DNA קצר באיזור הבקרה של גן USP26. מוטציה או באתר ה‑DNA הזה או באתר הפוספורילציה על ER‑α החלישה את עליית USP26, שמרה על רמות FBP2 גבוהות יותר, והחלישה את המעבר המטבולי וההתפתחותי לעבר יצירת עצם. בעכברים שנאלצו לרוץ ולהעמיס על מפרקי הברכיים שלהם, מחיקה של USP26 בכונדרוציטים שוב הפחיתה גדילת עצם מופרזת ונזק לסחוס, ואיששה את תפקידו כ"חוש–מבצע" מכני ברדמת החיים.
מדוע זה חשוב לעצמות ולמפרקים
בהגדרה פשוטה, USP26 מסייע לתאי הסחוס להמיר עומס מכני ומקורות דלק לפעילות בניית עצם. הוא עושה זאת על‑ידי הורדת FBP2, שמירה על מיטוכונדריות חזקות ומייצרות אנרגיה, ודחיפה של כונדרוציטים להתרחב ולהתמנן. זה הופך את USP26 לחיוני לגדילה שלדית תקינה ולריפוי יעיל של שברים. אך במפרקים מזדקנים או פגועים החשופים לעומס כרוני, אותו מסלול נראה כי מניע את התקשות והגדילה המופרזת של הסחוס הסימפטומטית לדלקת פרקים ניוונית. באמצעות מיקוד ב‑USP26 עצמו, או בבן‑הזוג התאי שלו FBP2, טיפולים עתידיים עשויים יום אחד להגביר באופן סלקטיבי אוסיפיקציה אנדוכרנלית כשנזדקק לעוד עצם—לאחר טראומה או בהפרעות גדילה—בעוד יורידו אותה במפרקים בסיכון למחלות ניווניות.
ציטוט: Li, C., Xu, Y., Zhou, L. et al. Ubiquitin-specific protease 26 facilitates endochondral ossification by driving chondrocyte hypertrophy and mineralization. Bone Res 14, 41 (2026). https://doi.org/10.1038/s41413-026-00517-5
מילות מפתח: אוסיפיקציה אנדוכרנלית, היפרטרופיה של כונדרוציטים, מטבוליזם מיטוכונדריאלי, מכנוטרנסדוקציה, דלקת פרקים ניוונית