Clear Sky Science · sv
Osteoblast‑producerat osteomodulin begränsar osteoklastogenes via ITGB8/RRM2‑medierad minskning av mitokondriell respiration och mitokondriell ATP‑produktion
Varför detta är viktigt för skelettet
Osteoporos försvagar tyst skelettet hos miljontals äldre vuxna, särskilt kvinnor efter klimakteriet. De flesta nuvarande läkemedel fungerar genom att i stort sett bromsa nedbrytningen eller öka uppbyggnaden av ben, ofta med biverkningar. Denna studie avslöjar en naturlig "broms" inbyggd i benet: ett protein som bildas av benbyggande celler och som berättar för benätande celler att skruva ner sin energianvändning och därmed deras destruktiva kraft. Att förstå detta inbyggda säkerhetssystem kan inspirera säkrare och mer riktade behandlingar mot osteoporos.
En dold signal mellan benceller
Bens hälsa beror på en konstant dragkamp mellan två huvudcelltyper. Osteoblaster bygger nytt ben, medan osteoklaster löser upp gammalt ben så att det kan ersättas. Författarna fokuserade på en förbisedda signal kallad osteomodulin, eller OMD, ett litet protein som utsöndras av osteoblaster in i benmatrisen. Genom att gräva i flera stora genetiska datamängder från olika osteoporosmodeller fann de att genen för OMD konsekvent var nedreglerad i sköra ben. När de undersökte benvävnad och blod från postmenopausala kvinnor hade de med osteoporos mindre OMD i både ben och cirkulation, och lägre OMD‑nivåer korrelerade med markörer för snabb benförlust. Liknande minskningar sågs i en musemodell för östrogenbortfall‑osteoporos, vilket tyder på att OMD‑nedgång är ett vanligt drag vid försvagning av ben. 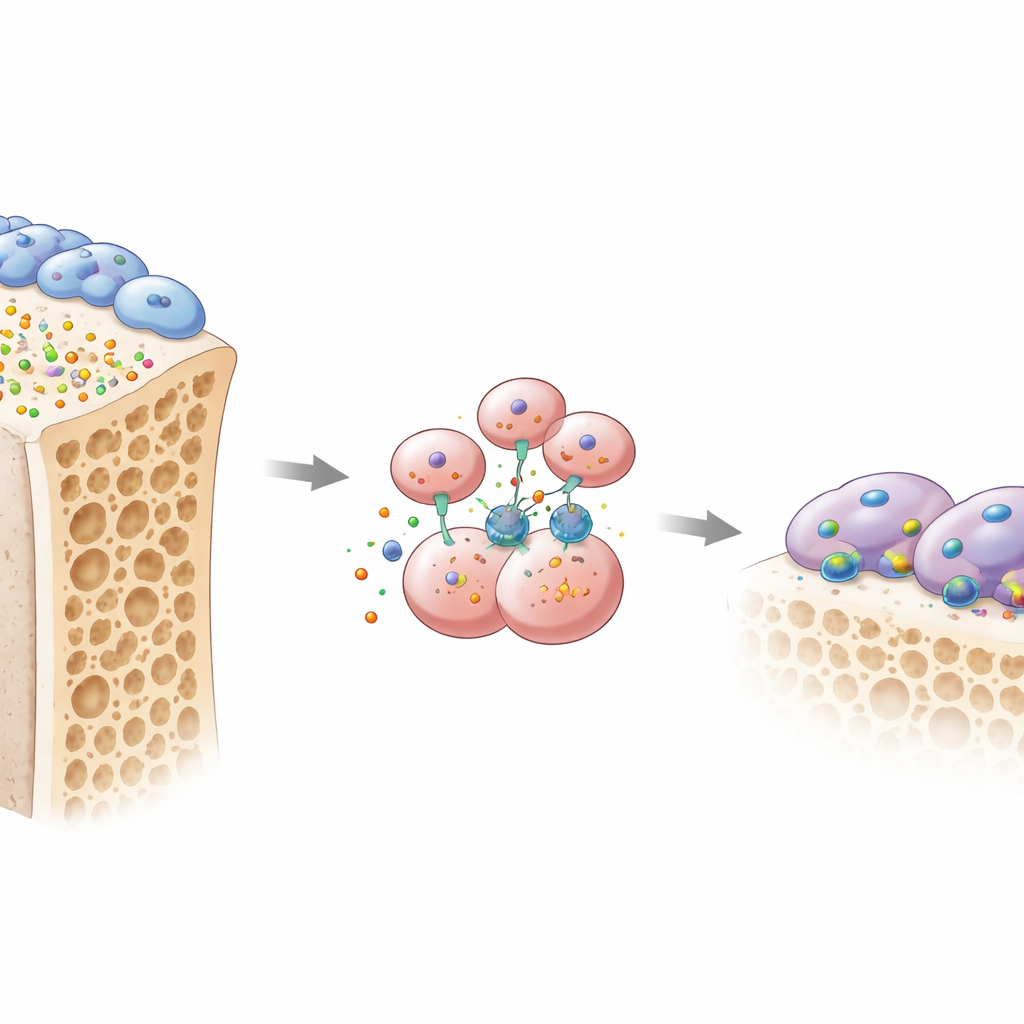
Vad händer när bromsen tas bort
För att testa orsak och verkan konstruerade teamet möss utan OMD. När OMD togs bort i hela kroppen, eller specifikt i osteoblaster, förlorade djuren betydligt mer spongiöst ben och visade en ökning av aktiva osteoklaster som betade längs bensurfar. I kontrast hade det liten effekt att ta bort OMD enbart från osteoklastföregångare, vilket antyder att OMD normalt fungerar som ett meddelande skickat från osteoblaster till deras benresorberande grannar. I odlingsskålar bildade osteoklastföregångare som växte tillsammans med osteoblaster som producerade lite OMD stora, aggressiva osteoklaster. Att tillsätta renat OMD‑protein förändrade bilden: det minskade kraftigt bildningen av dessa flerkärniga, benätande celler och störde deras specialiserade "tätningringar" som de använder för att greppa och lösa upp ben.
Nedreglering av cellernas kraftverk
Forskarna frågade sig sedan hur denna osteoblastsignal så kraftfullt kunde begränsa osteoklaster. Deras analyser pekade mot energimetabolism. Osteoklaster är energikrävande och förlitar sig i hög grad på mitokondrierna — cellens kraftverk — för att generera ATP. När osteoklastföregångare exponerades för OMD sjönk uttrycket av gener och proteiner involverade i mitokondriell respiration, antalet kopior av mitokondriellt DNA minskade, och direkta mätningar visade lägre syreförbrukning och ATP‑produktion från mitokondrierna. Glykolys, en backuppathway för sockernedbrytning, ökade endast marginellt och kunde inte fullt ut kompensera. Som ett resultat föll cellernas mitokondriella membranpotential och deras övergripande metabola profil skiftade mot ett energistressat tillstånd. Dessa förändringar var nära kopplade till reducerade nivåer av en nyckelenzym‑subenhet kallad RRM2, som hjälper till att förse byggstenar för DNA som krävs för att upprätthålla mitokondriellt DNA.
En steg‑för‑steg‑kedja från yt‑sensor till gener
Genom att gå djupare spårade teamet en signalväg som länkar ett yttre protein till inre energikontroll. OMD visade sig binda en specifik receptor, integrin β8, på osteoklastföregångare. Denna interaktion dämpade aktiviteten hos en molekylär strömbrytare, RhoA, och ökade fosforyleringen av regulatorn YAP, vilket fick YAP att lämna cellkärnan. Utan att YAP samarbetar med TEAD‑proteiner på DNA dämpades Rrm2‑genen. Lägre RRM2 innebar färre DNA‑byggstenar för mitokondrier, mindre mitokondriellt DNA, reducerad mängd komponenter i elektrontransportkedjan och slutligen svagare mitokondriell ATP‑produktion. När forskarna blockerade RRM2 med ett litet molekylärt ämne sjönk osteoklastbildning och mitokondriell funktion på liknande sätt som vid OMD‑behandling. Omvänt räddade tvångsuttryck av RRM2 delvis deras energiproduktion och osteoklast‑utveckling även i närvaro av OMD. 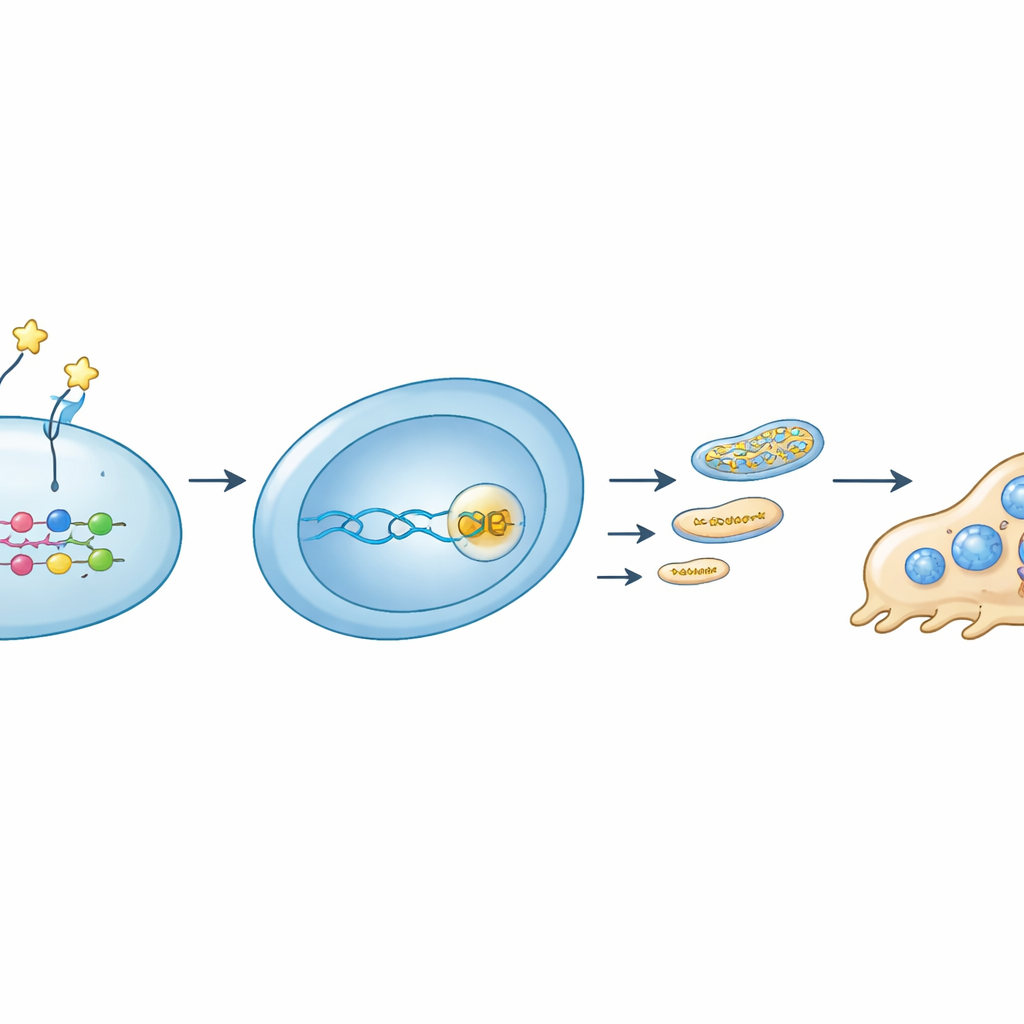
Test av potentiella nya behandlingsvinklar
Slutligen undersökte studien om förstärkning av denna naturliga broms kunde skydda ben hos levande djur. I möss som fick sina äggstockar borttagna för att efterlikna postmenopausal benförlust bevarade regelbundna injektioner av rekombinant OMD‑protein eller RRM2‑hämmaren osalmid båda benstrukturen. Behandlade möss hade tätare trabekulärt ben, färre osteoklaster och lägre nivåer av mitokondriella proteiner i dessa osteoklaster. Liknande fördelar observerades i en modell för snabb, inflammationsdriven benförlust utlöstad av bakteriella toxiner. Viktigt är att kortvarig behandling inte visuellt skadade större organ, även om längre och mer detaljerade säkerhetsstudier krävs.
Vad detta betyder för framtida vård
Sammantaget visar arbetet att osteomodulin fungerar som en viktig fredsbevarare i benet. När det produceras av osteoblaster signalerar det via integrin β8 för att omprogrammera osteoklastföregångare och strypa deras mitokondriella energiförsörjning så att de inte kan överväxa eller överarbeta. Vid osteoporos verkar denna broms försvagas, vilket tillåter de benresorberande cellerna att bli mer energiska och destruktiva. Genom att återställa OMD eller rikta in sig mot det nedströms energienzymet RRM2 kan det bli möjligt att mjukt sänka benresorptionen utan att stänga av den helt, vilket erbjuder en ny, metabolismfokuserad strategi för att skydda åldrande skelett.
Citering: Jiang, X., Chen, H., Hou, W. et al. Osteoblast-derived osteomodulin restrains osteoclastogenesis via ITGB8/RRM2-mediated reduction of mitochondrial respiration and mitochondrial ATP production. Exp Mol Med 58, 879–897 (2026). https://doi.org/10.1038/s12276-026-01682-7
Nyckelord: osteoporos, benombyggnad, osteoklaster, mitokondriell metabolism, osteomodulin