Clear Sky Science · ru
Остеобластный остеомодулин сдерживает остеокластогенез через ITGB8/RRM2‑опосредованное снижение митохондриального дыхания и образования митохондриального АТФ
Почему это важно для костей
Остеопороз незаметно ослабляет кости миллионов пожилых людей, особенно женщин в постменопаузе. Большинство существующих лекарств действуют, в целом замедляя разрушение кости или усиливая ее образование, часто с побочными эффектами. В этом исследовании выявлен естественный «тормоз», встроенный в саму кость: белок, вырабатываемый клетками, строящими кость, который приказывает клеткам, разрушающим кость, снизить потребление энергии и, следовательно, свою разрушительную силу. Понимание этой встроенной системы безопасности может вдохновить создание более безопасных и направленных методов лечения остеопороза.
Скрытый сигнал между клетками кости
Здоровье костей зависит от постоянной борьбы между двумя основными типами клеток. Остеобласты создают новую кость, а остеокласты растворяют старую, чтобы ее можно было заменить. Авторы сосредоточились на малоизученном сигнале, называемом остеомодулином, или OMD, небольшом белке, секретируемом остеобластами в костный матрикс. Анализ нескольких крупных генетических наборов данных из различных моделей остеопороза показал, что ген OMD последовательно снижен в хрупких костях. При обследовании костной ткани и крови у женщин в постменопаузе у больных остеопорозом было меньше OMD как в кости, так и в циркуляции, и более низкие уровни OMD коррелировали с маркерами быстрого потери кости. Сходные снижения обнаруживались в модели мышей с остеопорозом, вызванным потерей эстрогена, что указывает на то, что падение уровня OMD является общей чертой ослабления кости. 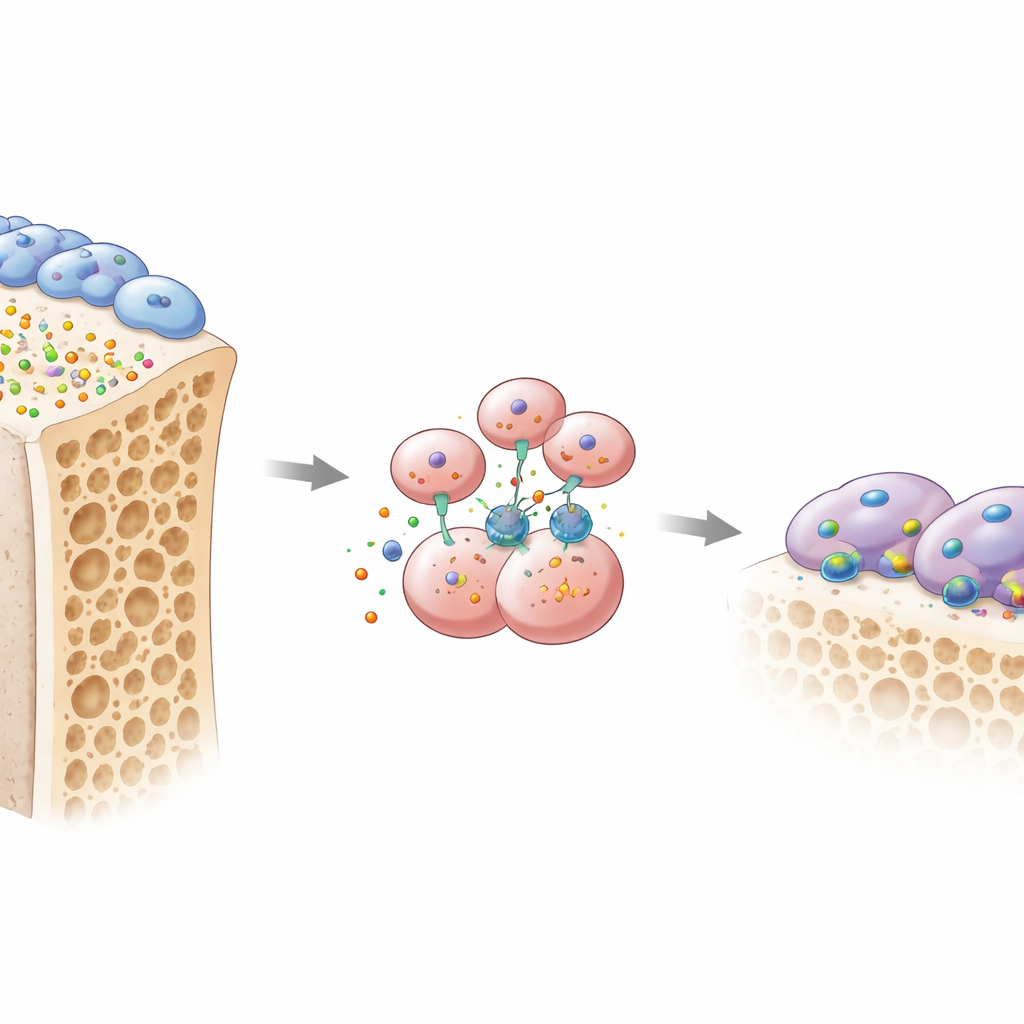
Что происходит, когда тормоз убирают
Чтобы проверить причинно-следственную связь, команда создала мышей без OMD. При удалении OMD по всему организму или специфически в остеобластах животные теряли значительно больше губчатой кости и демонстрировали всплеск активных остеокластов, поедающих кость по поверхностям. Напротив, удаление OMD только из предшественников остеокластов мало влияло, что подразумевает, что OMD действует как сигнал, посылаемый остеобластами их соседям‑ресорберам кости. В культурах клеток предшественники остеокластов, выращенные с остеобластами, продуцировавшими мало OMD, превращались в крупные агрессивные остеокласты. Возвращение очищенного белка OMD меняло ситуацию: резко сокращалось образование этих многоядерных костеразрушающих клеток и разрушались их специализированные «уплотняющие кольца», с помощью которых они захватывают и растворяют кость.
Понижение работы клеточных электростанций
Затем исследователи изучили, как этот сигнал от остеобластов может столь сильно сдерживать остеокласты. Их анализы указали на энергетический метаболизм. Остеокласты требовательны к энергии и сильно зависят от митохондрий, «электростанций» клетки, для выработки АТФ. При воздействии OMD в предшественниках остеокластов снижалась экспрессия генов и белков, участвующих в митохондриальном дыхании, уменьшалось количество копий митохондриальной ДНК, а прямые измерения показали более низкое потребление кислорода и продукцию АТФ митохондриями. Гликолиз, альтернативный путь сжигания сахара, повышался лишь немного и не мог полностью компенсировать потерю. В результате падал митохондриальный мембранный потенциал, и общий метаболический профиль клеток смещался в сторону энергетического стресса. Эти изменения тесно связывались со снижением уровня ключевого субъединичного фермента RRM2, который помогает обеспечивать строительные блоки ДНК, необходимые для поддержания митохондриальной ДНК.
Шаг за шагом: от поверхностного датчика к генам
Углубляясь, команда проследила сигнальную цепочку, связывающую внешний белок с внутренним энергетическим контролем. Было показано, что OMD связывается со специфическим рецептором, интегрином β8, на предшественниках остеокластов. Это взаимодействие подавляло активность молекулярного переключателя RhoA и усиливало фосфорилирование регулятора YAP, вызывая выход YAP из ядра. Без партнёрства YAP с белками TEAD на ДНК ген Rrm2 стихал. Более низкий уровень RRM2 означал меньше строительных блоков ДНК для митохондрий, меньше митохондриальной ДНК, снижение числа компонентов дыхательной цепи электронов и, в конечном итоге, слабее производство митохондриального АТФ. Когда исследователи блокировали RRM2 малой молекулой, формирование остеокластов и митохондриальная функция снижались так же, как при действии OMD. Напротив, вынужденная сверхэкспрессия RRM2 частично восстанавливала их энергетическое производство и развитие остеокластов даже в присутствии OMD. 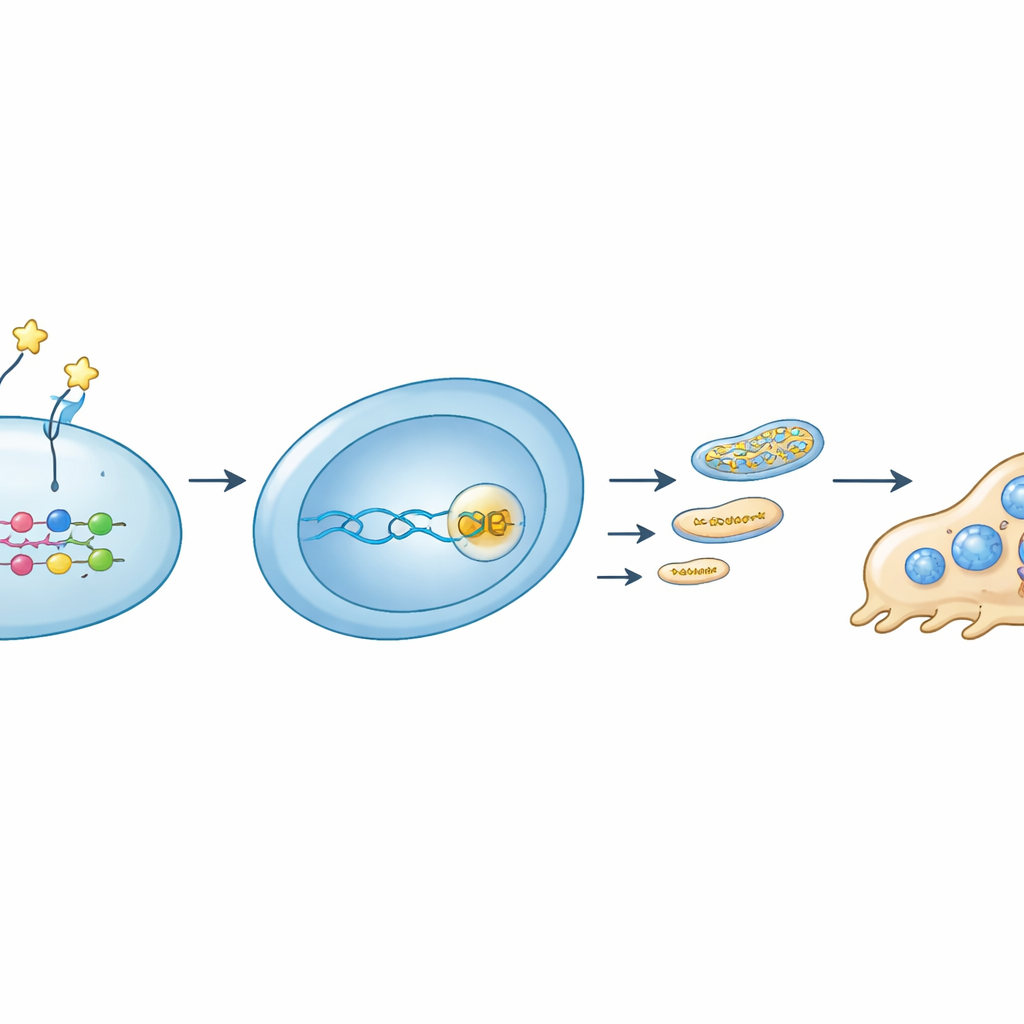
Испытание возможных новых лечебных подходов
Наконец, исследование спросило, может ли усиление этого естественного тормоза защитить кости в живых организмах. У мышей, которым удалили яичники для моделирования постменопаузального потери кости, регулярные инъекции рекомбинантного белка OMD или блокирующего RRM2 препарата осальмида сохраняли структуру кости. Леченые мыши имели более плотную трабекулярную кость, меньше остеокластов и более низкие уровни митохондриальных белков в этих остеокластах. Сходные преимущества наблюдались в модели быстрого воспалительного разрушения кости, вызванного бактериальными токсинами. Важно, что краткосрочное лечение не причиняло видимого вреда основным органам, хотя потребуются более продолжительные и детальные исследования безопасности.
Что это значит для будущего ухода
В совокупности работа показывает, что остеомодулин действует как важный миротворец в кости. При выработке остеобластами он сигнализирует через интегрин β8, перепрограммируя предшественников остеокластов и ограничивая их митохондриальное питание, чтобы они не могли чрезмерно разрастаться или чрезмерно работать. При остеопорозе этот тормоз, по-видимому, ослабевает, позволяя клеткам‑ресорберам кости становиться более энергичными и разрушительными. Восстановление OMD или нацеливание на нижестоящий энергетический фермент RRM2 может позволить мягко замедлить разрушение кости, не прекращая его полностью, предлагая новую, ориентированную на метаболизм стратегию защиты стареющего скелета.
Цитирование: Jiang, X., Chen, H., Hou, W. et al. Osteoblast-derived osteomodulin restrains osteoclastogenesis via ITGB8/RRM2-mediated reduction of mitochondrial respiration and mitochondrial ATP production. Exp Mol Med 58, 879–897 (2026). https://doi.org/10.1038/s12276-026-01682-7
Ключевые слова: остеопороз, ремоделирование кости, остеокласты, митохондриальный метаболизм, остеомодулин