Clear Sky Science · pl
Osteoblasty pochodny osteomodulina hamuje osteoklastogenezę poprzez ITGB8/RRM2‑zmediowane zmniejszenie oddechu mitochondrialnego i produkcji mitochondrialnego ATP
Dlaczego to ma znaczenie dla kości
Osteoporoza cicho osłabia kości u milionów starszych osób, szczególnie u kobiet po menopauzie. Większość dostępnych leków działa przez szerokie spowolnienie resorpcji kości lub pobudzenie jej tworzenia, często z efektami ubocznymi. W tym badaniu odkryto naturalny „hamulec” wbudowany w samą tkankę kostną: białko produkowane przez komórki budujące kość, które mówi komórkom trawiącym kość, żeby ograniczyły zużycie energii, a tym samym swoją destrukcyjną siłę. Zrozumienie tego wrodzonego systemu bezpieczeństwa może zainspirować bezpieczniejsze, bardziej ukierunkowane terapie osteoporozy.
Ukryty sygnał między komórkami kostnymi
Zdrowie kości zależy od stałej rywalizacji między dwoma głównymi typami komórek. Osteoblasty budują nową kość, podczas gdy osteoklasty rozpuszczają starą kość, aby mogła zostać zastąpiona. Autorzy skupili się na pomijanym sygnale zwanym osteomoduliną, czyli OMD, małym białku wydzielanym przez osteoblasty do macierzy kostnej. Analizując kilka dużych zbiorów genetycznych z różnych modeli osteoporozy, stwierdzili, że gen OMD był konsekwentnie wyciszony w kruchych kościach. Badania tkanki kostnej i krwi kobiet po menopauzie wykazały, że u chorych na osteoporozę OMD było mniej zarówno w kości, jak i w krążeniu, a niższe poziomy OMD korelowały z markerami szybkiej utraty kości. Podobne obniżenia zaobserwowano w modelu myszy z osteoporozą spowodowaną utratą estrogenów, co sugeruje, że spadek OMD jest wspólną cechą osłabienia kości. 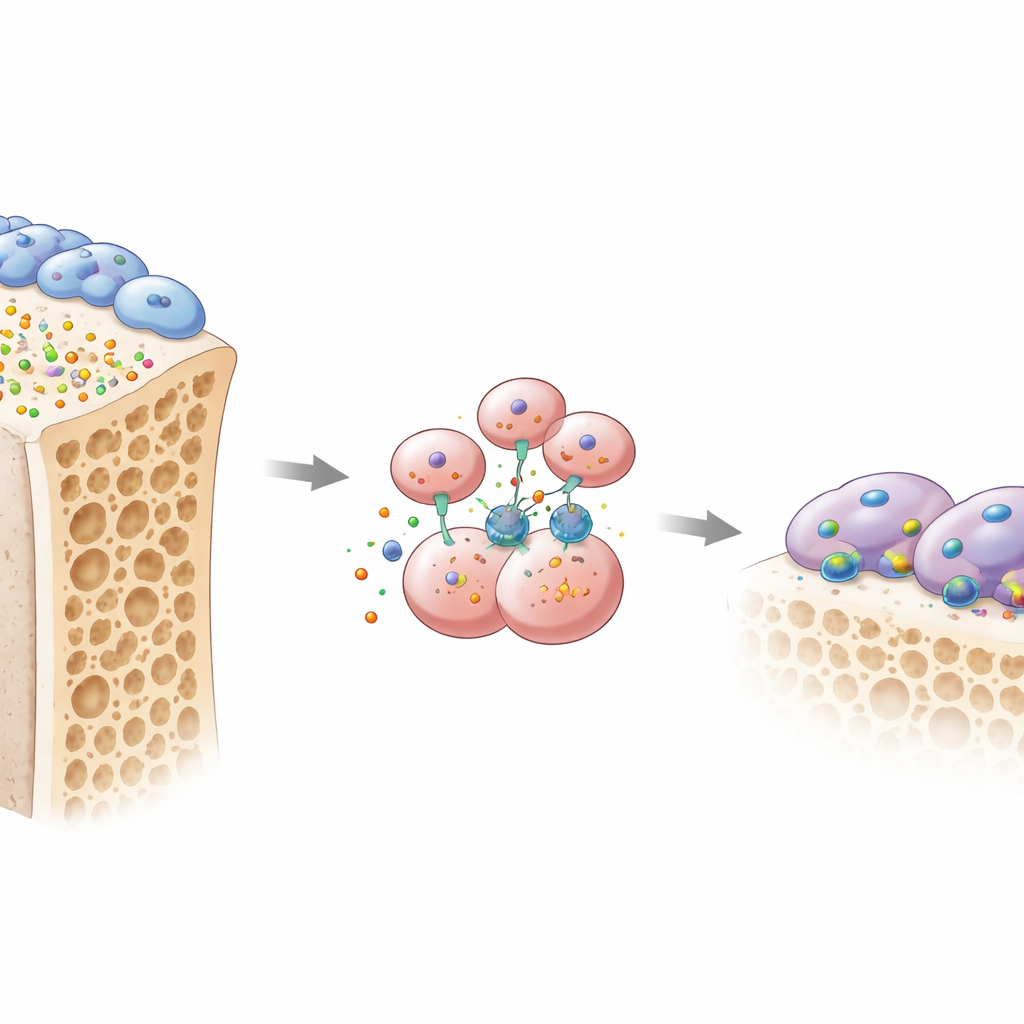
Co się dzieje, gdy hamulec zostaje usunięty
Aby sprawdzić przyczynowość, zespół stworzył myszy pozbawione OMD. Gdy OMD usunięto w całym organizmie lub specyficznie w osteoblastach, zwierzęta traciły znacznie więcej kości gąbczastej i wykazywały wzrost aktywnych osteoklastów żłobiących powierzchnie kostne. W przeciwieństwie do tego, usunięcie OMD jedynie z prekursorów osteoklastów miało niewielki wpływ, co sugeruje, że OMD działa jako sygnał wysyłany przez osteoblasty do sąsiednich komórek resorbujących kość. W hodowlach komórkowych prekursory osteoklastów rozmnażane z osteoblastami produkującymi mało OMD różnicowały się w duże, agresywne osteoklasty. Dodanie oczyszczonego białka OMD odwracało ten obraz: zdecydowanie zmniejszało formowanie się tych wielojądrowych komórek trawiących kość i zaburzało ich wyspecjalizowane struktury „pierścienia uszczelniającego”, których używają do przyczepu i rozpuszczania kości.
Wyłączanie komórkowych elektrowni
Następnie badacze pytali, jak ten sygnał osteoblastów może tak skutecznie hamować osteoklasty. Ich analizy wskazały na metabolizm energetyczny. Osteoklasty są łakome energetycznie i w dużym stopniu polegają na mitochondriach — „elektrowniach” komórkowych — do wytwarzania ATP. Gdy prekursory osteoklastów wystawiono na działanie OMD, spadła ekspresja genów i białek związanych z oddychaniem mitochondrialnym, zmniejszyła się liczba kopii DNA mitochondrialnego, a pomiary bezpośrednie wykazały obniżone zużycie tlenu i produkcję ATP przez mitochondria. Glikoliza, zapasowa ścieżka spalania cukrów, wzrosła tylko nieznacznie i nie była w stanie w pełni zrekompensować. W rezultacie potencjał błony mitochondrialnej spadł, a ogólny profil metaboliczny komórek przesunął się w stronę stanu niedoboru energii. Zmiany te ściśle wiązały się z obniżonym poziomem kluczowej podjednostki enzymu o nazwie RRM2, która pomaga dostarczać cegiełki DNA potrzebne do utrzymania DNA mitochondrialnego.
Krok po kroku: od czujnika na powierzchni do genów
Zaglądając głębiej, zespół odtworzył łańcuch sygnałowy łączący zewnętrzne białko z wewnętrzną kontrolą energetyczną. Stwierdzono, że OMD wiąże się ze specyficznym receptorem, integryną β8, na prekursorach osteoklastów. Ta interakcja tłumiła aktywność molekularnego przełącznika RhoA i zwiększała znakowanie (fosforylację) regulatora YAP, co powodowało opuszczenie jądra przez YAP. Bez partnerstwa YAP z białkami TEAD na DNA, gen Rrm2 został wyciszony. Niższy poziom RRM2 oznaczał mniej cegiełek DNA dla mitochondriów, mniej DNA mitochondrialnego, mniejszą ilość składników łańcucha transportu elektronów i w ostateczności słabszą produkcję mitochondrialnego ATP. Gdy badacze zablokowali RRM2 małą cząsteczką, formowanie osteoklastów i funkcje mitochondrialne spadły podobnie jak po ekspozycji na OMD. Natomiast wymuszenie w komórkach nadprodukcji RRM2 częściowo przywracało ich produkcję energii i rozwój osteoklastów nawet w obecności OMD. 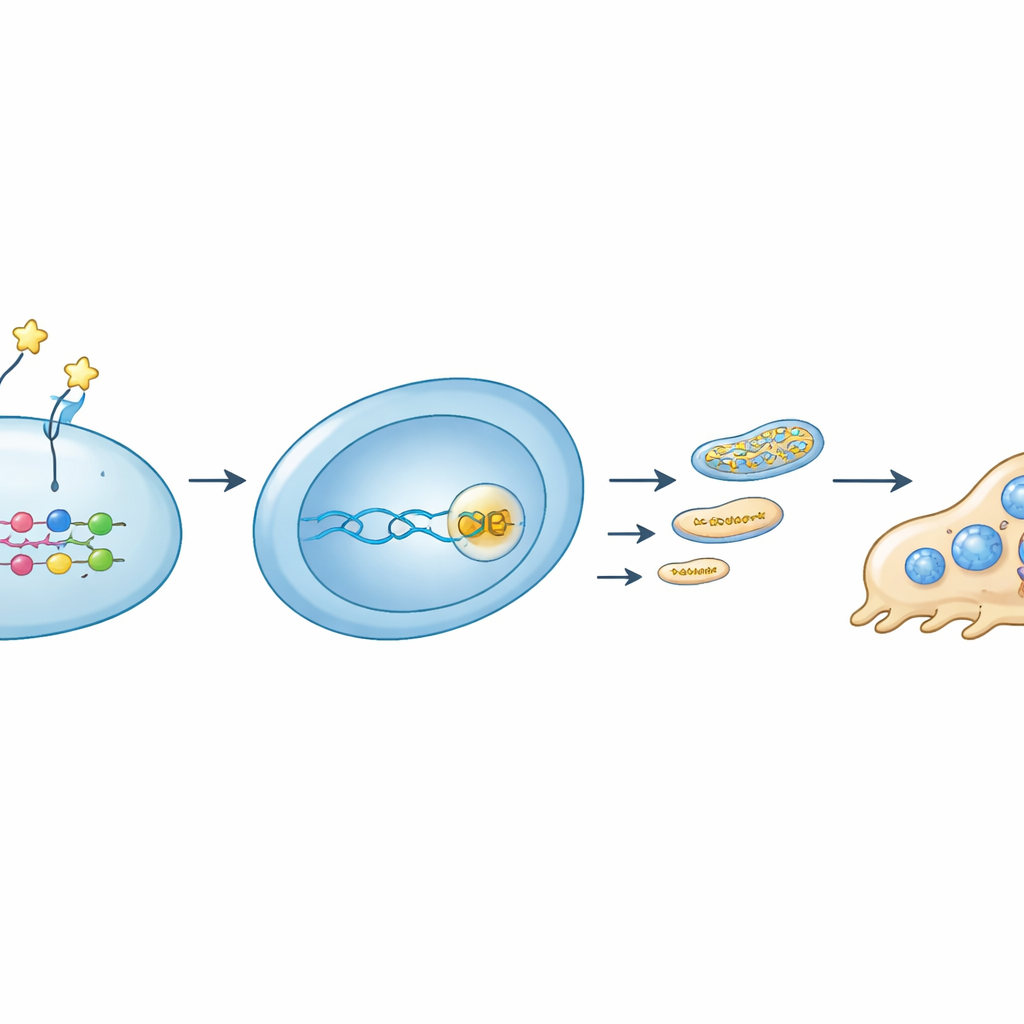
Testowanie potencjalnych nowych podejść terapeutycznych
Na koniec badanie sprawdziło, czy wzmocnienie tego naturalnego hamulca może chronić kości u żywych zwierząt. U myszy, którym usunięto jajniki, by naśladować utratę estrogenów po menopauzie, regularne iniekcje rekombinowanego białka OMD lub lek blokujący RRM2 — osalmid — zachowały strukturę kości. Leczone zwierzęta miały gęstsze beleczkowe kości, mniej osteoklastów i niższe poziomy białek mitochondrialnych w tych osteoklastach. Podobne korzyści zaobserwowano w modelu szybkiej, zapalnej utraty kości wywołanej toksynami bakteryjnymi. Co ważne, krótkotrwałe leczenie nie powodowało widocznych uszkodzeń głównych narządów, choć potrzebne będą dłuższe i dokładniejsze badania bezpieczeństwa.
Co to oznacza dla przyszłej opieki
W sumie praca ujawnia, że osteomodulina działa jako kluczowy mediator spokoju w kości. Produkowana przez osteoblasty, sygnalizuje przez integrynę β8, by przeprogramować prekursorów osteoklastów, dławiając ich mitochondrialne źródło energii tak, by nie mogły nadmiernie rosnąć ani nadmiernie pracować. W osteoporozie ten hamulec wydaje się słabnąć, pozwalając komórkom resorbującym kość stać się bardziej energetycznymi i destrukcyjnymi. Przywracając OMD lub celując w pochodną ścieżkę energetyczną — enzym RRM2 — może być możliwe delikatne spowolnienie rozpadu kości bez jego całkowitego wyłączenia, oferując nowe, oparte na metabolizmie podejście do ochrony starzejącego się szkieletu.
Cytowanie: Jiang, X., Chen, H., Hou, W. et al. Osteoblast-derived osteomodulin restrains osteoclastogenesis via ITGB8/RRM2-mediated reduction of mitochondrial respiration and mitochondrial ATP production. Exp Mol Med 58, 879–897 (2026). https://doi.org/10.1038/s12276-026-01682-7
Słowa kluczowe: osteoporoza, remodelowanie kości, osteoklasty, metabolizm mitochondrialny, osteomodulina