Clear Sky Science · it
L’osteomodulina derivata dagli osteoblasti limita l’osteoclastogenesi tramite la riduzione della respirazione mitocondriale e della produzione di ATP mitocondriale mediata da ITGB8/RRM2
Perché questo conta per le ossa
L’osteoporosi indebolisce silenziosamente le ossa di milioni di persone anziane, in particolare le donne dopo la menopausa. La maggior parte dei farmaci attuali agisce rallentando in modo esteso la degradazione ossea o stimolando la formazione ossea, spesso con effetti collaterali. Questo studio rivela un “freno” naturale incorporato nell’osso: una proteina prodotta dalle cellule che costruiscono osso che indica alle cellule che lo consumano di ridurre il loro consumo energetico e quindi il loro potere distruttivo. Comprendere questo sistema di sicurezza intrinseco potrebbe ispirare terapie per l’osteoporosi più sicure e mirate.
Un segnale nascosto tra le cellule ossee
La salute delle ossa dipende da una continua guerra di trazione tra due tipi cellulari principali. Gli osteoblasti costruiscono nuovo osso, mentre gli osteoclasti dissolvono l’osso vecchio per consentirne il ricambio. Gli autori si sono concentrati su un segnale finora trascurato chiamato osteomodulina, o OMD, una piccola proteina secreta dagli osteoblasti nella matrice ossea. Analizzando diversi grandi dataset genetici provenienti da modelli di osteoporosi, hanno rilevato che il gene per OMD risultava coerentemente downregolato nelle ossa fragili. Nell’esame dei tessuti ossei e del sangue di donne in postmenopausa, quelle con osteoporosi avevano meno OMD sia nell’osso sia nella circolazione, e livelli più bassi di OMD si associavano a marker di rapido riassorbimento osseo. Riduzioni simili sono apparse in un modello murino di osteoporosi da perdita di estrogeni, suggerendo che il calo di OMD è una caratteristica comune dell’indebolimento osseo. 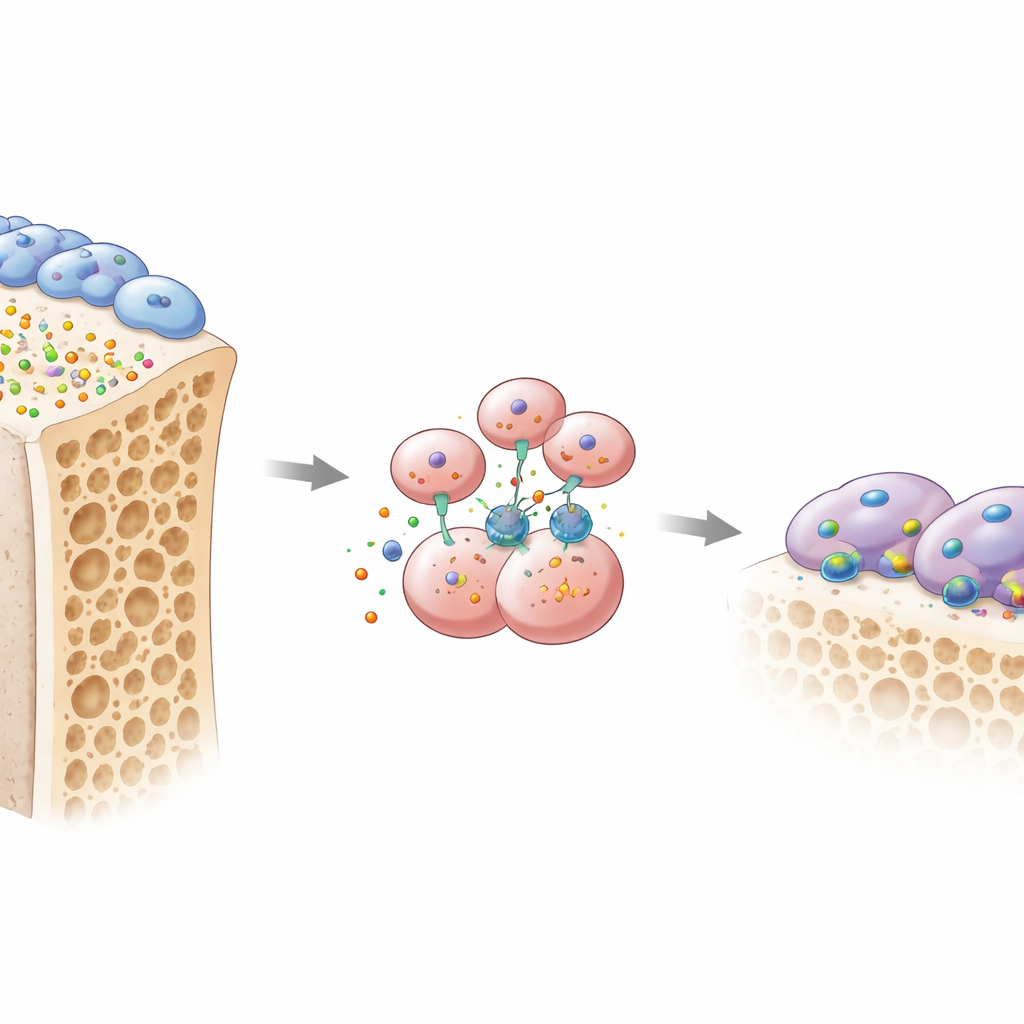
Cosa accade quando il freno viene rimosso
Per testare causa ed effetto, il gruppo ha generato topi privi di OMD. Quando OMD è stato eliminato in tutto l’organismo o specificamente negli osteoblasti, gli animali hanno perso una quantità maggiore di osso trabecolare e hanno mostrato una forte aumento di osteoclasti attivi che scavavano lungo le superfici ossee. Al contrario, l’eliminazione di OMD soltanto nei precursori degli osteoclasti ha avuto scarso impatto, suggerendo che OMD agisca normalmente come un messaggio inviato dagli osteoblasti ai vicini che riassorbono l’osso. In colture cellulari, i precursori degli osteoclasti cresciuti con osteoblasti che producevano poco OMD si sono trasformati in grandi osteoclasti aggressivi. La reintegrazione di OMD purificata ha invertito la situazione: ha ridotto nettamente la formazione di queste cellule multinucleate consumatrici di osso e ha alterato le loro strutture specializzate a “anello di sigillo” usate per aderire e dissolvere l’osso.
Ridurre l’attività delle centrali energetiche cellulari
I ricercatori si sono quindi chiesti come questo segnale da parte degli osteoblasti potesse così potentemente frenare gli osteoclasti. Le loro analisi hanno indicato il metabolismo energetico. Gli osteoclasti sono molto esigenti in termini energetici e dipendono fortemente dai mitocondri, le centrali energetiche della cellula, per generare ATP. Quando i precursori degli osteoclasti sono stati esposti a OMD, i geni e le proteine coinvolti nella respirazione mitocondriale sono diminuiti, le copie di DNA mitocondriale sono calate e misurazioni dirette hanno mostrato un minor consumo di ossigeno e una ridotta produzione di ATP mitocondriale. La glicolisi, una via alternativa di combustione degli zuccheri, è aumentata solo leggermente e non è stata in grado di compensare completamente. Di conseguenza, il potenziale di membrana mitocondriale è diminuito e il profilo metabolico complessivo delle cellule si è spostato verso uno stato di stress energetico. Questi cambiamenti erano strettamente collegati a livelli ridotti di una subunità enzimatica chiave chiamata RRM2, che contribuisce a fornire i mattoni del DNA necessari al mantenimento del DNA mitocondriale.
Una catena passo dopo passo dal sensore di superficie ai geni
Approfondendo, il team ha tracciato una catena di segnalazione che collega una proteina esterna al controllo energetico interno. Si è visto che OMD si lega a un recettore specifico, l’integrina β8, sui precursori degli osteoclasti. Questa interazione ha attenuato l’attività di un interruttore molecolare, RhoA, e ha aumentato la fosforilazione del regolatore YAP, determinando l’uscita di YAP dal nucleo. Senza YAP che collabora con le proteine TEAD sul DNA, il gene Rrm2 si è spento. Meno RRM2 ha significato meno mattoni del DNA per i mitocondri, meno DNA mitocondriale, minore abbondanza di componenti della catena di trasporto degli elettroni e, infine, una ridotta produzione di ATP mitocondriale. Quando i ricercatori hanno bloccato RRM2 con una piccola molecola, la formazione degli osteoclasti e la funzione mitocondriale sono diminuite in modo simile a quanto osservato con OMD. Al contrario, forzare le cellule a produrre RRM2 in eccesso ha parzialmente ripristinato la produzione energetica e lo sviluppo degli osteoclasti anche in presenza di OMD. 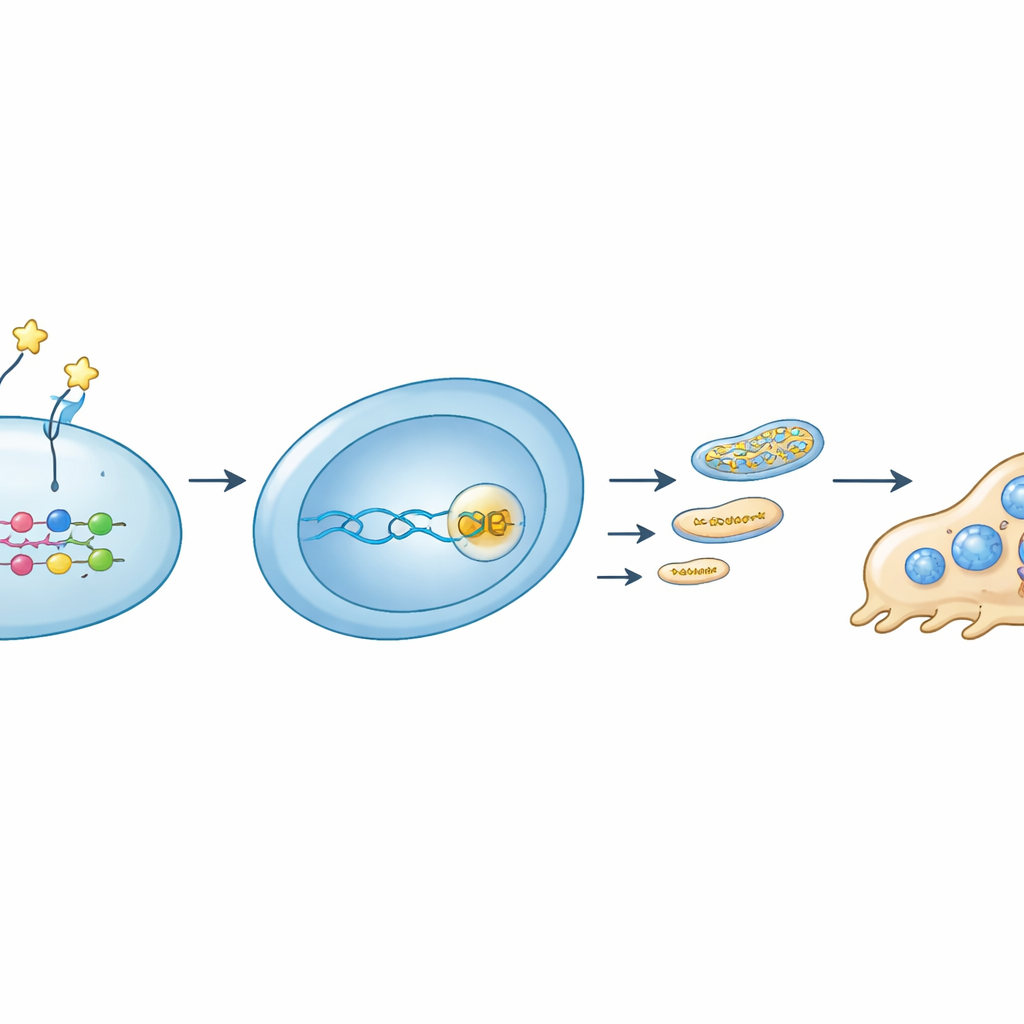
Testare possibili nuove strategie terapeutiche
Infine, lo studio ha verificato se potenziare questo freno naturale potesse proteggere le ossa in animali vivi. In topi sottoposti a ovariectomia per imitare la perdita ossea postmenopausale, iniezioni regolari di proteina OMD ricombinante o del farmaco inibitore di RRM2 osalmide hanno entrambi preservato la struttura ossea. I topi trattati avevano osso trabecolare più denso, meno osteoclasti e livelli più bassi di proteine mitocondriali all’interno di quegli osteoclasti. Benefici simili sono comparsi in un modello di perdita ossea rapida e guidata dall’infiammazione innescata da tossine batteriche. È importante notare che il trattamento a breve termine non ha danneggiato in modo evidente gli organi principali, sebbene siano necessari test di sicurezza più estesi e di lungo periodo.
Cosa significa per le cure future
Complessivamente, il lavoro rivela che l’osteomodulina agisce come un importante paciere nell’osso. Quando prodotta dagli osteoblasti, segnala tramite l’integrina β8 per riprogrammare i precursori degli osteoclasti, limitando il loro apporto energetico mitocondriale così che non possano proliferare o lavorare eccessivamente. Nell’osteoporosi questo freno sembra indebolirsi, permettendo alle cellule riassorbenti di diventare più energetiche e distruttive. Ripristinando OMD o mirandosi sull’enzima energetico a valle RRM2, potrebbe essere possibile rallentare delicatamente il riassorbimento osseo senza spegnerlo completamente, offrendo una nuova strategia focalizzata sul metabolismo per proteggere lo scheletro invecchiante.
Citazione: Jiang, X., Chen, H., Hou, W. et al. Osteoblast-derived osteomodulin restrains osteoclastogenesis via ITGB8/RRM2-mediated reduction of mitochondrial respiration and mitochondrial ATP production. Exp Mol Med 58, 879–897 (2026). https://doi.org/10.1038/s12276-026-01682-7
Parole chiave: osteoporosi, rimodellamento osseo, osteoclasti, metabolismo mitocondriale, osteomodulina