Clear Sky Science · fr
L’ostéomoduline d’origine ostéoblastique freine l’ostéoclastogenèse via une réduction de la respiration mitochondriale et de la production d’ATP mitochondriale médiée par ITGB8/RRM2
Pourquoi cela compte pour les os
L’ostéoporose fragilise silencieusement les os de millions de personnes âgées, en particulier les femmes après la ménopause. La plupart des traitements actuels agissent en ralentissant globalement la résorption osseuse ou en stimulant la formation osseuse, souvent avec des effets indésirables. Cette étude révèle un « frein » naturel intégré à l’os : une protéine produite par les cellules constructrices d’os qui dit aux cellules destructrices de réduire leur consommation d’énergie, et donc leur pouvoir destructeur. Comprendre ce système de sécurité interne pourrait inspirer des traitements de l’ostéoporose plus sûrs et plus ciblés.
Un signal caché entre les cellules osseuses
La santé osseuse dépend d’une lutte d’équilibre continue entre deux types cellulaires principaux. Les ostéoblastes construisent le nouvel os, tandis que les ostéoclastes dissolvent l’ancien os pour qu’il puisse être remplacé. Les auteurs se sont concentrés sur un signal négligé appelé ostéomoduline, ou OMD, une petite protéine sécrétée par les ostéoblastes dans la matrice osseuse. En exploitant plusieurs grandes bases de données génétiques issues de différents modèles d’ostéoporose, ils ont constaté que le gène codant OMD était systématiquement moins exprimé dans les os fragiles. Lorsqu’ils ont examiné des tissus osseux et des échantillons sanguins de femmes postménopausées, celles atteintes d’ostéoporose présentaient moins d’OMD tant dans l’os que dans la circulation, et des niveaux d’OMD plus bas concordaient avec des marqueurs d’une perte osseuse rapide. Des réductions similaires sont apparues dans un modèle murin d’ostéoporose liée à la perte d’œstrogènes, suggérant que le déclin d’OMD est une caractéristique commune de l’affaiblissement osseux. 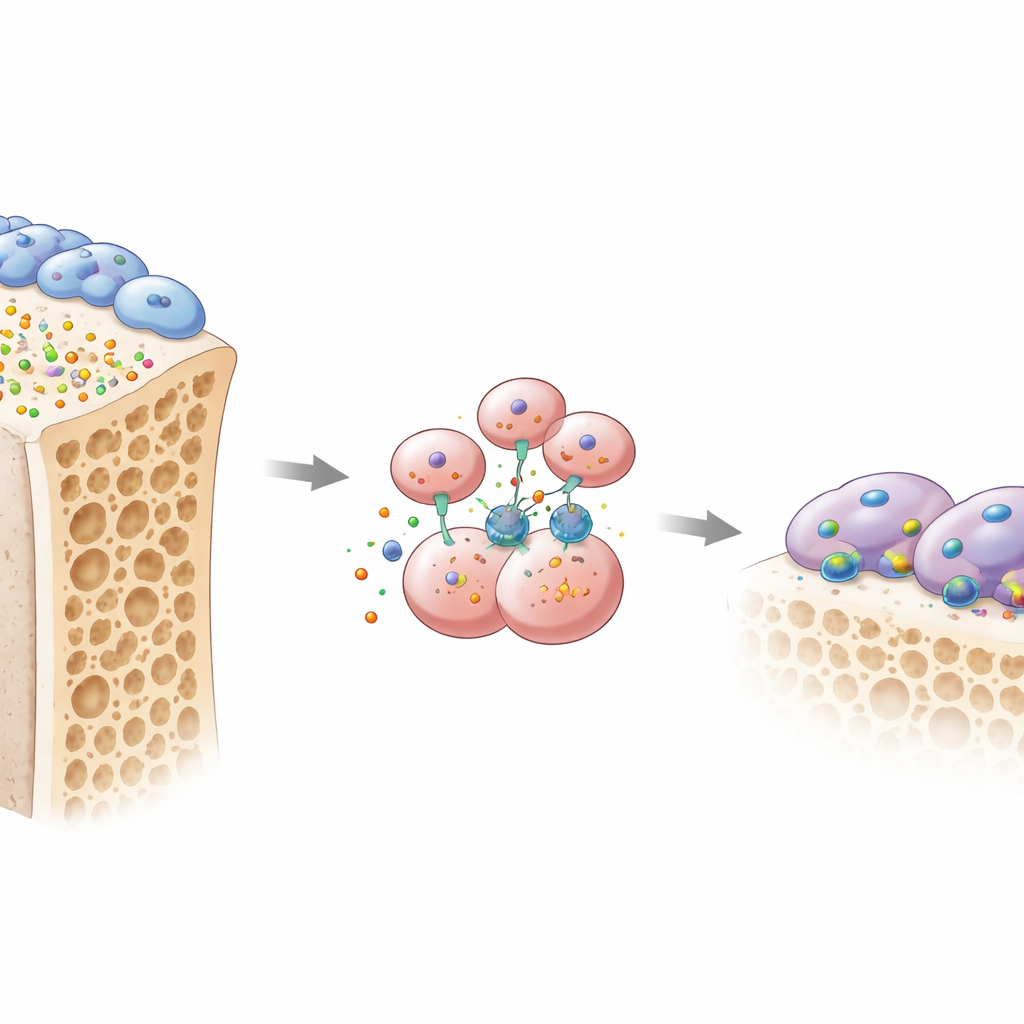
Que se passe-t-il quand le frein est retiré
Pour tester la causalité, l’équipe a modifié génétiquement des souris dépourvues d’OMD. Lorsque OMD était supprimée dans tout l’organisme, ou spécifiquement dans les ostéoblastes, les animaux perdaient beaucoup plus d’os spongieux et présentaient une montée d’ostéoclastes actifs ravageant les surfaces osseuses. En revanche, l’élimination d’OMD uniquement dans les précurseurs d’ostéoclastes avait peu d’impact, ce qui implique qu’OMD agit normalement comme un message envoyé par les ostéoblastes à leurs voisins résorbant l’os. En culture, des précurseurs d’ostéoclastes cultivés avec des ostéoblastes produisant peu d’OMD se sont différenciés en ostéoclastes grands et agressifs. Le réapprovisionnement en protéine OMD purifiée a renversé la situation : il a fortement réduit la formation de ces cellules multinucléées dévoreuses d’os et perturbé leurs structures spécialisées de « bague d’étanchéité » utilisées pour adhérer et dissoudre l’os.
Réduction de l’activité des centrales énergétiques cellulaires
Les chercheurs ont ensuite cherché comment ce signal ostéoblastique pouvait tellement freiner les ostéoclastes. Leurs analyses ont pointé vers le métabolisme énergétique. Les ostéoclastes ont un grand appétit en énergie et dépendent fortement des mitochondries, les centrales énergétiques de la cellule, pour générer de l’ATP. Lorsqu’on exposait les précurseurs d’ostéoclastes à OMD, l’expression des gènes et des protéines impliqués dans la respiration mitochondriale diminuait, le nombre de copies d’ADN mitochondrial baissait, et des mesures directes montraient une consommation d’oxygène et une production d’ATP mitochondriale réduites. La glycolyse, une voie de secours consommant le glucose, augmentait seulement légèrement et ne pouvait pas compenser entièrement. En conséquence, le potentiel de membrane mitochondrial des cellules chutait et leur profil métabolique global basculait vers un état de stress énergétique. Ces changements étaient étroitement liés à la baisse des niveaux d’une sous-unité enzymatique clé appelée RRM2, qui contribue à fournir les précurseurs d’ADN nécessaires au maintien de l’ADN mitochondrial.
Une chaîne étape par étape du capteur de surface aux gènes
En approfondissant, l’équipe a tracé une chaîne de signalisation reliant une protéine externe au contrôle énergétique interne. OMD se lie à un récepteur spécifique, l’intégrine β8, sur les précurseurs d’ostéoclastes. Cette interaction a atténué l’activité d’un interrupteur moléculaire, RhoA, et augmenté le marquage (phosphorylation) du régulateur YAP, provoquant l’exclusion de YAP du noyau. Sans YAP pour s’associer aux protéines TEAD sur l’ADN, le gène Rrm2 s’est mis en silence. Moins de RRM2 signifiait moins de précurseurs d’ADN pour les mitochondries, moins d’ADN mitochondrial, une moindre abondance des composants de la chaîne respiratoire, et in fine une production d’ATP mitochondriale affaiblie. Quand les chercheurs ont bloqué RRM2 avec une petite molécule, la formation d’ostéoclastes et la fonction mitochondriale ont décliné de façon comparable à l’effet d’OMD. À l’inverse, forcer l’expression de RRM2 dans les cellules a partiellement restauré leur production d’énergie et le développement des ostéoclastes même en présence d’OMD. 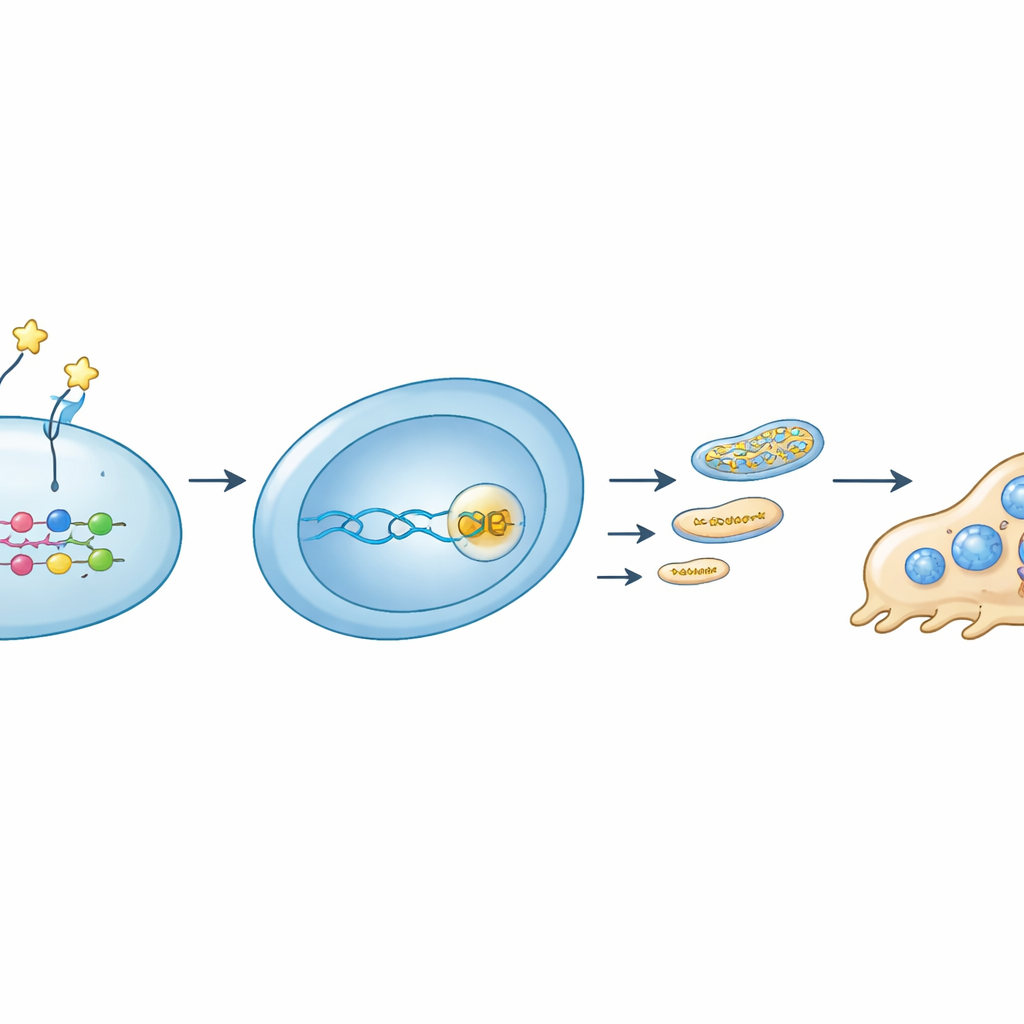
Test d’approches thérapeutiques potentielles
Enfin, l’étude a évalué si renforcer ce frein naturel pouvait protéger les os d’animaux vivants. Chez des souris ovariectomisées pour imiter la perte osseuse postménopausique, des injections régulières de protéine OMD recombinante ou du médicament inhibiteur de RRM2 osalmide ont toutes deux préservé la microarchitecture osseuse. Les rongeurs traités avaient une trame trabéculaire plus dense, moins d’ostéoclastes et des niveaux plus bas de protéines mitochondriales au sein de ces ostéoclastes. Des bénéfices similaires sont apparus dans un modèle de perte osseuse rapide et inflammatoire déclenchée par des toxines bactériennes. Il est important de noter qu’un traitement à court terme n’a pas visiblement endommagé les organes majeurs, même si des tests de sécurité plus longs et détaillés seront nécessaires.
Ce que cela signifie pour les soins futurs
Dans l’ensemble, ce travail révèle que l’ostéomoduline agit comme un gardien essentiel dans l’os. Produite par les ostéoblastes, elle signale via l’intégrine β8 pour reprogrammer les précurseurs d’ostéoclastes, en bridant leur approvisionnement mitochondrial en énergie afin qu’ils ne prolifèrent ni ne s’emballent. Dans l’ostéoporose, ce frein semble s’affaiblir, permettant aux cellules résorbantes de devenir plus énergétiques et destructrices. En restaurant OMD ou en ciblant l’enzyme énergétique en aval RRM2, il pourrait être possible de ralentir doucement la dégradation osseuse sans l’arrêter complètement, offrant une nouvelle stratégie axée sur le métabolisme pour protéger le squelette vieillissant.
Citation: Jiang, X., Chen, H., Hou, W. et al. Osteoblast-derived osteomodulin restrains osteoclastogenesis via ITGB8/RRM2-mediated reduction of mitochondrial respiration and mitochondrial ATP production. Exp Mol Med 58, 879–897 (2026). https://doi.org/10.1038/s12276-026-01682-7
Mots-clés: ostéoporose, remodelage osseux, ostéoclastes, métabolisme mitochondrial, ostéomoduline