Clear Sky Science · es
La osteomodulina derivada de osteoblastos frena la osteoclastogénesis mediante ITGB8/RRM2 al reducir la respiración mitocondrial y la producción de ATP mitocondrial
Por qué esto importa para los huesos
La osteoporosis debilita silenciosamente los huesos de millones de adultos mayores, especialmente las mujeres tras la menopausia. La mayoría de los fármacos actuales actúan ralentizando de forma general la degradación ósea o estimulando la formación de hueso, con frecuencia con efectos secundarios. Este estudio descubre un "freno" natural integrado en el propio hueso: una proteína fabricada por las células formadoras de hueso que indica a las células que consumen hueso que reduzcan su uso de energía y, por tanto, su capacidad destructiva. Comprender este sistema de seguridad incorporado podría inspirar tratamientos contra la osteoporosis más seguros y más dirigidos.
Una señal oculta entre las células óseas
La salud ósea depende de un constante tira y afloja entre dos tipos celulares principales. Los osteoblastos construyen nuevo hueso, mientras que los osteoclastos disuelven el hueso viejo para que pueda ser reemplazado. Los autores se centraron en una señal poco atendida llamada osteomodulina, o OMD, una proteína pequeña secretada por los osteoblastos en la matriz ósea. Al analizar varios grandes conjuntos de datos genéticos de diferentes modelos de osteoporosis, encontraron que el gen de OMD se expresaba de forma consistente a la baja en huesos frágiles. Al examinar tejido óseo y sangre de mujeres posmenopáusicas, las que presentaban osteoporosis tenían menos OMD tanto en el hueso como en la circulación, y niveles bajos de OMD se correlacionaban con marcadores de pérdida ósea rápida. Reducciones similares aparecieron en un modelo murino de osteoporosis por pérdida de estrógenos, lo que sugiere que el descenso de OMD es una característica común del debilitamiento óseo. 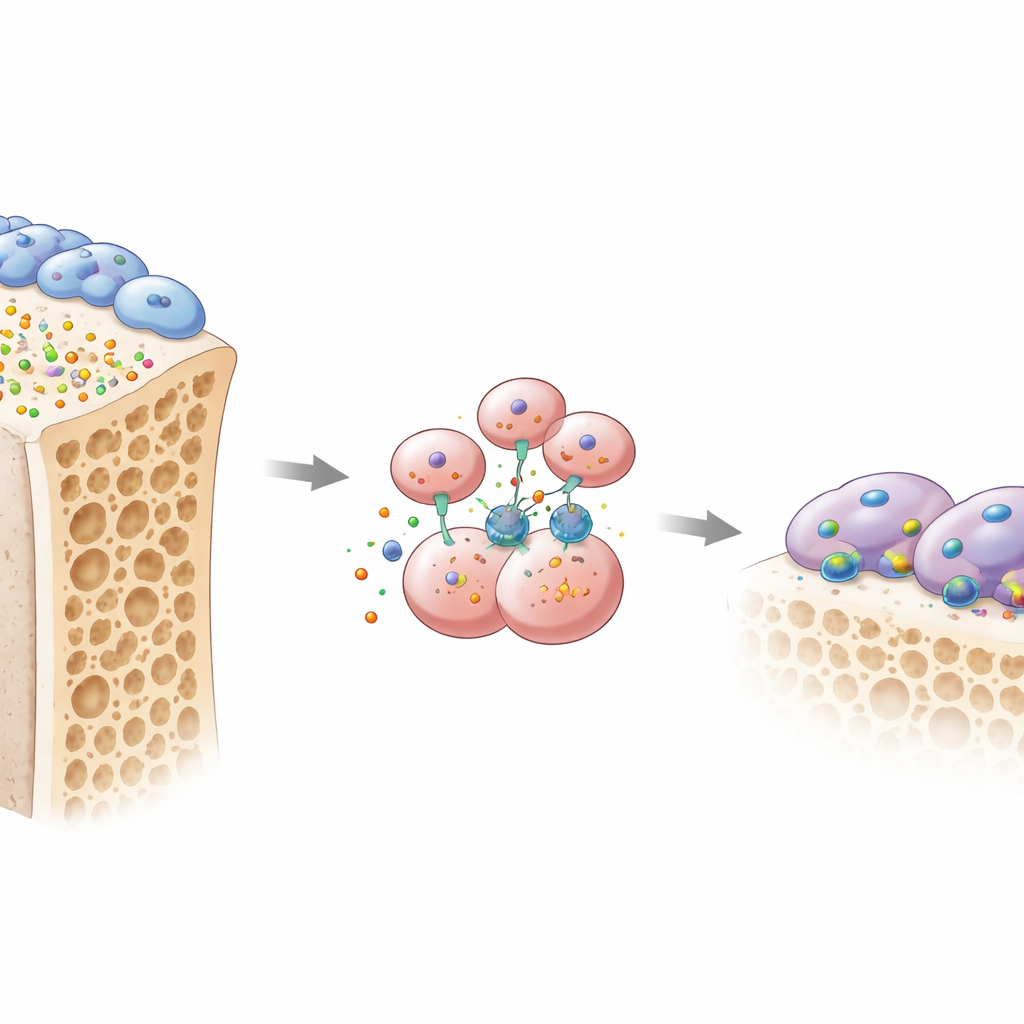
Qué ocurre cuando se quita el freno
Para probar causa y efecto, el equipo creó ratones carentes de OMD. Cuando OMD se eliminó en todo el organismo, o específicamente en los osteoblastos, los animales perdieron mucho más hueso esponjoso y mostraron un aumento de osteoclastos activos que masticaban las superficies óseas. En cambio, eliminar OMD únicamente de los precursores de osteoclastos tuvo poco impacto, lo que implica que OMD actúa normalmente como un mensaje enviado por los osteoblastos a sus vecinos que reabsorben hueso. En cultivos in vitro, los precursores de osteoclastos criados con osteoblastos que producían poca OMD se convirtieron en osteoclastos grandes y agresivos. Volver a añadir OMD purificado cambió la situación: redujo drásticamente la formación de estas células multinucleadas que comen hueso y desorganizó sus estructuras especializadas de "anillo de sellado" que usan para agarrar y disolver el hueso.
Reduciendo la potencia de las centrales celulares
Los investigadores preguntaron entonces cómo esta señal de los osteoblastos podía frenar tan poderosamente a los osteoclastos. Sus análisis apuntaron al metabolismo energético. Los osteoclastos consumen mucha energía y dependen en gran medida de las mitocondrias, las centrales energéticas de la célula, para generar ATP. Cuando los precursores de osteoclastos se expusieron a OMD, descendieron los genes y proteínas implicados en la respiración mitocondrial, disminuyeron las copias de ADN mitocondrial y medidas directas mostraron un menor consumo de oxígeno y producción de ATP por las mitocondrias. La glucólisis, una vía alternativa de consumo de azúcar, aumentó solo ligeramente y no pudo compensar por completo. Como resultado, el potencial de membrana mitocondrial cayó y el perfil metabólico global de las células se desplazó hacia un estado de estrés energético. Estos cambios se vincularon estrechamente con niveles reducidos de una subunidad enzimática clave llamada RRM2, que ayuda a suministrar los bloques de construcción del ADN necesarios para mantener el ADN mitocondrial.
Una cadena paso a paso desde el sensor de la superficie hasta los genes
Abordando el mecanismo en detalle, el equipo rastreó una cadena de señalización que enlaza una proteína externa con el control energético interno. Se descubrió que OMD se une a un receptor específico, la integrina β8, en los precursores de osteoclastos. Esta interacción amortiguó la actividad de un interruptor molecular, RhoA, e incrementó el marcado (fosforilación) del regulador YAP, provocando la salida de YAP del núcleo. Sin YAP asociándose con proteínas TEAD en el ADN, el gen Rrm2 se silenciaba. Menos RRM2 supuso menos bloques de construcción del ADN para las mitocondrias, menos ADN mitocondrial, menor abundancia de componentes de la cadena de transporte de electrones y, en última instancia, menor producción de ATP mitocondrial. Cuando los investigadores bloquearon RRM2 con una pequeña molécula, la formación de osteoclastos y la función mitocondrial disminuyeron de manera similar a lo observado con OMD. A la inversa, forzar a las células a producir RRM2 adicional rescató parcialmente su producción de energía y el desarrollo de osteoclastos incluso en presencia de OMD. 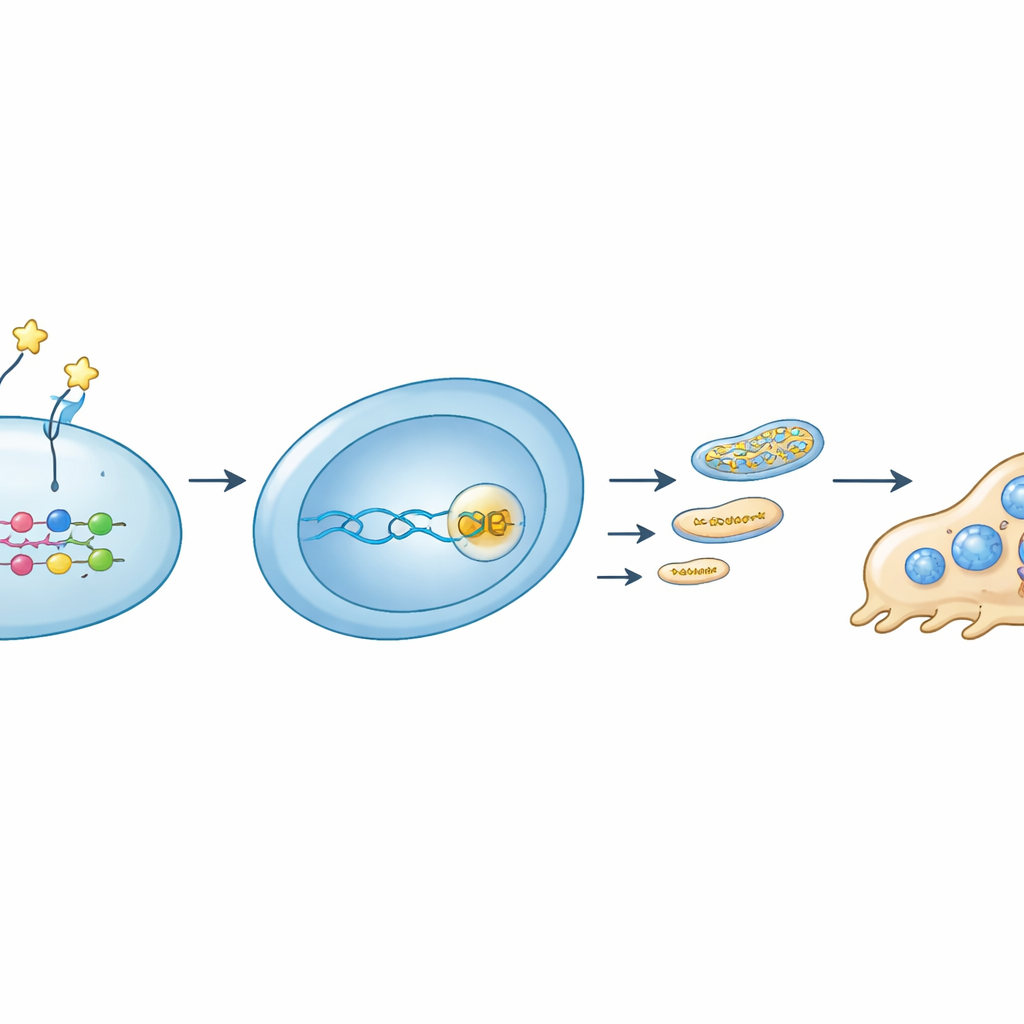
Probando posibles nuevos enfoques terapéuticos
Finalmente, el estudio evaluó si reforzar este freno natural podría proteger los huesos in vivo. En ratones a los que se les extirparon los ovarios para imitar la pérdida ósea posmenopáusica, inyecciones regulares de proteína recombinante OMD o del fármaco que bloquea RRM2, osalmida, preservaron la estructura ósea. Los ratones tratados tenían mayor densidad del hueso trabecular, menos osteoclastos y niveles más bajos de proteínas mitocondriales en esos osteoclastos. Beneficios similares se observaron en un modelo de pérdida ósea rápida impulsada por inflamación y desencadenada por toxinas bacterianas. Es importante señalar que el tratamiento a corto plazo no dañó visiblemente los principales órganos, aunque serán necesarias pruebas de seguridad más prolongadas y detalladas.
Qué significa esto para la atención futura
En conjunto, el trabajo revela que la osteomodulina actúa como un pacificador crucial en el hueso. Cuando la producen los osteoblastos, señaliza a través de la integrina β8 para reprogramar a los precursores de osteoclastos, reduciendo su suministro energético mitocondrial para que no crezcan ni trabajen en exceso. En la osteoporosis, este freno parece debilitarse, permitiendo que las células reabsorbentes se vuelvan más enérgicas y destructivas. Restaurar OMD o dirigirse a la enzima energética downstream RRM2 podría permitir frenar suavemente la degradación ósea sin detenerla por completo, ofreciendo una nueva estrategia centrada en el metabolismo para proteger el esqueleto envejecido.
Cita: Jiang, X., Chen, H., Hou, W. et al. Osteoblast-derived osteomodulin restrains osteoclastogenesis via ITGB8/RRM2-mediated reduction of mitochondrial respiration and mitochondrial ATP production. Exp Mol Med 58, 879–897 (2026). https://doi.org/10.1038/s12276-026-01682-7
Palabras clave: osteoporosis, remodelado óseo, osteoclastos, metabolismo mitocondrial, osteomodulina