Clear Sky Science · he
אוסטאובלאסט-מופק אוסטאומודולין מעכב אוסטאוקלסטוגנזה באמצעות הפחתה בנשימה המיטוכונדריאלית ובהפקת ATP מיטוכונדריאלית בתיווך ITGB8/RRM2
מדוע זה חשוב לעצמות
אוסטאופורוזיס מחליש בעדינות את העצמות במיליוני מבוגרים, במיוחד נשים אחרי מנופאוזה. רוב התרופות הנוכחיות פועלות על ידי האטה כוללת של פירוק העצם או הגברת בנייתה, לעתים עם תופעות לוואי. המחקר הזה חושף "בלם" טבעי המוטמע בעצם עצמה: חלבון המיוצר על ידי תאי בניית העצם שמורה לתאי אכילת העצם להקטין את צריכת האנרגיה שלהם, ובכך את יכולת ההרס שלהם. הבנה של מערכת בטיחות פנימית זו עשויה להניע פיתוח טיפולים בטוחים וממוקדים יותר לאוסטאופורוזיס.
אות מוסתר בין תאי עצם
בריאות העצם נשענת על מאבק מתמשך בין שני סוגי תאים עיקריים. אוסטאובלאסטים בונים עצם חדשה, בעוד אוסטאוקלסטים ממסים עצם ישנה כדי לאפשר החלפה. המחברים התרכזו באיתות שזכה להתעלמות יחסית בשם אוסטאומודולין, או OMD, חלבון קטן המופרש על ידי אוסטאובלאסטים למטריקס העצם. על ידי כריית מספר מאגרי גנטיקה גדולים ממודלים שונים של אוסטאופורוזיס, הם מצאו שגן OMD דוכא בעקביות בעצמות שבריריות. בבחינת רקמת עצם ודם מנשים לאחר מנופאוזה, אלה עם אוסטאופורוזיס הציגו פחות OMD הן בעצם והן במחזור הדם, ורמות OMD נמוכות נקשרו לסמנים של אובדן עצם מהיר. הפחתות דומות הופיעו גם במודל עכבר לאוסטאופורוזיס כתוצאה מאובדן אסטרוגן, מה שמרמז שירידת OMD היא תכונה נפוצה של עצם שמחלישה. 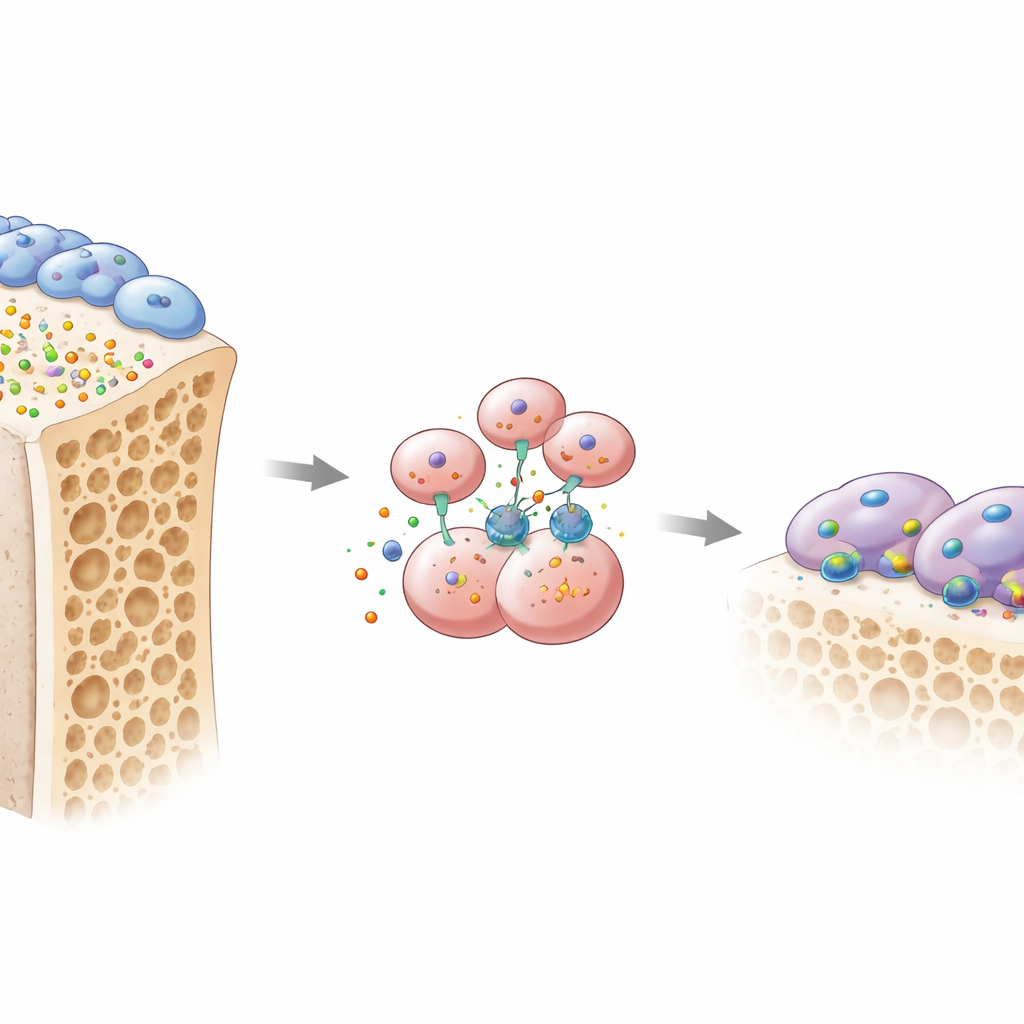
מה קורה כשמוסרים את הבלם
כדי לבדוק סיבה ותוצאה, הצוות מהנדס עכברים חסרי OMD. כאשר OMD הוסר בכל הגוף, או ספציפית באוסטאובלאסטים, בעלי החיים איבדו הרבה יותר עצם ספוגי והציגו פרץ של אוסטאוקלסטים פעילים המלעסים לאורך משטחי העצם. לעומת זאת, הסרת OMD רק מקדמונים לאוסטאוקלסטים השאירה כמעט ללא השפעה, מה שמעיד ש-OMD בדרך כלל פועלת כהודעה שנשלחת מאוסטאובלאסטים לשכני פירוק העצם שלהם. במעבדות, קדמוני אוסטאוקלסט שגדלו לצד אוסטאובלאסטים שמייצרים מעט OMD התמיינו לאוסטאוקלסטים גדולים ואגרסיביים. החזרת חלבון OMD מטוהר הפכה את המגמה: היא צמצמה במידה ניכרת את היווצרות התאים הרב־גרעיניים האלו והפריעה למבני "טבעת ההידוק" המיוחדים שבהם הם משתמשים כדי לאחוז ולמוסס עצם.
הורדת כוחות תחנות הכוח התאית
החוקרים שאלו כיצד אות האוסטאובלאסט הזה מעכב כל כך בעוצמה את האוסטאוקלסטים. הניתוחים שלהם הצביעו על מטבוליזם אנרגטי. אוסטאוקלסטים רעבים לאנרגיה ותלויים במידה רבה במיטוכונדריה, תחנות הכוח של התא, לייצור ATP. כאשר קדמוני אוסטאוקלסט נחשפו ל-OMD, גנים וחלבונים המעורבים בנשימה המיטוכונדריאלית ירדו, עותקי DNA מיטוכונדריאלי פחתו, ומדידות ישירות הראו שימוש חמצן נמוך יותר והפקת ATP מיטוכונדריאלית מופחתת. גליקוליזה, מסלול חמצון סוכר משלים, עלתה במעט בלבד ולא הצליחה לפצות במלואה. כתוצאה מכך פוטנציאל הממברנה המיטוכונדריאלי ירד והפרופיל המטבולי הכולל של התאים השתנה למצב של לחץ אנרגטי. שינויים אלה היו קשורים באופן הדוק לירידה ברמות תת־יחידת האנזים המרכזית RRM2, המסייעת באספקת אבני הבניין של ה-DNA הנדרשים לשימור ה-DNA המיטוכונדריאלי.
שרשרת שלב אחר שלב מחיישן שטחי לגנים
בעומק נוסף, הצוות שחזר מסלול איתות המקשר חלבון חיצוני לשליטה אנרגטית פנימית. נמצא ש-OMD נקשר לקולטן ספציפי, אינטגרין β8, על קדמוני האוסטאוקלסטים. אינטראקציה זו דיכאה את פעילות המתג המולקולרי RhoA והגבירה את תיוג הפוספורילציה של המסדר YAP, שגרם ליציאת YAP מהגרעין. ללא שותפותו של YAP עם חלבוני TEAD על ה-DNA, גן Rrm2 דוכא. רמות נמוכות של RRM2 פירושן פחות אבני בניין ל-DNA של המיטוכונדריה, פחות DNA מיטוכונדריאלי, ירידה בשפע רכיבי שרשרת הטרנספורט האלקטרוני, ולבסוף תפוקת ATP מיטוכונדריאלית חלשה יותר. כאשר החוקרים חסמו את RRM2 באמצעות מולקולה קטנה, היווצרות האוסטאוקלסטים ותפקוד המיטוכונדריה ירדו באופן דומה למה שנצפה תחת OMD. להיפך, אילוץ התאים לייצר RRM2 עודף הציל חלקית את ייצור האנרגיה וההתפתחות של האוסטאוקלסטים גם בנוכחות OMD. 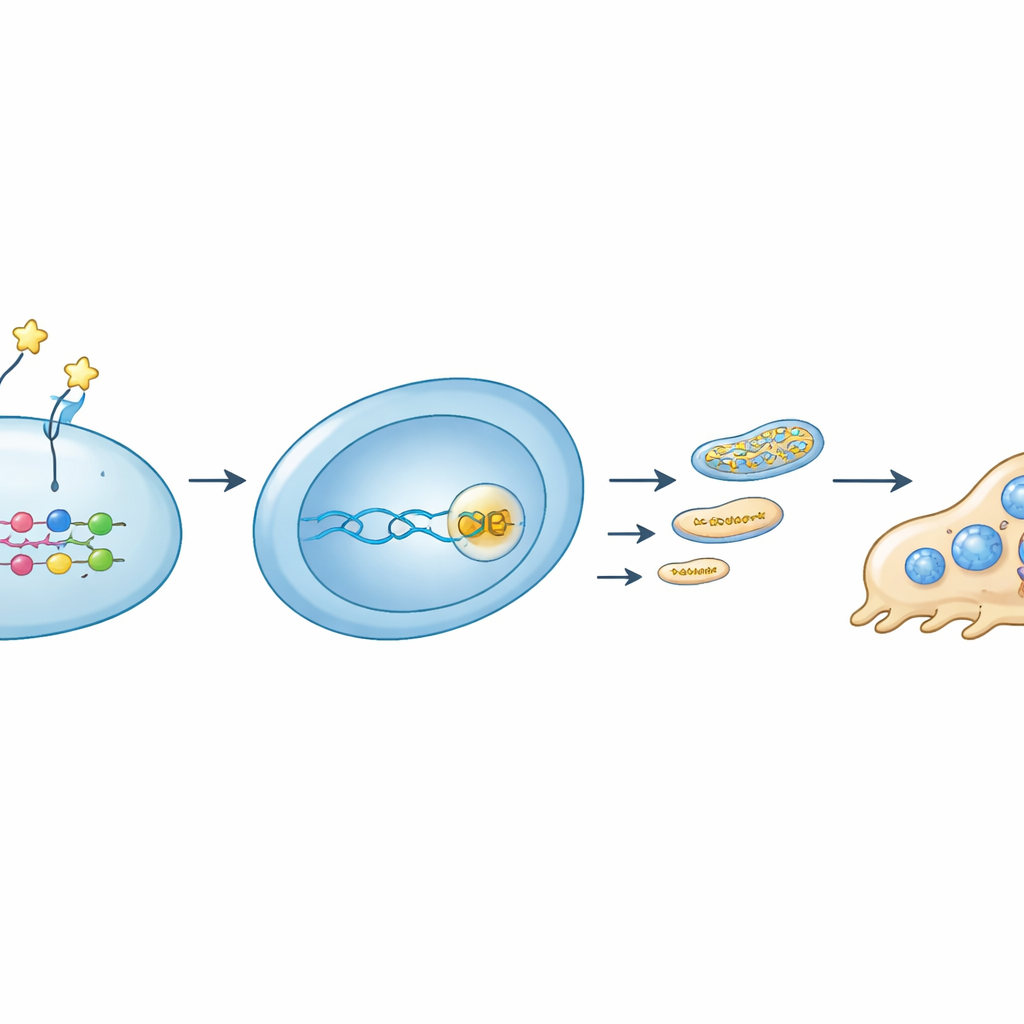
בדיקת אסטרטגיות טיפוליות פוטנציאליות
לבסוף, המחקר בדק האם הגברה של הבלם הטבעי הזה יכולה להגן על עצמות בחי. בעכברים שעברו כריתת שחלה כדי לדמות אובדן עצם שאחרי מנופאוזה, הזרקות קבועות של חלבון OMD רקומביננטי או של תרופה חוסמת RRM2, אוזאלמיד, שימרו את מבנה העצם. בעכברים מטופלים היה צפיפות גבוהה יותר בעצם הסחוסית, פחות אוסטאוקלסטים ורמות נמוכות יותר של חלבונים מיטוכונדריאליים בתוך אותם אוסטאוקלסטים. יתרונות דומים נצפו במודל של אובדן עצם מהיר מונע-דלקת באמצעות רעלני חיידקים. חשוב לציין שטיפול קצר-טווח לא פגע באופן נראה לעין באיברים מרכזיים, אם כי נדרש ניסוי בטיחות ארוך ומפורט יותר.
מתי זה משנה לטיפול עתידי
בסיכום, הממצא מראה שאוסטאומודולין פועל כמגשר חיוני של שלום בעצם. כאשר הוא מיוצר על ידי אוסטאובלאסטים, הוא משדר דרך אינטגרין β8 כדי לתכנת מחדש קדמוני אוסטאוקלסטים, מצמצם את אספקת הכוח המיטוכונדריאלית שלהם כך שלא יוכלו להתפתח יתר על המידה או לפעול ביתר. באוסטאופורוזיס, הבלם הזה נראה כמתחלש, ומאפשר לתאי פירוק העצם להפוך לאנרגטיים והרסניים יותר. על ידי השבת OMD או מיקוד באנזים האנרגטי התחתון RRM2, ייתכן שאפשר להאט בעדינות את פירוק העצם מבלי לכבותו לחלוטין, ולהציע אסטרטגיה חדשה ממוקדת־מטבוליזם להגנה על שלד המזדקן.
ציטוט: Jiang, X., Chen, H., Hou, W. et al. Osteoblast-derived osteomodulin restrains osteoclastogenesis via ITGB8/RRM2-mediated reduction of mitochondrial respiration and mitochondrial ATP production. Exp Mol Med 58, 879–897 (2026). https://doi.org/10.1038/s12276-026-01682-7
מילות מפתח: אוסטאופורוזיס, חידוש עצם, אוסטאוקלסטים, מטבוליזם מיטוכונדריאלי, אוסטאומודולין