Clear Sky Science · ar
الأوستيوبلاست المُنتِج للأوستيومودولين يقيّد تكوّن ناقِرات العظم عبر خفض التنفّس الميتوكوندري وإنتاج ATP الميتوكوندري بواسطة ITGB8/RRM2
لماذا يهم هذا العظام
هشاشة العظام تُضعف العظام بصمت لدى ملايين البالغين الأكبر سناً، وخصوصاً النساء بعد انقطاع الطمث. تعمل معظم الأدوية الحالية عبر إبطاء تكسُّر العظم بشكل عام أو تعزيز بناء العظم، وغالباً ما تصاحبها آثار جانبية. تكشف هذه الدراسة عن "مكابح" داخلية طبيعية في العظم نفسه: بروتين تصنعه خلايا بناء العظم يخبر الخلايا الهادمة للعظم بتقليل استهلاكها للطاقة، وبالتالي تقليل قدرتها التدميرية. فهم هذا النظام الوقائي المدمج قد يلهم علاجات هشاشة عظام أكثر أماناً وأكثر استهدافاً.
إشارة خفيّة بين خلايا العظم
تعتمد صحة العظم على صراع مستمر بين نوعين رئيسيين من الخلايا. تبني الأوستيوبلاستات عظمًا جديدًا، بينما تحلّ الأوستيوكلاستات العظم القديم ليجري استبداله. ركز المؤلفون على إشارة مهملة تُدعى أوستيومودولين، أو OMD، وهو بروتين صغير تفرزه الأوستيوبلاستات إلى مصفوفة العظم. من خلال تنقيبهم في عدة مجموعات بيانات جينية كبيرة من نماذج هشاشة عظام مختلفة، وجدوا أن جين OMD كان مـُثبَّطًا باستمرار في العظام الهشة. عندما فحصوا نسيج العظم والدم من نساء بعد انقطاع الطمث، كان لدى المصابات بهشاشة العظام مستويات أقل من OMD في كل من العظم والدورة الدموية، وكان انخفاض مستويات OMD مرتبطًا بعلامات فقدان العظم السريع. ظهرت انخفاضات مماثلة في نموذج فأري لهشاشة العظام الناجمة عن فقدان الإستروجين، ما يوحي بأن تراجع OMD سمة شائعة للعظام الضعيفة. 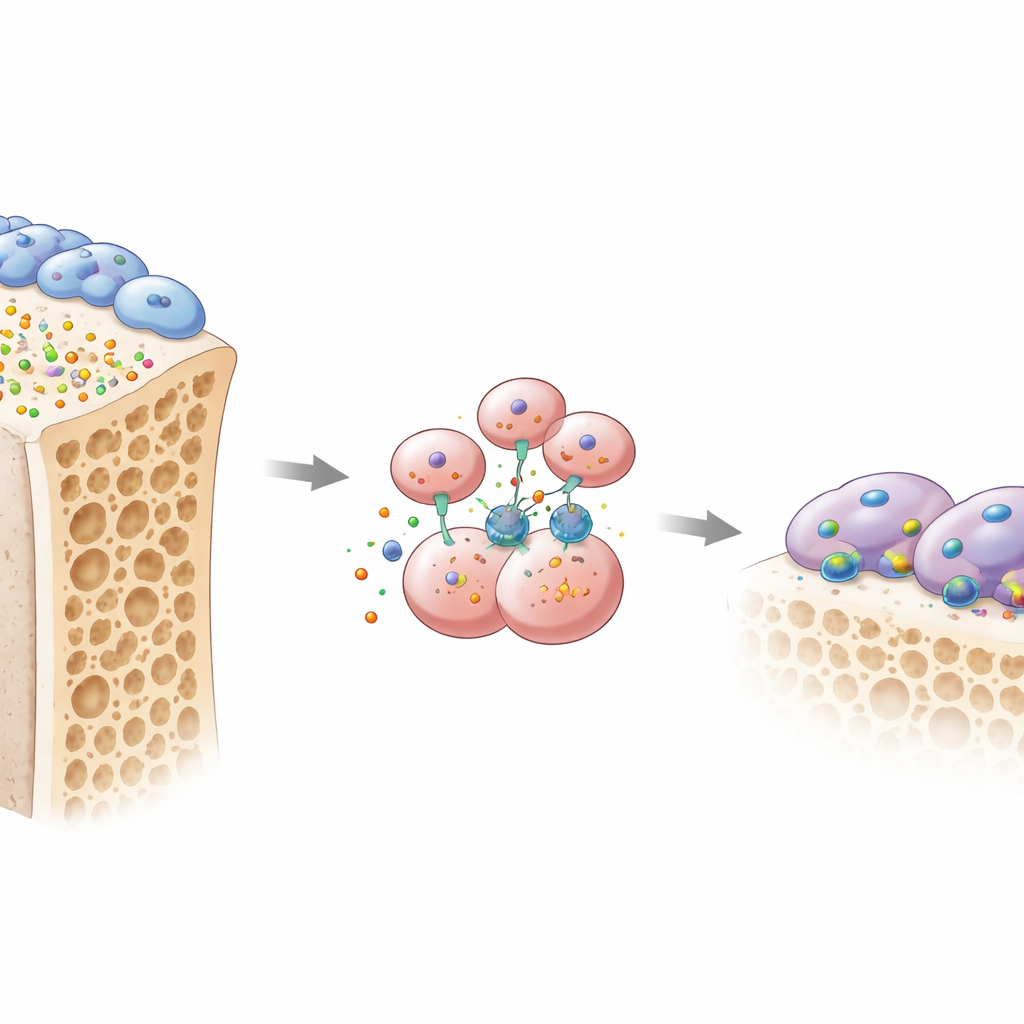
ماذا يحدث عند إزالة المكبح
لاختبار السببية، هندس الفريق فئرانًا تفتقر إلى OMD. عندما حُذِف OMD في الجسم كله، أو خصيصًا في الأوستيوبلاستات، فقدت الحيوانات قدرًا أكبر من العظم الإسفنجي وظهرت زيادة في الأوستيوكلاستات النشطة التي تأكل على طول أسطح العظم. بالمقابل، لم يَسفر إزالة OMD فقط من الخلايا السلفية للأوستيوكلاستات عن تأثير كبير، مما يوحي بأن OMD يعمل عادة كرسالة مرسلة من الأوستيوبلاستات إلى جيرانها الهادمين للعظم. في الأطباق المختبرية، تحولت الخلايا السلفية للأوستيوكلاستات المزروعة مع أوستيوبلاستات تصنع القليل من OMD إلى أوستيوكلاستات كبيرة وعدوانية. إعادة إضافة بروتين OMD النقي بدلت النتيجة: فقد قلّلت بشكل حاد من تكوّن هذه الخلايا متعددة النوى الهادمة للعظم وأعاقت هياكلها المتخصصة "حلقة الختم" التي تستخدمها للتماسك وإذابة العظم.
خفض محطات الطاقة الخلوية
سأل الباحثون بعد ذلك كيف يمكن لإشارة الأوستيوبلاست أن تكبح الأوستيوكلاستات بهذه القوة. أشارت تحليلاتهم إلى استقلاب الطاقة. الأوستيوكلاستات خلايا نهمة للطاقة وتعتمد بشكل كبير على الميتوكوندريا، محطات طاقة الخلية، لتوليد ATP. عندما تعرضت الخلايا السلفية للأوستيوكلاستات لـOMD، انخفضت الجينات والبروتينات المشاركة في التنفّس الميتوكوندري، تراجعت نسخ DNA الميتوكوندري، وأظهرت القياسات المباشرة انخفاضًا في استخدام الأكسجين وإنتاج ATP عبر الميتوكوندريا. ارتفع التحلّل السكري (التحلل السكري الخلوي)، وهو مسار احتياطي لحرق السكر، بشكل طفيف فقط ولم يتمكن من التعويض الكامل. ونتيجة لذلك، انخفض الجهد الغشائي الميتوكوندري وتحوّل الملف الأيضي العام للخلايا نحو حالة إجهاد طاقي. ارتبطت هذه التغيرات ارتباطًا وثيقًا بانخفاض مستويات وحدة إنزيمية رئيسية تُدعى RRM2، التي تساعد في تزويد اللبنات الأساسية للحمض النووي اللازمة للحفاظ على DNA الميتوكوندري.
سلسلة خطوة بخطوة من حسّاس السطح إلى الجينات
بتعمّق أكبر، تعقّب الفريق سلسلة إشارية تربط بروتينًا خارجيًا بضبط الطاقة الداخلي. وُجد أن OMD يرتبط بمستقبل محدد، إنتغرين β8، على الخلايا السلفية للأوستيوكلاستات. قللت هذه التفاعلات من نشاط مفتاح جزيئي، RhoA، وزادت من وضع العلامات (الفوسفorylation) للمُنظِم YAP، مما أدى إلى خروج YAP من النواة. بدون شراكة YAP مع بروتينات TEAD على الحمض النووي، كَفَّ جين Rrm2 عن النشاط. يعني انخفاض RRM2 توفرًا أقل من اللبنات الأساسية للـDNA للميتوكوندريا، انخفاضًا في DNA الميتوكوندري، تناقصًا في مكوّنات سلسلة نقل الإلكترون، وفي النهاية انخفاضًا في إنتاج ATP الميتوكوندري. عندما قام الباحثون بحجب RRM2 بجزيء صغير، انخفض تكوّن الأوستيوكلاستات ووظيفة الميتوكوندريا بطريقة مماثلة لما حدث تحت تأثير OMD. وعلى العكس، إن إجبار الخلايا على إنتاج RRM2 إضافي أنقذ جزئيًا إنتاج طاقتها وتطور الأوستيوكلاستات حتى في وجود OMD. 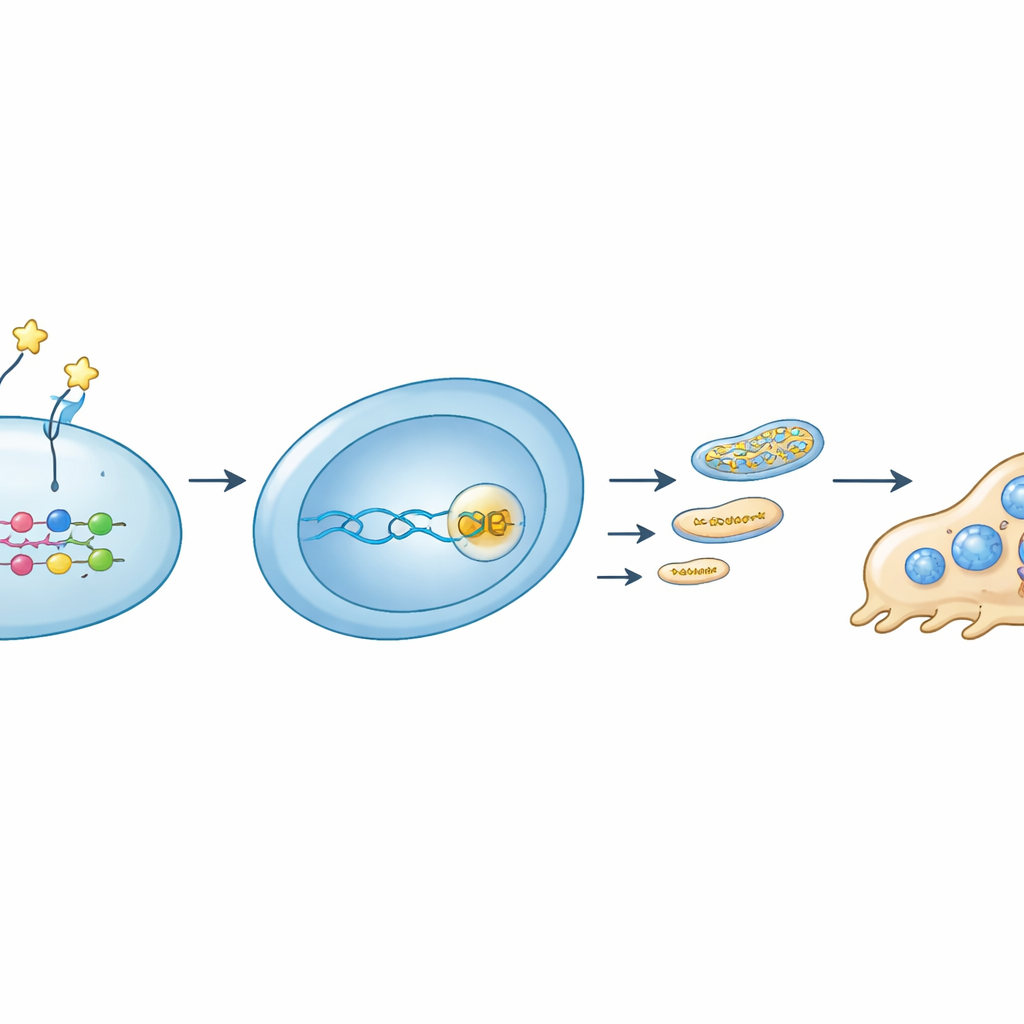
اختبار زوايا علاجية محتملة جديدة
أخيرًا، سأل البحث ما إذا كان تعزيز هذا المكبح الطبيعي يمكن أن يحمي العظام في الحيوانات الحية. في فئران أُزيلت مبايضها لمحاكاة فقدان العظم بعد انقطاع الطمث، حافظت الحقن المنتظمة ببروتين OMD المألق أو الدواء المحجب لـRRM2 أوزالميْد على بنية العظم. أظهرت الفئران المعالجة كثافة أكبر في العظم الشبكي، عددًا أقل من الأوستيوكلاستات، ومستويات أقل من البروتينات الميتوكوندرية داخل تلك الأوستيوكلاستات. ظهرت فوائد مماثلة في نموذج لفقدان العظم السريع الناجم عن الالتهاب المحفز بسموم بكتيرية. ومن المهم أن العلاج قصير المدى لم يَبدُ أنه يضرّ بالأعضاء الرئيسية ظاهريًا، رغم أن اختبارات سلامة أطول وأكثر تفصيلاً ستكون مطلوبة.
ما الذي يعنيه هذا للرعاية المستقبلية
مجتمعة، تكشف هذه النتائج أن الأوستيومودولين يعمل كحافظ سلام أساسي في العظم. عندما تُنتَج الأوستيوبلاستات هذا البروتين، فإنها تُرسِل إشارة عبر الإنتغرين β8 لإعادة برمجة الخلايا السلفية للأوستيوكلاستات، مقيّدةً إمدادات طاقتها الميتوكوندرية حتى لا تفرط في النمو أو النشاط. في هشاشة العظام، يبدو أن هذا المكبح يضعف، مما يسمح لخلايا هدم العظم بأن تصبح أكثر طاقة وتدميرية. من خلال استعادة OMD أو استهداف الإنزيم الطاقي اللاحق RRM2، قد يكون من الممكن إبطاء تكسير العظم برفق دون إيقافه كليًا، ما يوفّر استراتيجية جديدة تركز على الاستقلاب لحماية الهيكل العظمي المتقدم في السن.
الاستشهاد: Jiang, X., Chen, H., Hou, W. et al. Osteoblast-derived osteomodulin restrains osteoclastogenesis via ITGB8/RRM2-mediated reduction of mitochondrial respiration and mitochondrial ATP production. Exp Mol Med 58, 879–897 (2026). https://doi.org/10.1038/s12276-026-01682-7
الكلمات المفتاحية: هشاشة العظام, إعادة تشكيل العظم, الخلايا الهادمة للعظم (أوستيوكلاست), استقلاب الميتوكوندريا, أوستيومودولين