Clear Sky Science · de
Von Osteoblasten stammendes Osteomodulin hemmt die Osteoklastogenese über ITGB8/RRM2-vermittelte Reduktion der mitochondrialen Atmung und der mitochondrialen ATP-Produktion
Warum das für Knochen wichtig ist
Osteoporose schwächt leise die Knochen von Millionen älterer Menschen, besonders Frauen nach den Wechseljahren. Die meisten derzeit verfügbaren Medikamente wirken, indem sie den Knochenabbau allgemein bremsen oder die Knochenbildung anregen, oft mit Nebenwirkungen. Diese Studie deckt eine natürliche „Bremse“ im Knochen selbst auf: ein von knochenaufbauenden Zellen produziertes Protein, das den knochenabbauenden Zellen sagt, ihren Energieverbrauch zu drosseln und damit ihre zerstörerische Kraft zu verringern. Das Verständnis dieses eingebauten Sicherheitsmechanismus könnte sicherere, gezieltere Behandlungsansätze gegen Osteoporose inspirieren.
Ein verstecktes Signal zwischen Knochenzellen
Die Knochengesundheit beruht auf einem ständigen Tauziehen zwischen zwei Hauptzelltypen. Osteoblasten bauen neuen Knochen auf, während Osteoklasten alten Knochen auflösen, damit er ersetzt werden kann. Die Autoren konzentrierten sich auf ein bislang wenig beachtetes Signal namens Osteomodulin oder OMD, ein kleines von Osteoblasten in die Knochenmatrix ausgeschiedenes Protein. Beim Durchsuchen mehrerer großer genetischer Datensätze aus unterschiedlichen Osteoporose-Modellen stellten sie fest, dass das Gen für OMD in brüchigen Knochen durchgängig herunterreguliert war. Bei der Untersuchung von Knochengewebe und Blut postmenopausaler Frauen hatten jene mit Osteoporose weniger OMD sowohl im Knochen als auch im Blutkreislauf, und niedrigere OMD-Spiegel korrelierten mit Markern schnellen Knochenabbaus. Ähnliche Abnahmen zeigten sich in einem Mausmodell der Östrogenmangel-induzierten Osteoporose, was nahelegt, dass der Rückgang von OMD ein gemeinsames Merkmal schwächer werdender Knochen ist. 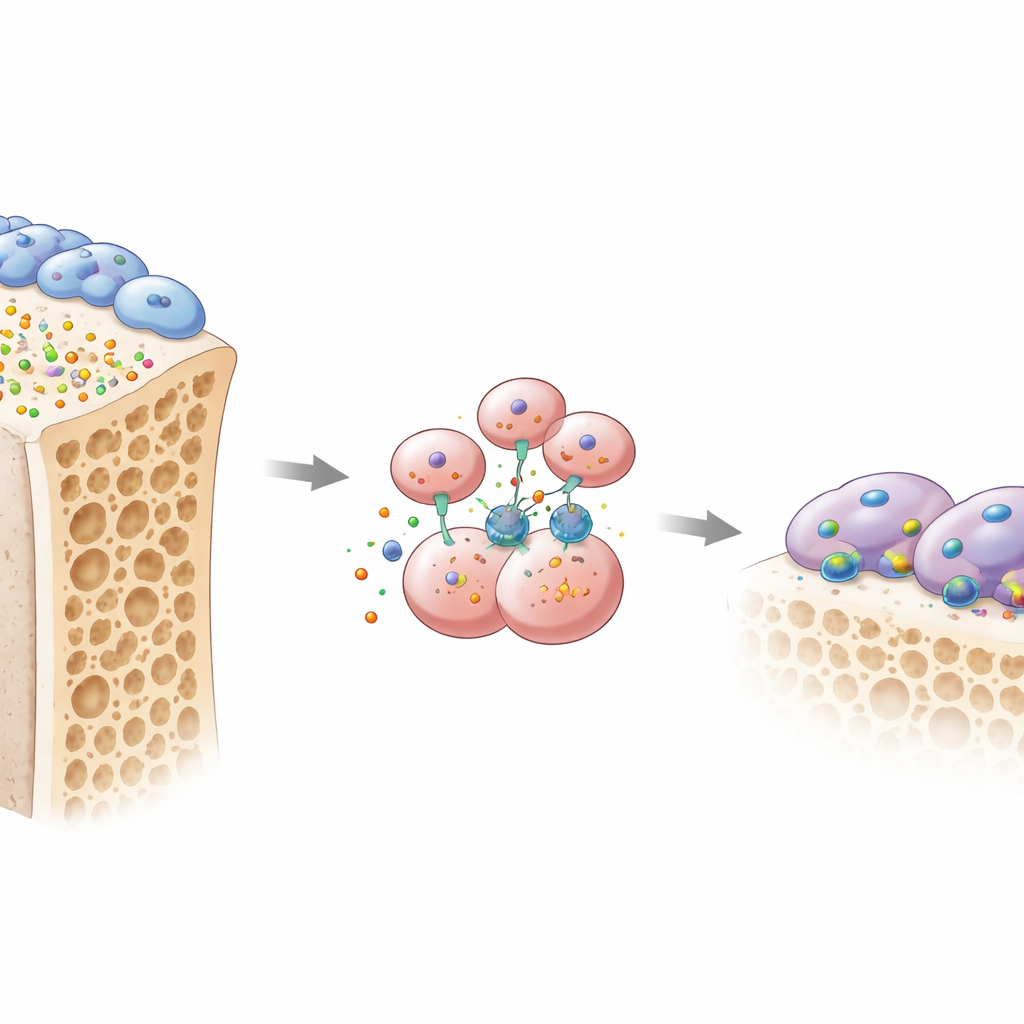
Was passiert, wenn die Bremse entfernt wird
Um Ursache und Wirkung zu prüfen, erzeugte das Team Mäuse ohne OMD. Wurde OMD im gesamten Körper oder spezifisch in Osteoblasten entfernt, verloren die Tiere deutlich mehr schwammartigen (trabekulären) Knochen und zeigten einen Anstieg aktiver Osteoklasten, die an Knochenoberflächen nagen. Im Gegensatz dazu hatte das Entfernen von OMD nur in Osteoklastvorläufern wenig Auswirkungen, was darauf hindeutet, dass OMD normalerweise als Botschaft von Osteoblasten an ihre knochenresorbierenden Nachbarn wirkt. In Zellkulturen differenzierten sich Osteoklastvorläufer, die mit Osteoblasten kultiviert wurden, die wenig OMD produzierten, zu großen, aggressiven Osteoklasten. Das Wiederzugeben von gereinigtem OMD-Protein kehrte den Effekt um: Es reduzierte deutlich die Bildung dieser mehrkernigen Knochenfresser und störte ihre spezialisierten „Versiegelungsring“-Strukturen, mit denen sie Knochen greifen und auflösen.
Die Energiezentralen der Zelle herunterfahren
Die Forscher fragten dann, wie dieses Osteoblasten-Signal Osteoklasten so wirkungsvoll bremsen kann. Ihre Analysen deuteten auf den Energiestoffwechsel hin. Osteoklasten sind energiehungrig und verlassen sich stark auf Mitochondrien, die „Kraftwerke“ der Zelle, zur ATP-Produktion. Wurden Osteoklastvorläufer OMD ausgesetzt, sanken Gene und Proteine, die an der mitochondrialen Atmung beteiligt sind, die Kopien mitochondrialer DNA verringerten sich, und direkte Messungen zeigten eine geringere Sauerstoffnutzung und ATP-Produktion durch Mitochondrien. Die Glykolyse, ein alternatives zuckerabbauendes System, stieg nur leicht an und konnte das Defizit nicht vollständig ausgleichen. Infolgedessen fiel das mitochondriale Membranpotential und das gesamte metabolische Profil der Zellen verschob sich in einen energiegestressten Zustand. Diese Veränderungen standen in engem Zusammenhang mit reduzierten Leveln einer Schlüsseluntereinheit des Enzyms namens RRM2, die hilft, die für die Erhaltung mitochondrialer DNA benötigten DNA-Bausteine bereitzustellen.
Eine Schritt‑für‑Schritt-Kette vom Oberflächen-Sensor zu Genen
Tiefer untersuchten die Autoren eine Signalkette, die ein äußeres Protein mit der inneren Energie-Kontrolle verbindet. OMD wurde an einen spezifischen Rezeptor, Integrin β8, auf Osteoklastvorläufern gebunden. Diese Interaktion dämpfte die Aktivität eines molekularen Schalters, RhoA, und erhöhte die Markierung (Phosphorylierung) des Regulators YAP, wodurch YAP den Zellkern verließ. Ohne YAP, das mit TEAD-Proteinen an der DNA zusammenarbeitet, wurde das Rrm2-Gen herunterreguliert. Weniger RRM2 bedeutete weniger DNA-Bausteine für Mitochondrien, weniger mitochondriale DNA, geringere Mengen an Komponenten der Elektronentransportkette und letztlich eine schwächere mitochondriale ATP-Produktion. Blockierten die Forscher RRM2 mit einem kleinen Molekül, verringerten sich Osteoklastbildung und mitochondriale Funktion ähnlich wie unter OMD. Umgekehrt rettete das erzwungene Überproduzieren von RRM2 die Energieproduktion und die Osteoklastentwicklung teilweise, selbst in Gegenwart von OMD. 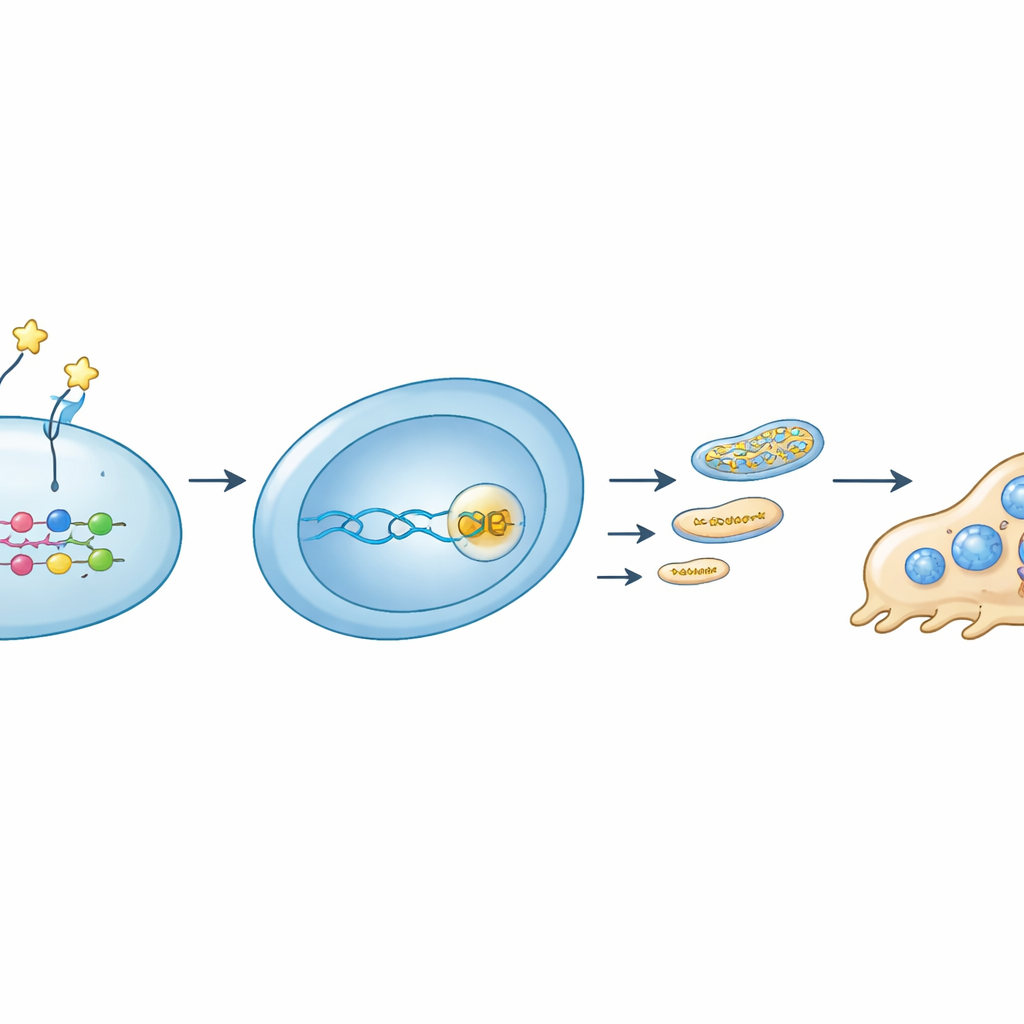
Mögliche neue Behandlungsansätze testen
Abschließend prüfte die Studie, ob das Verstärken dieser natürlichen Bremse Knochen in lebenden Tieren schützen kann. In Mäusen, denen die Eierstöcke entfernt wurden, um den postmenopausalen Knochenverlust zu simulieren, bewahrten regelmäßige Injektionen von rekombinantem OMD-Protein oder das RRM2-blockierende Medikament Osalmid beide die Knochenstruktur. Die behandelten Mäuse hatten dichtere trabekuläre Knochen, weniger Osteoklasten und geringere Mengen mitochondrialer Proteine in diesen Osteoklasten. Ähnliche Vorteile zeigten sich in einem Modell schnellen, entzündungsgetriebenen Knochenverlusts, ausgelöst durch bakterielle Toxine. Wichtig ist, dass eine kurzfristige Behandlung keine sichtbaren Schäden an wichtigen Organen verursachte, obwohl längere und detailliertere Sicherheitstests erforderlich sind.
Was das für die zukünftige Versorgung bedeutet
Zusammengefasst zeigen die Ergebnisse, dass Osteomodulin als entscheidender Friedenswächter im Knochen wirkt. Wenn es von Osteoblasten produziert wird, signalisiert es über Integrin β8, um Osteoklastvorläufer umzuprogrammieren und ihre mitochondriale Energiezufuhr zu drosseln, sodass sie nicht übermäßig wachsen oder übermäßig aktiv werden. Bei Osteoporose scheint diese Bremse zu schwächeln, wodurch knochenresorbierende Zellen energiereicher und zerstörerischer werden. Durch die Wiederherstellung von OMD oder das gezielte Eingreifen in das nachgelagerte Energieenzym RRM2 könnte es möglich sein, den Knochenabbau sanft zu verlangsamen, ohne ihn vollständig auszuschalten, und so eine neue, stoffwechselfokussierte Strategie zum Schutz des alternden Skeletts zu bieten.
Zitation: Jiang, X., Chen, H., Hou, W. et al. Osteoblast-derived osteomodulin restrains osteoclastogenesis via ITGB8/RRM2-mediated reduction of mitochondrial respiration and mitochondrial ATP production. Exp Mol Med 58, 879–897 (2026). https://doi.org/10.1038/s12276-026-01682-7
Schlüsselwörter: Osteoporose, Knochenumbau, Osteoklasten, mitochondriale Stoffwechsel, Osteomodulin