Clear Sky Science · ja
骨芽細胞由来のオステオモジュリンはITGB8/RRM2を介したミトコンドリア呼吸とミトコンドリアATP産生の低下を通じて破骨細胞形成を抑制する
骨にとってなぜ重要か
骨粗鬆症は、特に閉経後の女性を中心に何百万もの高齢者の骨を静かに脆弱化させます。現在の治療薬の多くは骨の分解を広く抑えるか骨形成を促進しますが、副作用を伴うことがしばしばです。本研究は、骨そのものに備わる自然の「制動装置」を明らかにします。骨を作る細胞が産生するタンパク質が、骨を壊す細胞に対してエネルギー使用を抑えるよう指示し、それによって破壊力を弱めるという仕組みです。この組み込みの安全機構を理解すれば、安全で標的化された新しい骨粗鬆症治療の発想につながる可能性があります。
骨細胞間の隠れたシグナル
骨の健康は、主に二つの細胞種間の綱引きに依存しています。骨芽細胞は新しい骨を作り、破骨細胞は古い骨を溶かして置換を可能にします。著者らは、骨芽細胞が骨基質に分泌する小さなタンパク質であるオステオモジュリン(OMD)という見落とされがちなシグナルに着目しました。複数の大規模な遺伝データセットを骨粗鬆症モデルから解析したところ、脆弱な骨ではOMD遺伝子の発現が一貫して低下していることが分かりました。閉経後女性の骨組織と血液を調べると、骨粗鬆症の患者は骨内と循環の双方でOMDが少なく、OMD低値は急速な骨喪失の指標と相関していました。類似の低下はエストロゲン欠乏のマウスモデルでも見られ、OMDの低下が骨の脆弱化に共通する特徴であることを示唆しています。 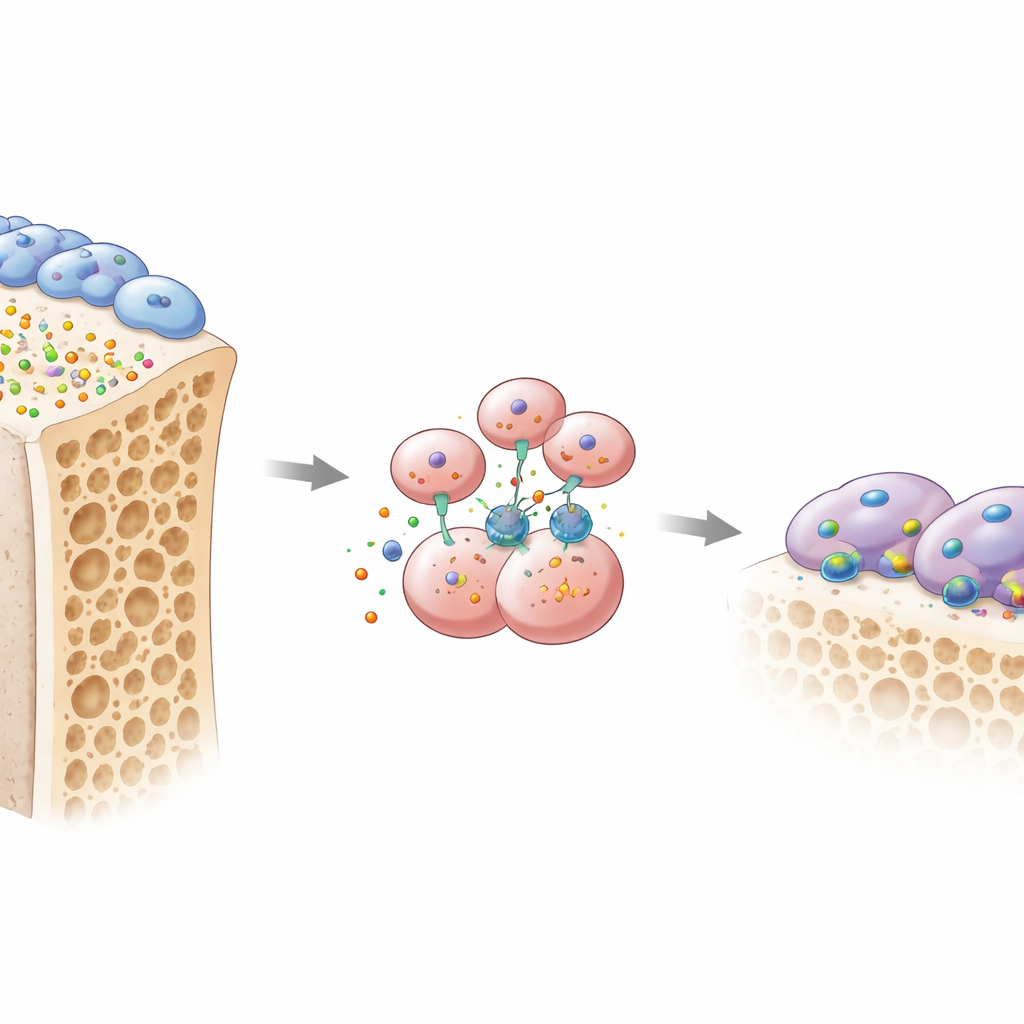
制動装置が外れるとどうなるか
因果関係を確かめるために、研究チームはOMD欠損マウスを作製しました。全身性にOMDを欠失させても、骨芽細胞特異的にOMDを除去しても、海綿骨の喪失が著しく進み、骨表面で活性化した破骨細胞が急増しました。対照的に、破骨細胞前駆細胞自体からのみOMDを除去してもほとんど影響はなく、OMDは通常、骨芽細胞から骨を吸収する近隣細胞へ送られるメッセージとして働いていることを示唆しました。培養皿で観察すると、OMD産生が少ない骨芽細胞と共培養された破骨細胞前駆細胞は大型で攻撃的な破骨細胞に分化しました。純化したOMDタンパク質を加えると状況は一変し、多核の骨吸収細胞の形成が著しく抑えられ、骨を把持して溶かすための特有の「シーリングリング」構造が破壊されました。
細胞内の発電所を抑える
研究者らは次に、この骨芽細胞由来シグナルがどのようにして破骨細胞を強力に抑制するのかを探りました。解析はエネルギー代謝に向かいました。破骨細胞はエネルギーを大量に消費し、ATPを生成するミトコンドリアに大きく依存しています。破骨細胞前駆細胞をOMDにさらすと、ミトコンドリア呼吸に関与する遺伝子やタンパク質が減少し、ミトコンドリアDNAのコピー数が減り、直接測定でもミトコンドリアによる酸素消費とATP産生が低下しました。補助的な糖分解(解糖系)はわずかに上昇しましたが、完全な補償には至りませんでした。その結果、ミトコンドリア膜電位が低下し、全体の代謝プロファイルはエネルギー不足の状態へとシフトしました。これらの変化は、ミトコンドリアDNAを維持するためのDNA構成要素を供給するのに関わる主要な酵素サブユニットであるRRM2の低下と密接に結びついていました。
表面センサーから遺伝子までの段階的連鎖
さらに掘り下げたところ、細胞外のタンパク質を内側のエネルギー制御につなぐシグナル連鎖が追跡されました。OMDは破骨細胞前駆細胞の特定の受容体、インテグリンβ8(ITGB8)に結合することが見いだされました。この相互作用は分子スイッチであるRhoAの活性を抑え、調節因子YAPのリン酸化(タグ付け)を増加させてYAPを核外に追いやりました。YAPがTEADタンパク質とともにDNA上で働けなくなると、Rrm2遺伝子の発現が沈静化します。RRM2減少はミトコンドリアのためのDNA構成要素を減らし、ミトコンドリアDNAの量を減少させ、電子伝達鎖構成要素の量を低下させ、最終的にミトコンドリアATP産生を弱めます。研究者らが小分子でRRM2を阻害すると、OMD処理と同様に破骨細胞形成とミトコンドリア機能が低下しました。逆に、細胞に余分なRRM2を強制発現させると、OMD存在下でもエネルギー産生と破骨細胞の発達が部分的に回復しました。 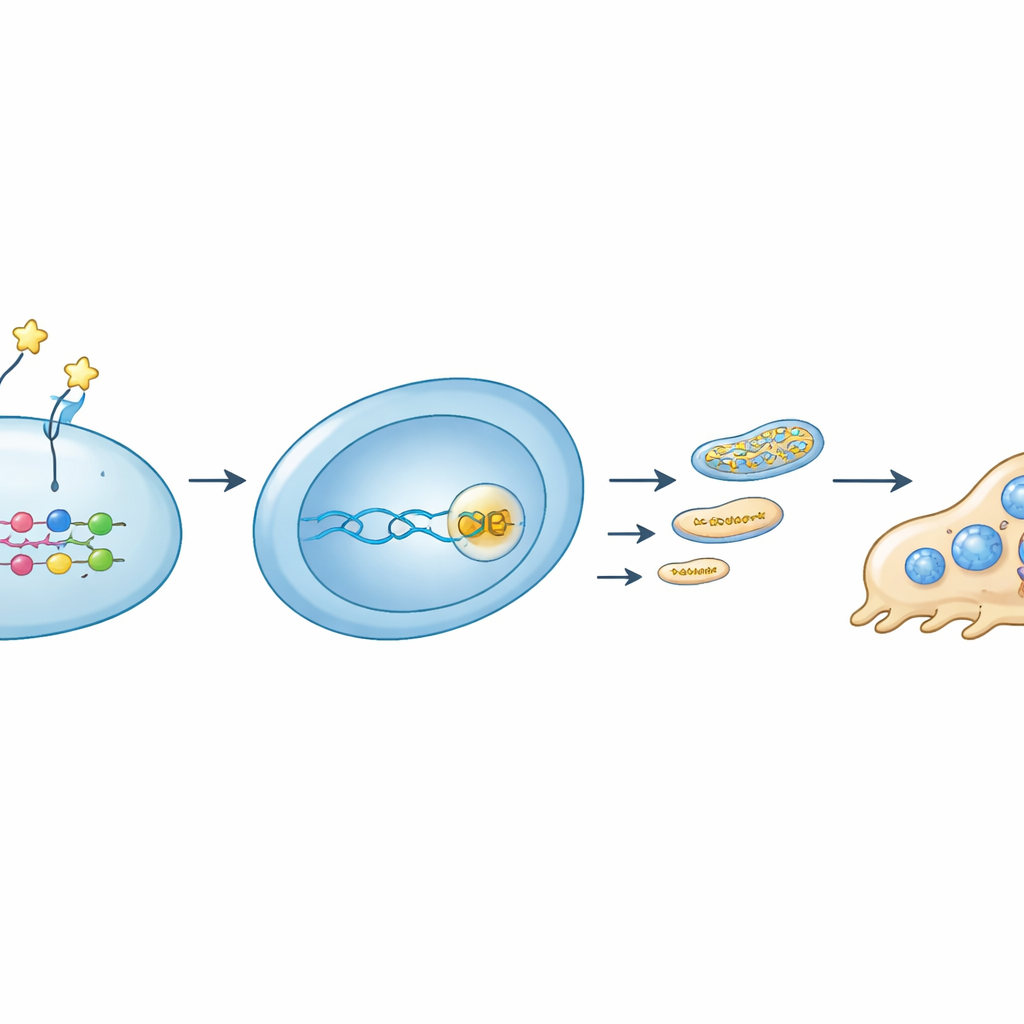
治療の新たな角度を試す
最後に、自然の制動装置を強化することで生体の骨を保護できるかを検証しました。閉経後の骨喪失を模すために卵巣を摘出したマウスに、組換えOMDタンパク質またはRRM2阻害薬オサルミドを定期的に注射すると、骨構造が維持されました。治療を受けたマウスは細柱状骨の骨密度が高く、破骨細胞が減少し、それら破骨細胞内のミトコンドリアタンパク質レベルも低下していました。細菌毒素で引き起こされる迅速な炎症性骨喪失モデルでも類似の有益効果が見られました。重要なのは、短期的な処置では主要臓器に明らかな損傷は認められなかったことですが、より長期で詳細な安全性評価が今後必要です。
今後の治療への意味
総括すると、本研究はオステオモジュリンが骨の重要な平和維持因子として働くことを明らかにしました。骨芽細胞がOMDを産生すると、インテグリンβ8を介して破骨細胞前駆細胞を再プログラムし、ミトコンドリアへのエネルギー供給を絞って過剰な増殖や過活動を防ぎます。骨粗鬆症ではこの制動装置が弱まり、骨を吸収する細胞がよりエネルギッシュで破壊的になります。OMDを回復させるか、下流のエネルギー酵素RRM2を標的にすることで、骨の分解を完全に止めることなく穏やかに遅らせる新たな代謝志向の戦略で高齢化する骨格を守る可能性があります。
引用: Jiang, X., Chen, H., Hou, W. et al. Osteoblast-derived osteomodulin restrains osteoclastogenesis via ITGB8/RRM2-mediated reduction of mitochondrial respiration and mitochondrial ATP production. Exp Mol Med 58, 879–897 (2026). https://doi.org/10.1038/s12276-026-01682-7
キーワード: 骨粗鬆症, 骨リモデリング, 破骨細胞, ミトコンドリア代謝, オステオモジュリン