Clear Sky Science · ru
Критическая роль фосфорилирования STAT3 на Thr714 в опухолеобразовании, вызванном NPM-ALK
Как небольшая переключающая метка в раковых клетках может изменить их судьбу
Рак часто присваивает себе нормальные системы контроля организма, превращая обычные клеточные сигналы в постоянные команды «расти и делиться». В этом исследовании рассматривается один такой контрольный переключатель внутри иммунных клеток, вовлечённых в тип заболевания крови, называемый анапластической крупноклеточной лимфомой (ALCL). Углубившись в изучение одной химической метки, прикреплённой к ключевому белку, исследователи показывают, как, казалось бы, небольшое изменение может решить, будут ли раковые клетки продолжать размножаться или останутся под контролем.
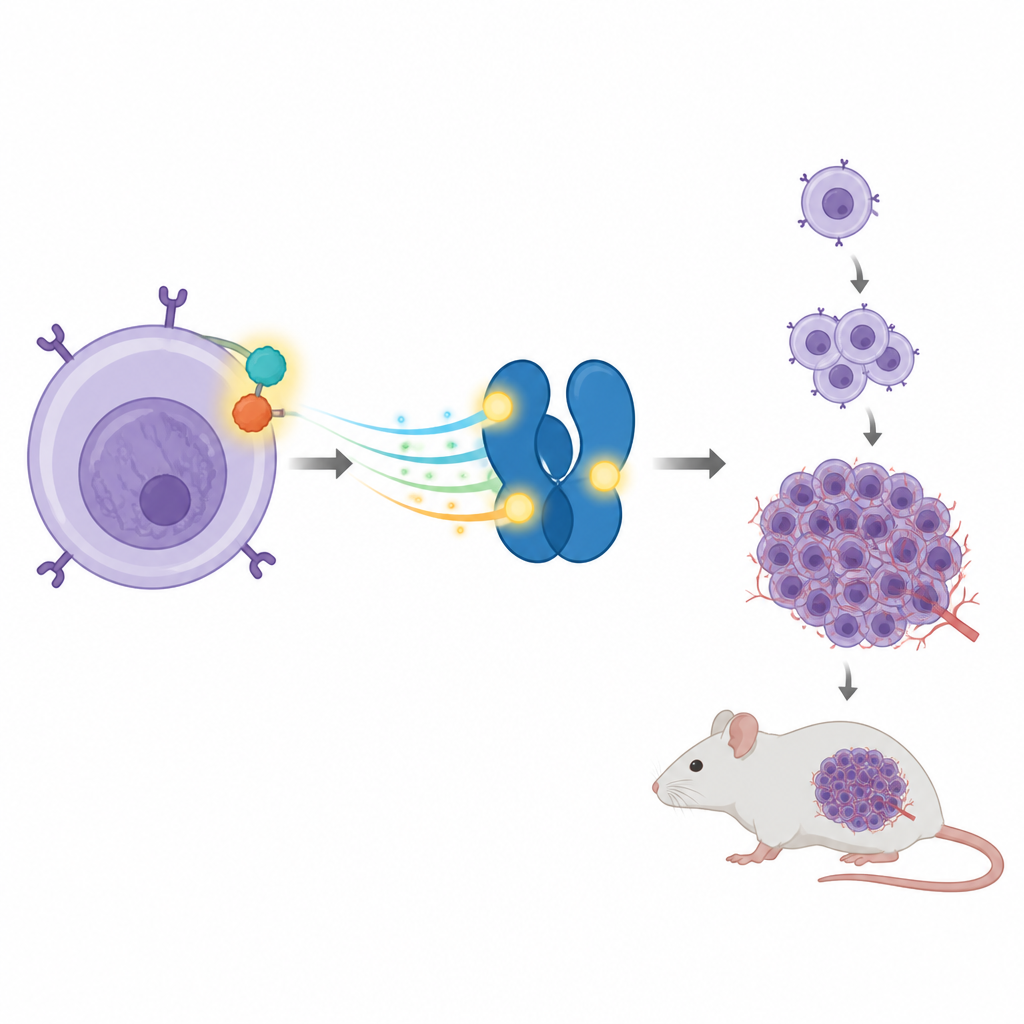
Партнёрство, приводящее к раку, внутри иммунных клеток
В некоторых опухолях ALCL имеется разорванный и вновь сшитый ген, который сливает два белка в один, называемый NPM‑ALK. Этот гибридный белок ведёт себя как зажатая педаль газа, постоянно посылая сигналы роста внутри клетки. Одной из его излюбленных мишеней является другой белок — STAT3, который в норме помогает клеткам отвечать на внешние сигналы, включая или выключая определённые гены. При ALCL NPM‑ALK поддерживает STAT3 в включённом состоянии, что в свою очередь повышает активность генов, толкающих клетки к делению и выживанию тогда, когда этого не должно происходить.
Новое контрольное место на знакомом белке
STAT3 активируется только тогда, когда на определённых мелких сайтах появляются фосфатные группы — процесс, называемый фосфорилированием. Два таких сайта уже были известны как важные, но роль третьего сайта, обозначенного как T714, оставалась неясной. Команда создала специальный антитело, которое распознаёт STAT3 только тогда, когда этот сайт помечен, и использовала его для изучения клеточных линий пациентов и мышиной модельной системы. Они обнаружили, что при активном NPM‑ALK STAT3 фосфорилировался на всех трёх сайтах, включая T714, и что блокирование NPM‑ALK существующими препаратами снимало эти метки. Это показало, что опухолеобразующий белок‑фьюжн прямо контролирует фосфорилирование на T714 наряду с уже известными сайтами.
Что происходит, когда переключатель на T714 удалён
Чтобы проверить, что именно делает T714, исследователи модифицировали мышиные кровяные клетки так, чтобы они экспрессировали NPM‑ALK, затем уменьшили уровень их природного STAT3 и заменили его либо нормальной версией, либо мутантом, в котором T714 изменён так, что не может быть помечен. Нормальный STAT3 правильно модифицировался на двух основных контрольных сайтах, перемещался в ядро клетки и активировал связанные с раком гены, такие как Cyclin D1 и гены семейства Pim. В отличие от этого, мутант T714 получал лишь одну из обычных меток, в основном оставался за пределами ядра и не активировал эти гены. В результате клетки с мутантным STAT3 росли медленнее, реже делились и не приобретали ту свободу роста, которую обычно даёт NPM‑ALK.
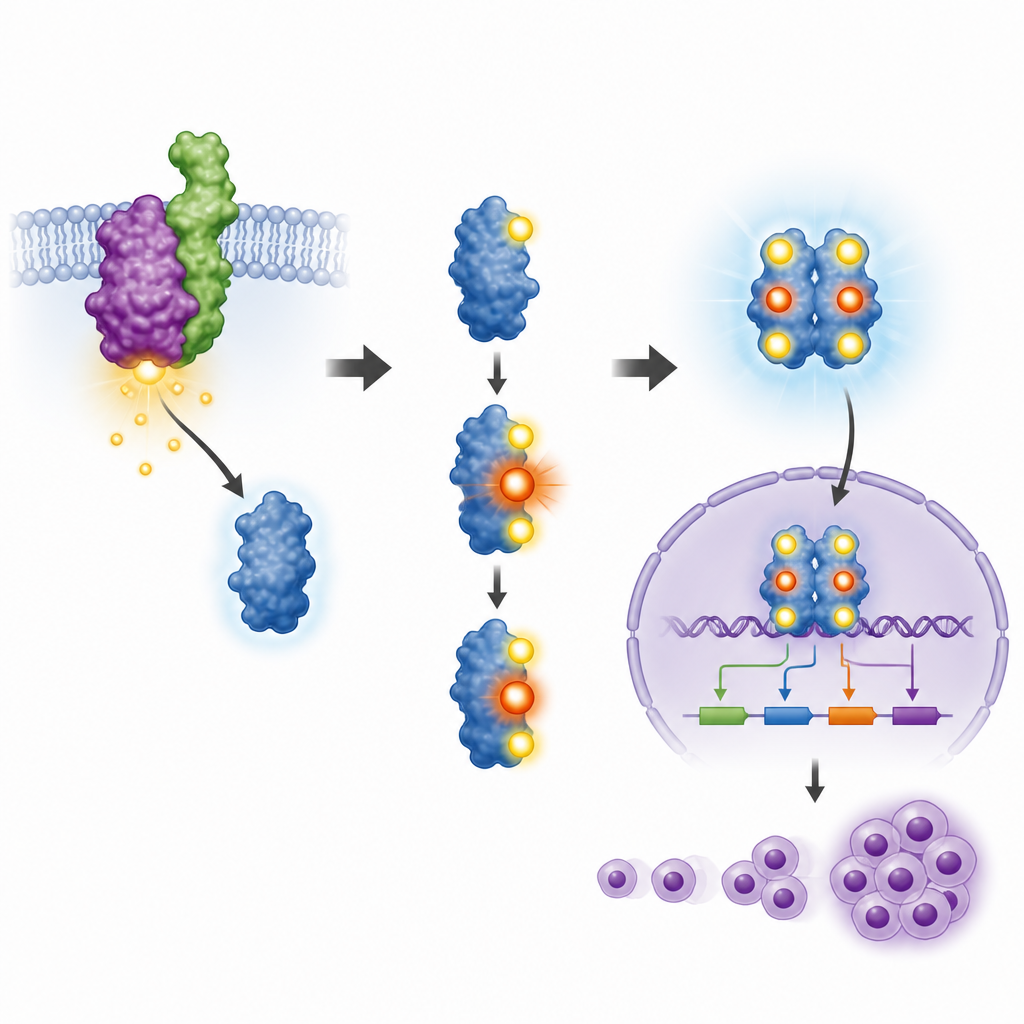
От клеточных культур до опухолей в живых мышах
Затем команда спросила, влияет ли этот единичный сайт на STAT3 также на рост опухолей в живых животных. Они ввели разные модифицированные клетки подкожно мышам. Клетки с NPM‑ALK и нормальным STAT3 формировали большие опухоли и вызывали увеличение печени и селезёнки у животных, что отражало агрессивное течение болезни. При снижении уровня STAT3 рост опухолей резко падал. Возвращение нормального STAT3 восстанавливало большую часть способности к образованию опухолей, тогда как добавление мутанта T714 — нет. У мышей, получивших клетки с мутантным белком, опухоли были значительно меньшими, а размеры органов — близки к нормальным. Эти результаты связали крошечную фосфатную метку на T714 с полной онкогенной силой в этой модели.
Что это значит для будущих методов лечения рака
В совокупности результаты указывают, что T714 действует как верхнеуровневый «включатель» для STAT3 в клетках, управляемых NPM‑ALK, помогая запустить последующие изменения, которые позволяют STAT3 войти в ядро и включить гены роста. Для неспециалистов это означает, что вместо того чтобы нацеливаться только на хорошо заметные «кнопки» в раковом пути, возможно также атаковать скрытый первичный переключатель, который подготавливает систему к активации. Препараты, созданные для блокирования пометки STAT3 на T714 или фермента, выполняющего этот шаг, могли бы предложить новый способ «приглушить» сверхактивный сигнал роста при ALCL и, возможно, при других раках, зависящих от подобных белков‑фьюжн.
Цитирование: Lin, X., Yao, Y., Moriwaki, Y. et al. A critical role for STAT3 Thr714 phosphorylation in NPM-ALK-driven tumorigenesis. Sci Rep 16, 15005 (2026). https://doi.org/10.1038/s41598-026-44867-w
Ключевые слова: STAT3, NPM-ALK, анапластическая крупноклеточная лимфома, фосфорилирование, опухолеобразование