Clear Sky Science · pt
Um papel crítico da fosforilação de STAT3 Thr714 na tumorigenese impulsionada por NPM-ALK
Como um pequeno interruptor nas células cancerosas pode mudar seu destino
O câncer frequentemente sequestra os sistemas normais de controle do corpo, transformando sinais celulares ordinários em comandos contínuos de crescer e dividir. Este estudo examina um desses interruptores de controle dentro de células imunes envolvidas em um tipo de câncer do sangue chamado linfoma anaplásico de grandes células (ALCL). Ao focalizar uma única marca química ligada a uma proteína-chave, os pesquisadores mostram como uma mudança aparentemente pequena pode decidir se as células cancerosas continuam a se multiplicar ou são contidas.
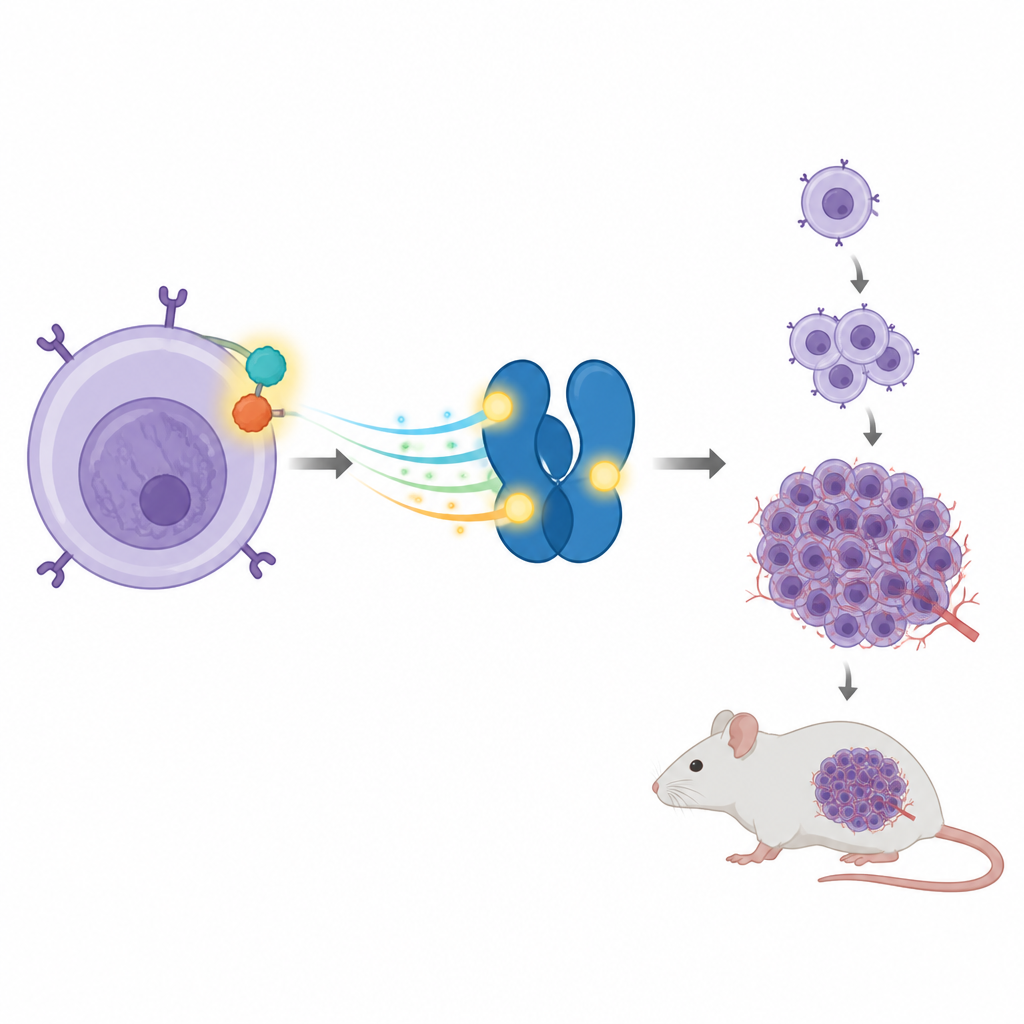
Uma parceria promotora de câncer dentro de células imunes
Alguns tumores de ALCL carregam um gene quebrado e religado que funde duas proteínas em uma só, chamada NPM-ALK. Essa proteína híbrida se comporta como um pedal do acelerador preso, enviando continuamente sinais de crescimento dentro da célula. Um de seus alvos preferidos é outra proteína chamada STAT3, que normalmente ajuda as células a responder a sinais externos ligando ou desligando genes específicos. No ALCL, NPM-ALK mantém STAT3 ligado, o que por sua vez aumenta a expressão de genes que impulsionam a divisão e a sobrevivência celular quando não deveriam.
Um novo ponto de controle em uma proteína conhecida
STAT3 funciona apenas quando certos locais minúsculos são marcados com grupos fosfato, um processo chamado fosforilação. Dois desses locais já eram conhecidos como importantes, mas o papel de um terceiro sítio, chamado T714, era pouco claro. A equipe criou um anticorpo personalizado capaz de reconhecer STAT3 somente quando esse sítio estava fosforilado, e o utilizou para estudar linhagens celulares de pacientes e um modelo celular de camundongo. Eles descobriram que, quando NPM-ALK estava ativo, STAT3 era fosforilado nos três sítios, incluindo T714, e que bloquear NPM-ALK com fármacos existentes removia essas marcas. Isso demonstrou que a proteína de fusão promotora de câncer controla diretamente T714 junto aos sítios mais conhecidos.
O que acontece quando o interruptor em T714 é removido
Para testar o que T714 realmente faz, os pesquisadores engenheiraram células sanguíneas de camundongo para expressar NPM-ALK, então reduziram seu STAT3 natural e o substituíram pela versão normal ou por um mutante no qual T714 foi alterado para que não pudesse ser fosforilado. O STAT3 normal foi adequadamente modificado em seus dois principais sítios de controle, migrou para o núcleo celular e ativou genes ligados ao câncer, como Cyclin D1 e genes da família Pim. Em contraste, o mutante T714 recebeu apenas uma das marcas habituais, permaneceu majoritariamente fora do núcleo e não conseguiu ativar esses genes. Como resultado, células com STAT3 mutante cresceram mais devagar, dividiram-se com menos frequência e não adquiriram a mesma independência dos sinais de crescimento que NPM-ALK normalmente confere.
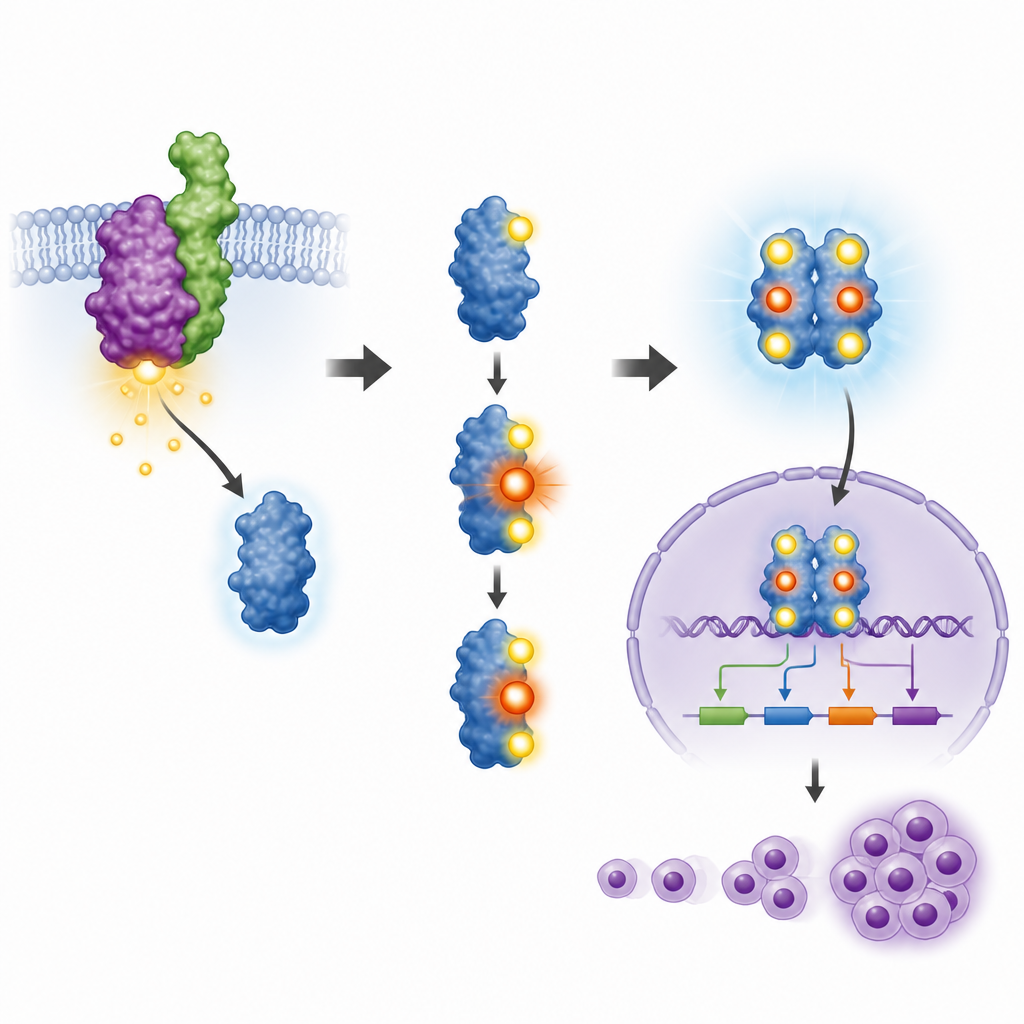
Da cultura celular a tumores em camundongos vivos
A equipe então investigou se esse único sítio em STAT3 também afeta o crescimento tumoral em animais vivos. Eles injetaram as diferentes células modificadas sob a pele de camundongos. As células com NPM-ALK e STAT3 normal formaram grandes tumores e causaram aumento do fígado e do baço dos animais, refletindo doença agressiva. Quando STAT3 foi silenciado, o crescimento tumoral caiu drasticamente. Reintroduzir STAT3 normal restaurou grande parte da capacidade de formar tumores, mas reintroduzir o mutante T714 não o fez. Camundongos que receberam células com a proteína mutante apresentaram tumores muito menores e tamanhos de órgãos próximos do normal. Esses resultados ligaram a pequena marca de fosfato em T714 ao pleno poder cancerígeno neste modelo.
O que isso significa para tratamentos futuros do câncer
Em conjunto, os achados sugerem que T714 atua como um interruptor inicial para STAT3 em células dirigidas por NPM-ALK, ajudando a permitir mudanças posteriores que deixam STAT3 entrar no núcleo e ligar genes de crescimento. Para não especialistas, isso significa que, em vez de mirar apenas os botões principais visíveis em uma via cancerígena, também pode ser possível atingir um interruptor oculto que prepara o sistema para a ativação. Fármacos projetados para bloquear a fosforilação de STAT3 em T714, ou a enzima que realiza essa etapa, poderiam oferecer uma nova forma de silenciar um sinal de crescimento hiperativo no ALCL e possivelmente em outros cânceres que dependem de proteínas de fusão semelhantes.
Citação: Lin, X., Yao, Y., Moriwaki, Y. et al. A critical role for STAT3 Thr714 phosphorylation in NPM-ALK-driven tumorigenesis. Sci Rep 16, 15005 (2026). https://doi.org/10.1038/s41598-026-44867-w
Palavras-chave: STAT3, NPM-ALK, linfoma anaplásico de grandes células, fosforilação, tumorigenese