Clear Sky Science · ja
NPM-ALK駆動の腫瘍形成におけるSTAT3 Thr714リン酸化の重要な役割
がん細胞の小さなスイッチが運命を変える仕組み
がんはしばしば体の正常な制御システムを乗っ取り、通常の細胞シグナルを持続的な増殖・分裂の指令に変えてしまいます。本研究は、未分化大細胞リンパ腫(ALCL)という血液がんに関わる免疫細胞内のひとつの制御スイッチに注目します。主要タンパク質に付く単一の化学的標識を精密に調べることで、見かけは小さな変化が、がん細胞が増え続けるか抑えられるかを決めうることを示しています。
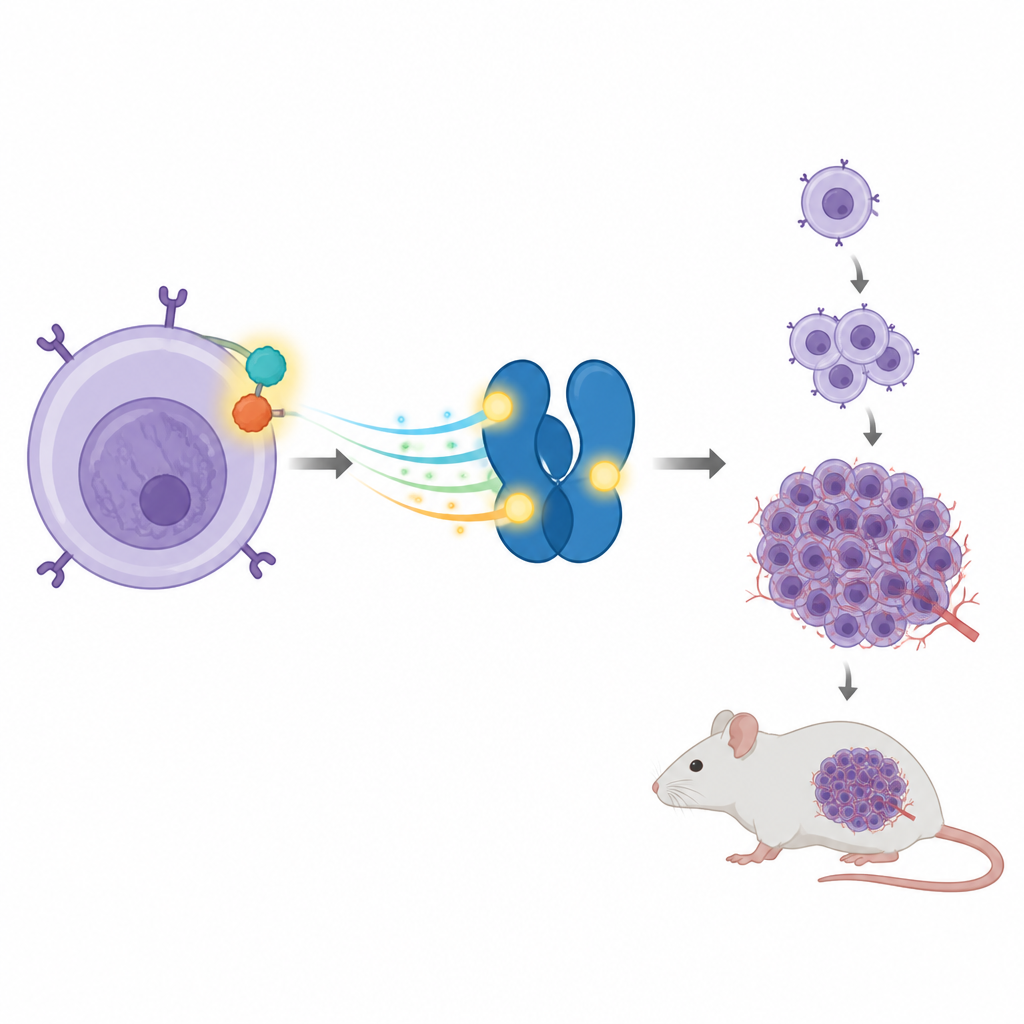
免疫細胞内でがんを駆動するパートナー関係
一部のALCL腫瘍では、2つの遺伝子が切れて再結合することでNPM‑ALKと呼ばれる融合タンパク質が生じます。このハイブリッドはアクセルが戻らないように振る舞い、細胞内に持続的な増殖シグナルを送り続けます。標的の一つがSTAT3というタンパク質で、通常は外部からの刺激に応じて特定の遺伝子をオン・オフする役割を担います。ALCLではNPM‑ALKがSTAT3を持続的に活性化し、それによって細胞の不適切な増殖や生存を促す遺伝子が高発現します。
よく知られたタンパク質上の新たな制御点
STAT3は特定の部位がリン酸化されることでのみ機能します。これまでに重要とされていた部位は二つありますが、三つ目の部位T714の役割は不明でした。研究チームはこの部位がリン酸化されたSTAT3だけを認識する特注抗体を作製し、患者由来のがん細胞株やマウス細胞モデルで調べました。その結果、NPM‑ALKが活性化しているときにはSTAT3の三つの部位すべて、T714を含めてリン酸化されており、既存の薬でNPM‑ALKを阻害するとこれらの標識が消えることが判明しました。これは、がんを駆動する融合タンパク質が既知の主要部位に加えT714も直接制御していることを示します。
T714のスイッチが外れると何が起きるか
T714の実際の役割を確かめるため、研究者らはNPM‑ALKを発現させるマウス血液細胞を作り、内在性のSTAT3を減少させたうえで、正常型またはT714が変異してリン酸化されない型のいずれかを補完しました。正常なSTAT3は主な二つの制御部位で適切に修飾され、核へ移行してCyclin D1やPimファミリーなどのがん関連遺伝子を活性化しました。一方、T714変異体は通常の標識のうち一つしか受けず、主に細胞質にとどまり、これらの遺伝子を活性化できませんでした。その結果、変異STAT3をもつ細胞は増殖が遅く、分裂頻度が低くなり、NPM‑ALKが通常与える増殖信号からの解放を得られませんでした。
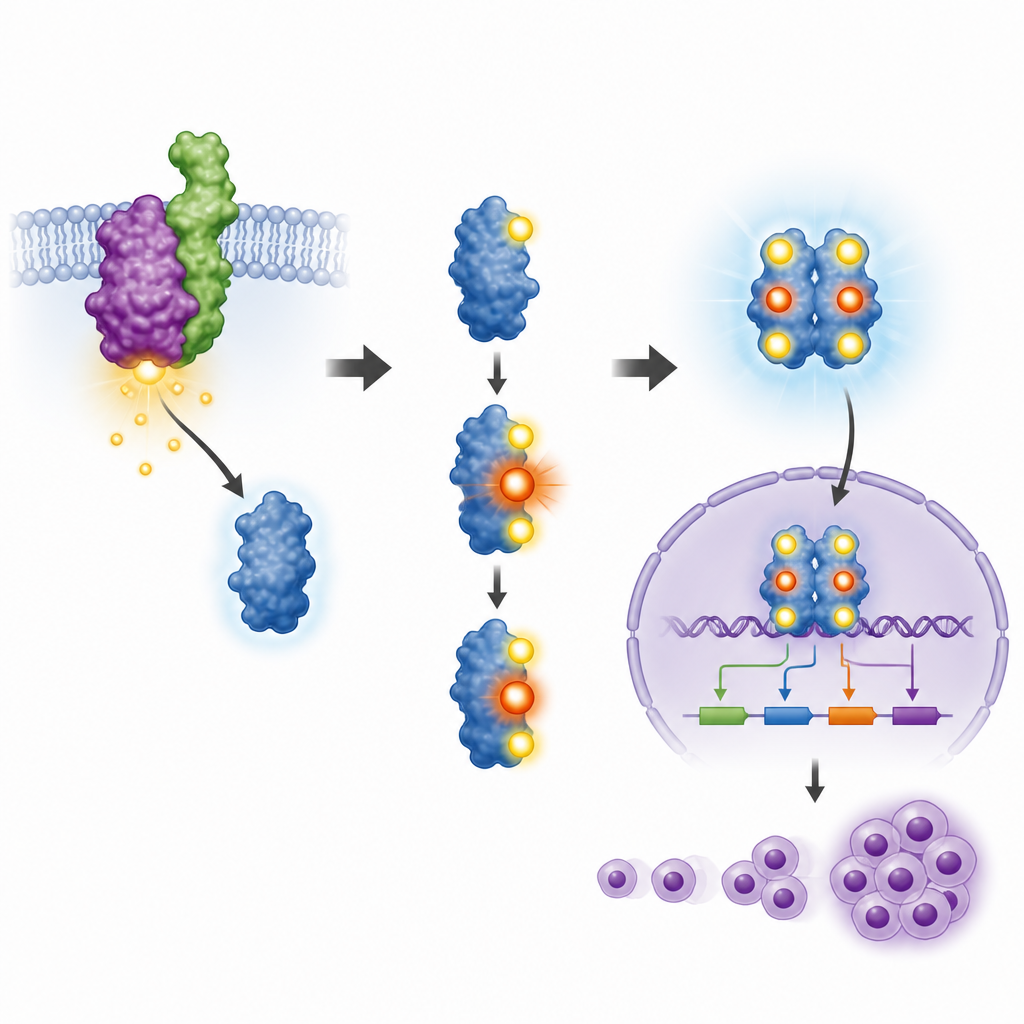
培養系から生体内の腫瘍へ
次にチームは、この単一部位の変化が生体内での腫瘍成長にも影響するかを調べました。異なる改変細胞をマウスの皮下に注入したところ、NPM‑ALKと正常なSTAT3を持つ細胞は大きな腫瘍を形成し、肝臓や脾臓の腫大を引き起こして攻撃的な病態を示しました。STAT3をノックダウンすると腫瘍成長は著しく低下しました。正常なSTAT3を戻すと腫瘍形成能は大部分回復しましたが、T714変異体を戻しても回復しませんでした。変異体を持つ細胞を移植されたマウスでは腫瘍ははるかに小さく、臓器サイズはほぼ正常でした。これらの結果は、T714に付く小さなリン酸化がこのモデルにおける完全な発がん能に結びつくことを示しています。
将来のがん治療への示唆
総じて、これらの発見はT714がNPM‑ALK依存細胞におけるSTAT3の上流のオン・スイッチとして働き、STAT3の核移行と増殖遺伝子の活性化を可能にする後続の変化を促すことを示唆します。専門外の方に言えば、がん経路の目に見える主要なボタンだけを標的にするのではなく、システムを活性化するための隠れたプライマー的スイッチを狙うことが可能かもしれない、ということです。STAT3のT714への標識やその酵素を阻害する薬剤は、ALCLや類似の融合タンパク質に依存する他のがんで過剰な増殖シグナルを抑える新たな手段を提供する可能性があります。
引用: Lin, X., Yao, Y., Moriwaki, Y. et al. A critical role for STAT3 Thr714 phosphorylation in NPM-ALK-driven tumorigenesis. Sci Rep 16, 15005 (2026). https://doi.org/10.1038/s41598-026-44867-w
キーワード: STAT3, NPM-ALK, 未分化大細胞リンパ腫, リン酸化, 腫瘍形成