Clear Sky Science · es
Un papel crítico de la fosforilación de STAT3 Thr714 en la tumorogénesis impulsada por NPM-ALK
Cómo un pequeño interruptor en las células cancerosas puede cambiar su destino
El cáncer a menudo secuestra los sistemas de control normales del organismo, convirtiendo señales celulares ordinarias en órdenes constantes de crecer y dividirse. Este estudio examina uno de esos interruptores de control dentro de células inmunitarias implicadas en un tipo de cáncer sanguíneo llamado linfoma anaplásico de células grandes (LACG). Al acercarse a una única etiqueta química unida a una proteína clave, los investigadores muestran cómo un cambio aparentemente menor puede decidir si las células cancerosas continúan multiplicándose o quedan controladas.
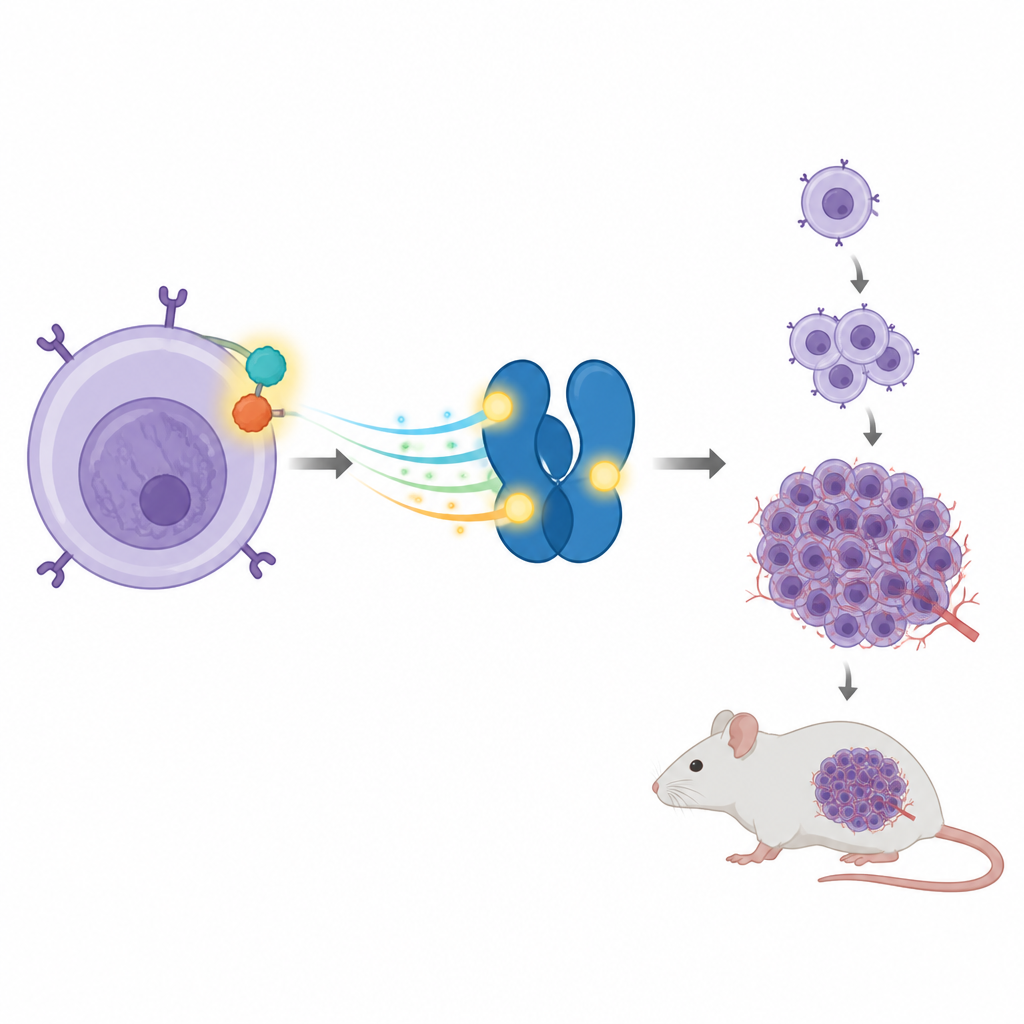
Una asociación que impulsa el cáncer dentro de las células inmunitarias
Algunos tumores de LACG contienen un gen roto y reensamblado que fusiona dos proteínas en una, denominada NPM‑ALK. Esta proteína híbrida actúa como un pedal del acelerador atascado, enviando constantemente señales de crecimiento dentro de la célula. Uno de sus blancos preferidos es otra proteína llamada STAT3, que normalmente ayuda a las células a responder a señales externas activando o desactivando genes concretos. En LACG, NPM‑ALK mantiene a STAT3 activado, lo que a su vez potencia genes que empujan a las células a dividirse y sobrevivir cuando no deberían hacerlo.
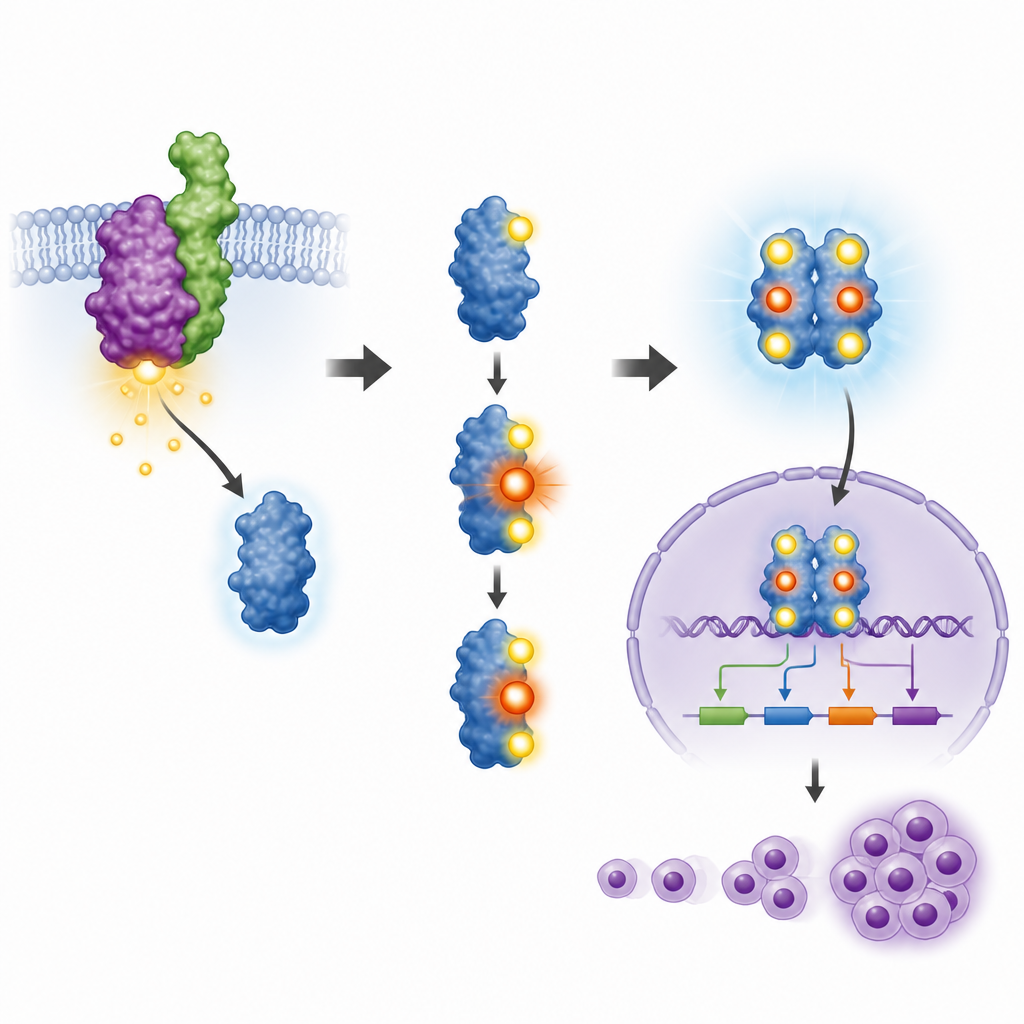
Un nuevo punto de control en una proteína conocida
STAT3 funciona solo cuando ciertos sitios diminutos en su secuencia están marcados con grupos fosfato, un proceso denominado fosforilación. Dos de estos sitios ya se conocían como importantes, pero el papel de un tercer sitio, llamado T714, no quedaba claro. El equipo creó un anticuerpo específico capaz de reconocer STAT3 únicamente cuando este sitio estaba fosforilado, y lo usó para estudiar líneas celulares cancerosas de pacientes y un modelo celular murino. Encontraron que cuando NPM‑ALK estaba activo, STAT3 estaba fosforilado en los tres sitios, incluido T714, y que bloquear NPM‑ALK con fármacos disponibles eliminaba estas marcas. Esto mostró que la proteína de fusión que impulsa el cáncer controla directamente T714 junto con los sitios más conocidos.
Qué ocurre cuando se elimina el interruptor en T714
Para probar la función real de T714, los investigadores diseñaron células sanguíneas de ratón para que expresaran NPM‑ALK, luego redujeron su STAT3 natural y lo reemplazaron por la versión normal o por un mutante en el que T714 se había cambiado para que no pudiera fosforilarse. STAT3 normal quedó correctamente modificado en sus dos sitios principales de control, se trasladó al núcleo celular y activó genes asociados al cáncer como Cyclin D1 y miembros de la familia Pim. En cambio, el mutante T714 recibió solo una de las marcas habituales, permaneció mayoritariamente fuera del núcleo y no logró activar estos genes. Como resultado, las células con STAT3 mutante crecieron más despacio, se dividieron con menos frecuencia y no adquirieron la misma independencia de las señales de crecimiento que NPM‑ALK suele conferir.
De cultivo celular a tumores en ratones vivos
El equipo preguntó entonces si este único sitio en STAT3 también influye en el crecimiento tumoral en animales vivos. Inyectaron las distintas células modificadas bajo la piel de ratones. Las células con NPM‑ALK y STAT3 normal formaron grandes tumores y provocaron agrandamiento del hígado y del bazo de los animales, reflejando una enfermedad agresiva. Cuando se redujo STAT3, el crecimiento tumoral cayó drásticamente. Volver a añadir STAT3 normal restauró gran parte de la capacidad de formar tumores, pero añadir el mutante T714 no lo hizo. Los ratones que recibieron células con la proteína mutante tuvieron tumores mucho más pequeños y tamaños de órganos cercanos a la normalidad. Estos resultados vinculan la pequeña etiqueta fosfato en T714 con el pleno poder cancerígeno en este modelo.
Qué implica esto para futuros tratamientos contra el cáncer
En conjunto, los hallazgos sugieren que T714 actúa como un interruptor inicial para STAT3 en las células impulsadas por NPM‑ALK, ayudando a habilitar cambios posteriores que permiten a STAT3 entrar en el núcleo y activar genes de crecimiento. Para el público no especializado, esto significa que, en lugar de apuntar solo a los botones más visibles de una vía oncogénica, también podría ser posible dirigirse a un interruptor precursor oculto que prepara el sistema para la activación. Fármacos diseñados para bloquear la fosforilación de STAT3 en T714, o la enzima que realiza este paso, podrían ofrecer una nueva manera de silenciar una señal de crecimiento sobreactivada en LACG y posiblemente en otros cánceres que dependen de proteínas de fusión similares.
Cita: Lin, X., Yao, Y., Moriwaki, Y. et al. A critical role for STAT3 Thr714 phosphorylation in NPM-ALK-driven tumorigenesis. Sci Rep 16, 15005 (2026). https://doi.org/10.1038/s41598-026-44867-w
Palabras clave: STAT3, NPM-ALK, linfoma anaplásico de células grandes, fosforilación, tumorogénesis