Clear Sky Science · nl
Een cruciale rol voor STAT3 Thr714-fosforylering in NPM-ALK-gedreven tumorvorming
Hoe een klein schakelaartje in kankercellen hun lot kan veranderen
Kanker kaapt vaak de normale controlesystemen van het lichaam en verandert gewone celsignalen in een constant bevel om te groeien en te delen. Deze studie onderzoekt één zo’n controleschakelaar binnen immuuncellen die betrokken zijn bij een type bloedkanker genaamd anaplastisch grootcellig lymfoom (ALCL). Door in te zoomen op een enkele chemische markering die aan een sleuteleiwit wordt bevestigd, laten de onderzoekers zien hoe een ogenschijnlijk kleine wijziging kan bepalen of kankercellen blijven vermenigvuldigen of juist onder controle worden gehouden.
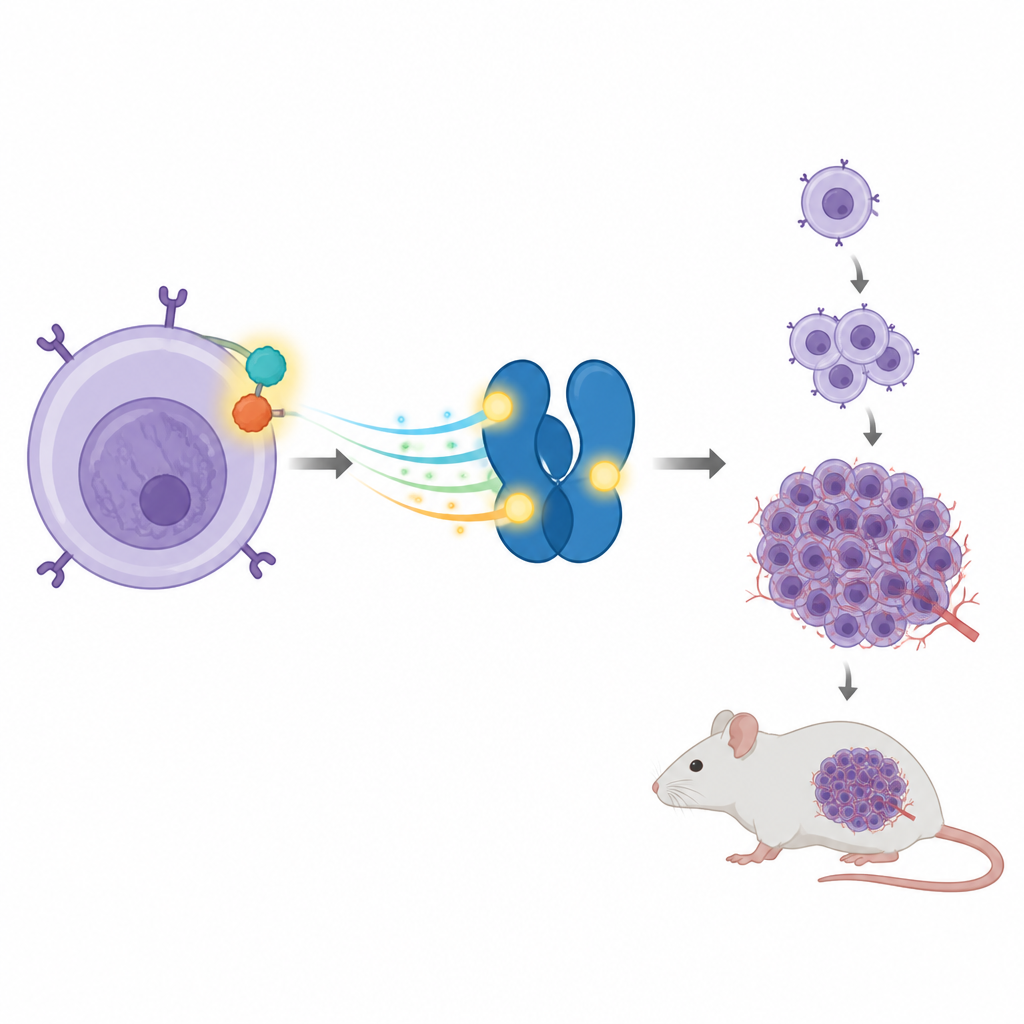
Een kankerveroorzakende samenwerking binnen immuuncellen
Sommige ALCL-tumoren dragen een gebroken en opnieuw verbonden gen dat twee eiwitten tot één fuseert, genoemd NPM-ALK. Dit hybride eiwit gedraagt zich als een vastzittend gaspedaal en stuurt voortdurend groeisignalen binnen de cel. Een van zijn favoriete doelwitten is een ander eiwit genaamd STAT3, dat normaal gesproken cellen helpt reageren op externe signalen door specifieke genen aan of uit te zetten. In ALCL houdt NPM-ALK STAT3 continu aan, wat op zijn beurt genen versterkt die cellen aanzetten tot delen en overleven wanneer dat eigenlijk niet zou moeten.
Een nieuwe bedieningsplek op een bekend eiwit
STAT3 werkt alleen wanneer bepaalde kleine locaties erop zijn voorzien van fosfaatgroepen, een proces dat fosforylering wordt genoemd. Twee van deze plaatsen waren al bekend als belangrijk, maar de rol van een derde plaats, T714 genoemd, was onduidelijk. Het team ontwikkelde een specifieke antilichaam dat STAT3 alleen herkent wanneer deze plaats gemarkeerd is, en gebruikte het om kankercellijnen van patiënten en een muismodel te bestuderen. Ze vonden dat wanneer NPM-ALK actief was, STAT3 op alle drie de plekken werd gemarkeerd, inclusief T714, en dat het blokkeren van NPM-ALK met bestaande geneesmiddelen deze markeringen verwijderde. Dit toonde aan dat het kankerveroorzakende fusie-eiwit T714 direct reguleert naast de beter bekende sites.
Wat er gebeurt wanneer de schakel op T714 wordt verwijderd
Om te testen wat T714 werkelijk doet, voorzagen de onderzoekers muis-bloedcellen van NPM-ALK, reduceerden vervolgens hun natuurlijke STAT3 en vervingen dit door óf de normale versie óf een mutant waarin T714 zo was veranderd dat het niet gemarkeerd kon worden. De normale STAT3 werd correct aangepast op de twee belangrijkste controlesites, verplaatste zich naar de celkern en schakelde kankergeassocieerde genen in zoals Cyclin D1 en leden van de Pim-familie. De T714-mutant daarentegen kreeg slechts één van de gebruikelijke markeringen, bleef grotendeels buiten de kern en activeerde deze genen niet. Als gevolg daarvan groeiden cellen met de mutant-STAT3 langzamer, deelden minder vaak en kregen ze niet dezelfde onafhankelijkheid van groeisignalen die NPM-ALK normaal geeft.
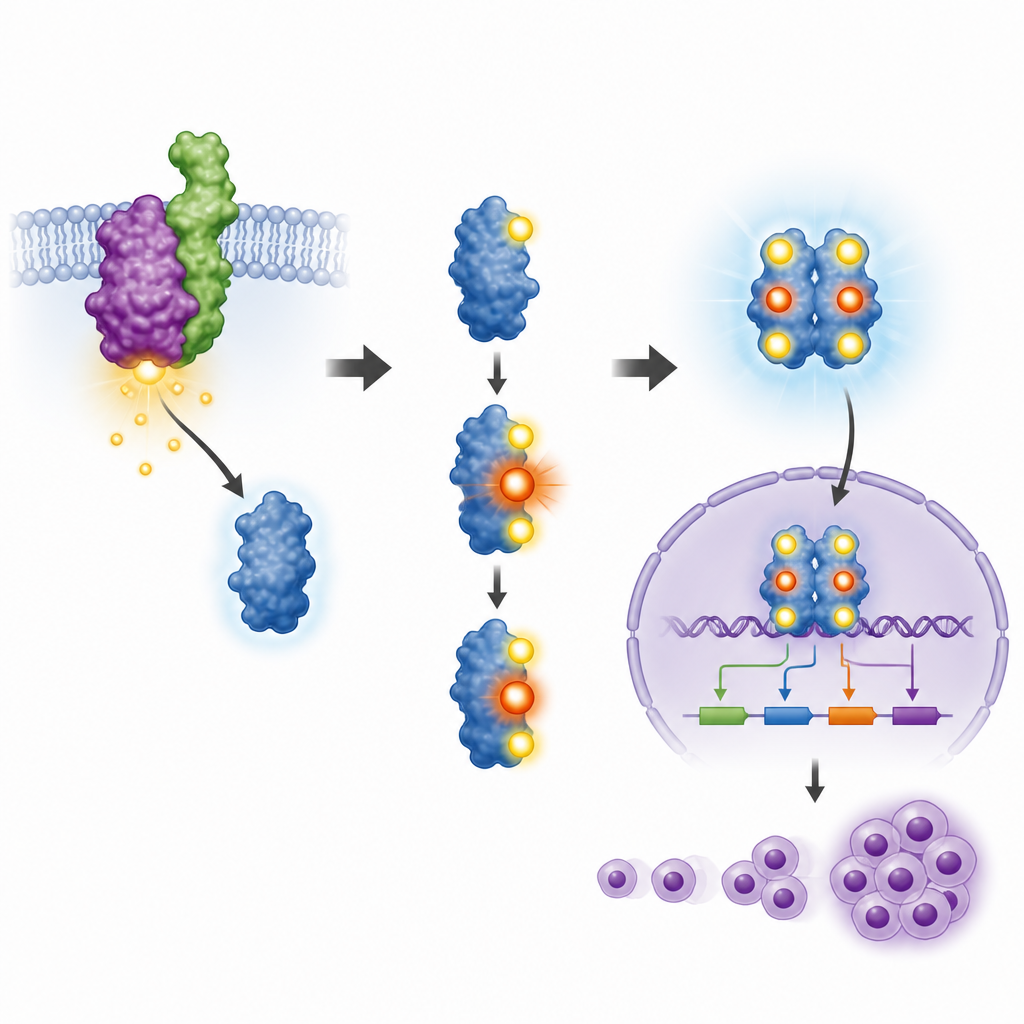
Van celkweek naar tumoren in levende muizen
Het team onderzocht daarna of deze enkele plek op STAT3 ook de tumorgroei in levende dieren beïnvloedt. Ze injecteerden de verschillende gemodificeerde cellen onder de huid van muizen. Cellen met NPM-ALK en normale STAT3 vormden grote tumoren en leidden tot vergroting van lever en milt bij de dieren, wat wijst op agressieve ziekte. Wanneer STAT3 werd onderdrukt, daalde de tumorgroei sterk. Het terugplaatsen van normale STAT3 herstelde grotendeels het tumorvermogen, maar het terugplaatsen van de T714-mutant deed dat niet. Muizen die cellen met het mutant-eiwit kregen hadden veel kleinere tumoren en nagenoeg normale orgaangroottes. Deze resultaten koppelen de kleine fosfaatmarkering op T714 aan de volledige kankerveroorzakende kracht in dit model.
Wat dit betekent voor toekomstige kankerbehandelingen
Gezamenlijk suggereren de bevindingen dat T714 fungeert als een upstream-aan-schakelaar voor STAT3 in cellen die door NPM-ALK worden gedreven, en helpt bij het mogelijk maken van latere veranderingen die STAT3 toelaten de kern binnen te gaan en groeigenen aan te zetten. Voor niet-specialisten betekent dit dat het, in plaats van alleen de zichtbare hoofdknoppen in een kankerpaa d te richten, mogelijk ook aantrekkelijk is om te mikken op een verborgen voor-schakelaar die het systeem voorbereidt op activatie. Geneesmiddelen die de markering van STAT3 op T714 blokkeren, of het enzym dat deze stap uitvoert, zouden een nieuwe manier kunnen bieden om een overactief groeisignaal in ALCL en mogelijk andere kankers die op soortgelijke fusie-eiwitten vertrouwen, te dempen.
Bronvermelding: Lin, X., Yao, Y., Moriwaki, Y. et al. A critical role for STAT3 Thr714 phosphorylation in NPM-ALK-driven tumorigenesis. Sci Rep 16, 15005 (2026). https://doi.org/10.1038/s41598-026-44867-w
Trefwoorden: STAT3, NPM-ALK, anaplastisch grootcellig lymfoom, fosforylering, tumorvorming