Clear Sky Science · pl
Kluczowa rola fosforylacji STAT3 Thr714 w nowotworzeniu napędzanym przez NPM-ALK
Jak drobny przełącznik w komórkach nowotworowych może zmienić ich los
Rak często zawłaszcza normalne systemy kontroli organizmu, zamieniając zwykłe sygnały komórkowe w stałe polecenia „rosnij i dziel się”. To badanie dotyczy jednego takiego przełącznika w komórkach odpornościowych uczestniczących w rodzaju nowotworu krwi zwanego anaplastycznym chłoniakiem z dużych komórek (ALCL). Poprzez przyjrzenie się pojedynczemu chemicznemu znacznikowi przyczepionemu do kluczowego białka, badacze pokazują, jak pozornie niewielka zmiana może zadecydować, czy komórki nowotworowe będą się nadal mnożyć, czy zostaną powstrzymane.
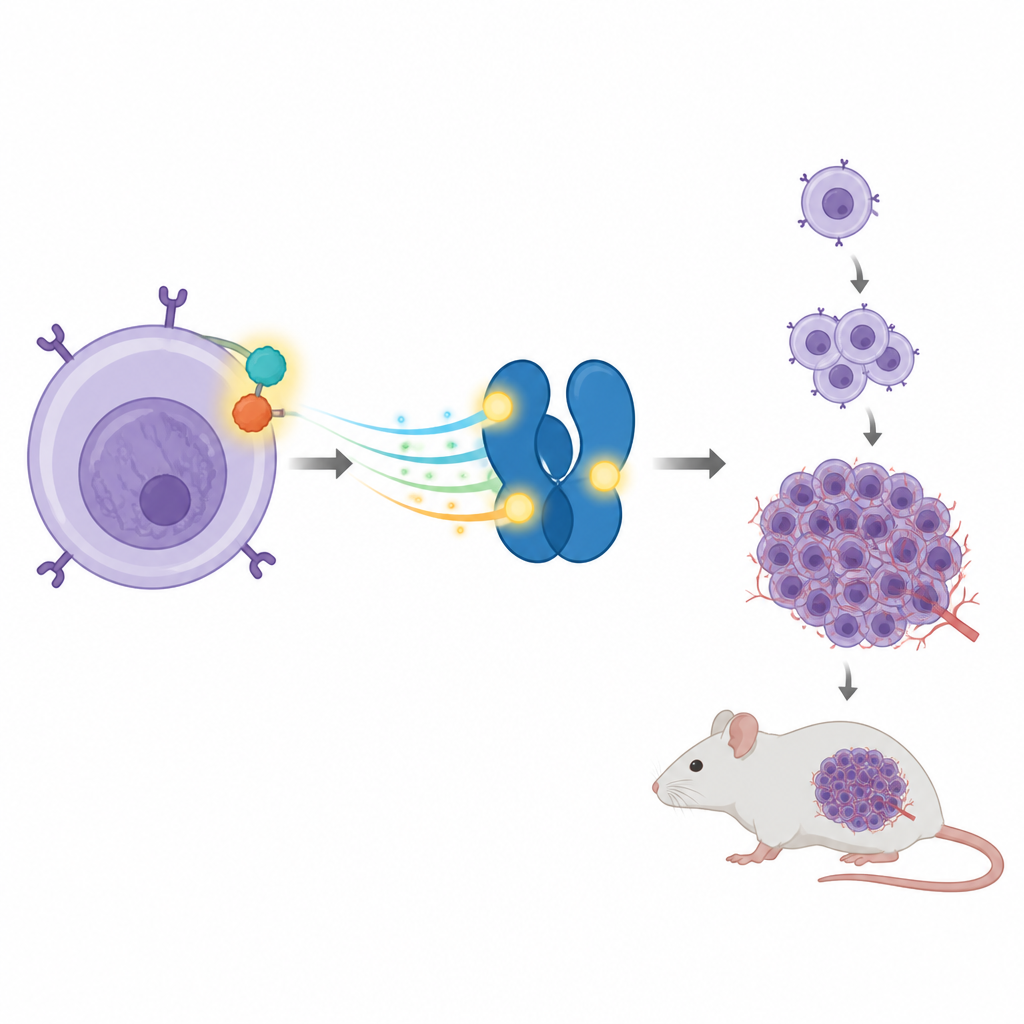
Partnerska relacja napędzająca raka w komórkach odpornościowych
Niektóre guzy ALCL niosą przerwany i ponownie złączony gen tworzący białko fuzyjne zwane NPM‑ALK. Ten hybrydowy białkowy tworzy coś w rodzaju przyciśniętego pedału przyspieszenia, stale wysyłając sygnały wzrostu wewnątrz komórki. Jednym z jego ulubionych celów jest inne białko o nazwie STAT3, które normalnie pomaga komórkom reagować na sygnały z zewnątrz poprzez włączanie lub wyłączanie określonych genów. W ALCL NPM‑ALK utrzymuje STAT3 w stanie aktywnym, co z kolei wzmacnia geny popychające komórki do podziału i przeżycia, kiedy nie powinny tego robić.
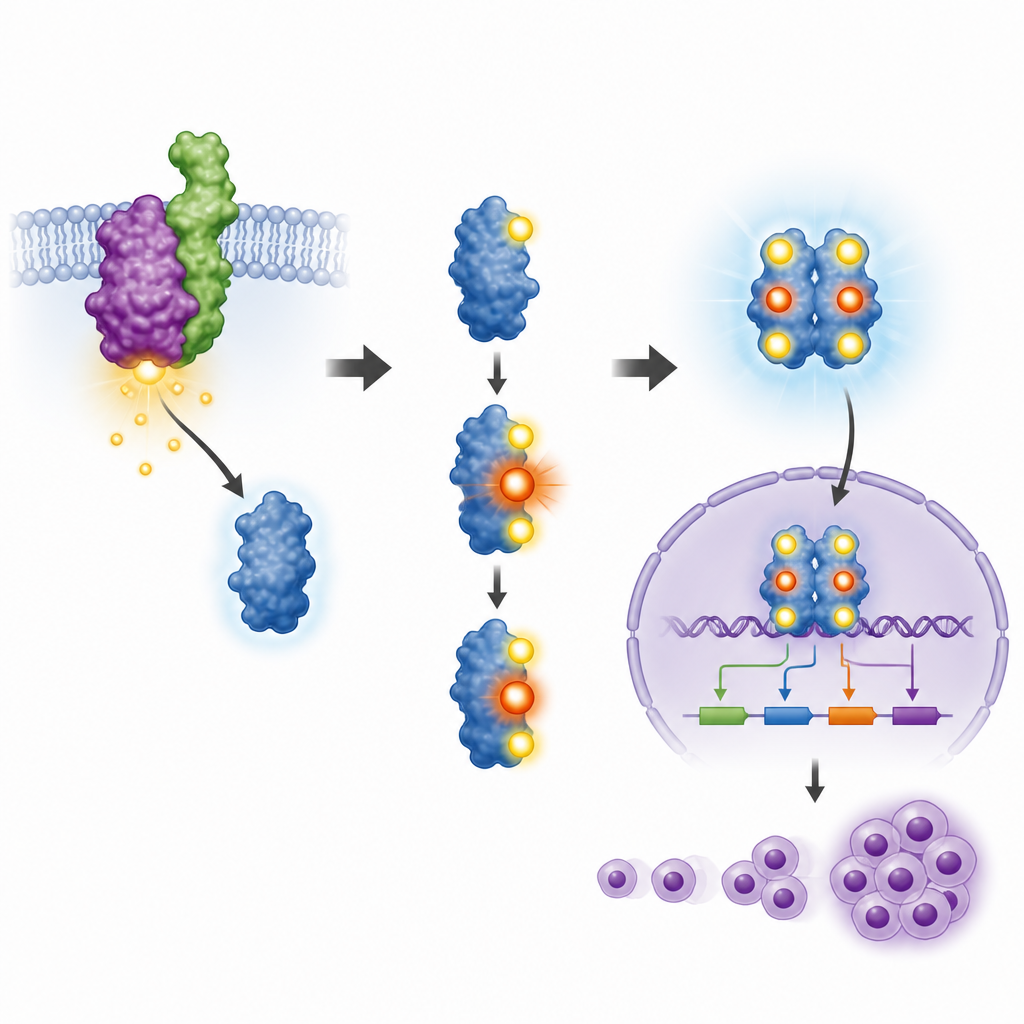
Nowe miejsce kontroli w znanym białku
STAT3 działa tylko wtedy, gdy pewne drobne miejsca na nim zostaną oznakowane grupami fosforanowymi, procesu zwanego fosforylacją. Dwa z tych miejsc były już znane jako ważne, ale rola trzeciego miejsca, nazwanego T714, była niejasna. Zespół stworzył swoistą przeciwciało zdolne rozpoznać STAT3 tylko wtedy, gdy to miejsce było oznakowane, i użył go do badania linii komórkowych pochodzących od pacjentów oraz modelu mysiego. Stwierdzili, że gdy NPM‑ALK był aktywny, STAT3 był oznakowany we wszystkich trzech miejscach, w tym w T714, a zablokowanie NPM‑ALK istniejącymi lekami usuwało te znaki. Pokazało to, że rakotwórcze białko fuzyjne bezpośrednio kontroluje T714 obok lepiej poznanych miejsc.
Co się dzieje, gdy przełącznik przy T714 jest usunięty
Aby sprawdzić, co faktycznie robi T714, badacze zaprojektowali mysie komórki krwi do ekspresji NPM‑ALK, następnie zredukowali ich naturalny STAT3 i zastąpili go albo wersją normalną, albo mutantem, w którym T714 został zmieniony tak, że nie mógł być oznakowany. Normalny STAT3 był prawidłowo modyfikowany w dwóch głównych miejscach kontrolnych, przemieszczał się do jądra komórkowego i włączał geny związane z rakiem, takie jak Cyclin D1 i geny z rodziny Pim. W przeciwieństwie do tego mutant T714 otrzymał tylko jeden z zwykłych znaków, pozostał głównie poza jądrem i nie aktywował tych genów. W rezultacie komórki z mutowanym STAT3 rosły wolniej, dzieliły się rzadziej i nie zyskały tej samej swobody od sygnałów wzrostu, którą zwykle zapewnia NPM‑ALK.
Od hodowli komórek do guzów u żywych myszy
Zespół zapytał następnie, czy to pojedyncze miejsce w STAT3 wpływa również na wzrost guzów u żywych zwierząt. Wstrzyknęli różne zaprojektowane komórki pod skórę myszy. Komórki z NPM‑ALK i normalnym STAT3 tworzyły duże guzy i powodowały powiększenie wątroby oraz śledziony u zwierząt, co odzwierciedla agresywną chorobę. Gdy STAT3 został stłumiony, wzrost guzów spadł gwałtownie. Przywrócenie normalnego STAT3 odtworzyło w dużym stopniu zdolność do tworzenia guzów, ale przywrócenie mutanta T714 nie. Myszy otrzymujące komórki z białkiem mutantem miały znacznie mniejsze guzy i niemal normalne rozmiary narządów. Wyniki te powiązały maleńką fosforanową etykietę przy T714 z pełną zdolnością do wywoływania raka w tym modelu.
Co to oznacza dla przyszłych terapii przeciwnowotworowych
W sumie wyniki sugerują, że T714 działa jak włącznik upstream dla STAT3 w komórkach napędzanych przez NPM‑ALK, pomagając umożliwić późniejsze zmiany pozwalające STAT3 wejść do jądra i włączyć geny wzrostu. Dla laików oznacza to, że zamiast celować tylko w główne widoczne przyciski na ścieżce nowotworowej, możliwe może być także wymierzenie w ukryty przełącznik primerski, który przygotowuje system do aktywacji. Leki zaprojektowane tak, by blokować znakowanie STAT3 przy T714 lub enzym wykonujący ten krok, mogłyby zaoferować nowy sposób uciszenia nadaktywnego sygnału wzrostu w ALCL, a być może także w innych nowotworach opierających się na podobnych białkach fuzyjnych.
Cytowanie: Lin, X., Yao, Y., Moriwaki, Y. et al. A critical role for STAT3 Thr714 phosphorylation in NPM-ALK-driven tumorigenesis. Sci Rep 16, 15005 (2026). https://doi.org/10.1038/s41598-026-44867-w
Słowa kluczowe: STAT3, NPM-ALK, anaplastyczny chłoniak z dużych komórek, fosforylacja, nowotworzenie