Clear Sky Science · ar
دور حاسم لفوسفorylation ثريونين STAT3 عند الموضع 714 في نشوء الأورام المدفوعة بـ NPM-ALK
كيف يمكن لمفتاح صغير في الخلايا السرطانية أن يغير مصيرها
غالبًا ما تستولي السرطان على أنظمة التحكم الطبيعية في الجسم، محولة إشارات خلوية عادية إلى أوامر مستمرة بالنمو والانقسام. تدرس هذه الدراسة واحدًا من هذه المفاتيح الداخلية داخل خلايا الجهاز المناعي المشاركة في نوع من سرطانات الدم يُدعى اللمفوما كبيرة الخلايا اللانمطية (ALCL). من خلال التركيز على علامة كيميائية واحدة مرتبطة ببروتين رئيسي، يبيّن الباحثون كيف يمكن لتغيير يبدو طفيفًا أن يقرر ما إذا كانت الخلايا السرطانية ستستمر في التكاثر أو تُحبَط.
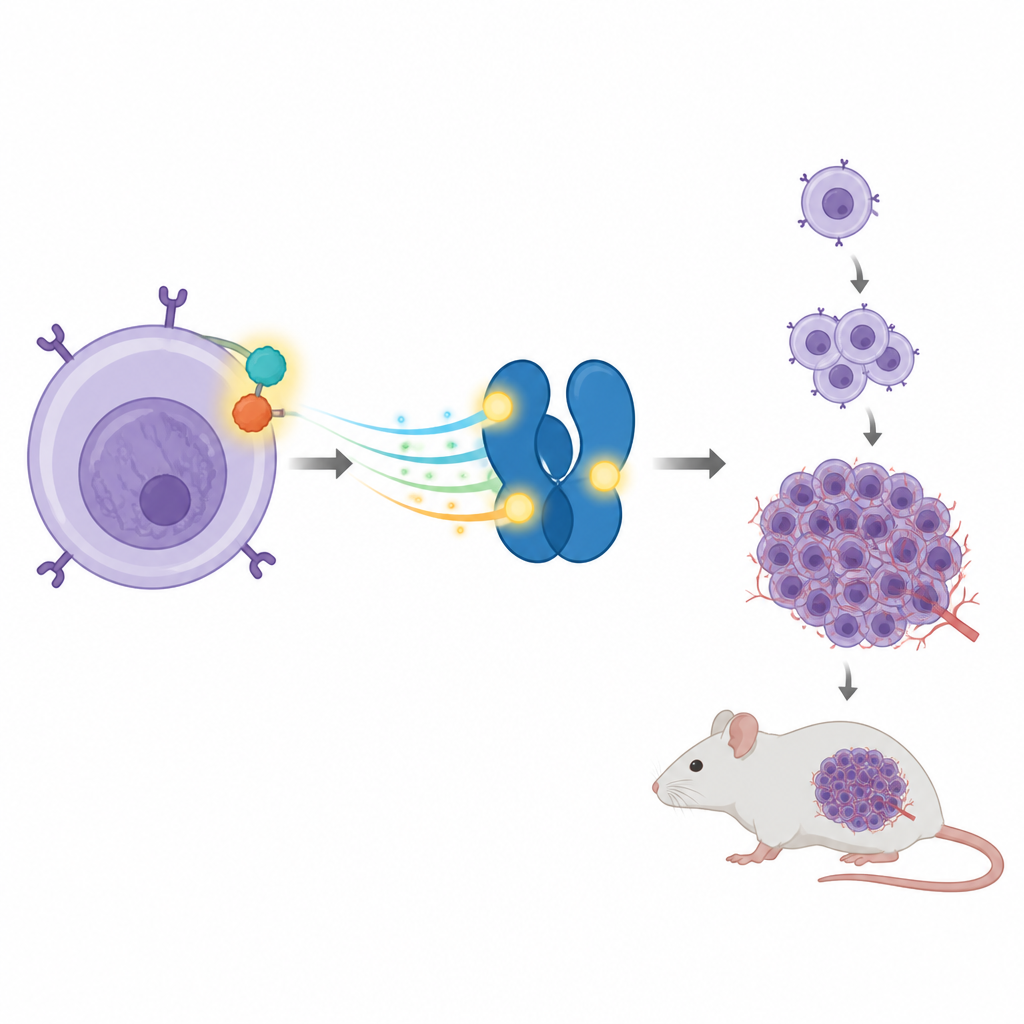
شراكة محركة للسرطان داخل خلايا الجهاز المناعي
تحمل بعض أورام ALCL جينًا مكسورًا ومعاد الربط يُدمج بروتينين في واحد، يُدعى NPM‑ALK. يتصرف هذا البروتين المختلط كدواسة تسارع عالقة، مُرسلًا باستمرار إشارات النمو داخل الخلية. أحد أهدافه المفضلة هو بروتين آخر يُسمى STAT3، الذي يساعد الخلايا عادةً على الاستجابة للإشارات الخارجية عن طريق تشغيل أو إيقاف جينات محددة. في ALCL، يبقي NPM‑ALK STAT3 مُفعّلًا، ما يؤدي بدوره إلى تعزيز جينات تدفع الخلايا إلى الانقسام والبقاء عندما لا ينبغي لها ذلك.
موقع تحكم جديد على بروتين مألوف
يعمل STAT3 فقط عندما تُعرَّف مواقع صغيرة عليه بمجموعة فوسفات، وهي عملية تُسمى الفسفرة. كان معروفًا أن موقعين من هذه المواقع مهمان، لكن دور الموقع الثالث المسمى T714 لم يكن واضحًا. ابتكر الفريق جسمًا مضادًا مخصّصًا يمكنه التعرف على STAT3 فقط عندما يكون هذا الموقع مصفَّرًا، واستخدمه لدراسة خطوط خلايا سرطانية مأخوذة من مرضى ونموذج خلوي فأري. وجدوا أنه عند نشاط NPM‑ALK، كان STAT3 مصفَّرًا عند المواقع الثلاثة بما في ذلك T714، وأن حجب NPM‑ALK بأدوية متوفرة أزال هذه الوسوم. أبان ذلك أن البروتين الانصهاري المحرِّك للسرطان يتحكم مباشرةً في T714 إلى جانب المواقع المعروفة أفضل.
ماذا يحدث عندما يُزال المفتاح عند T714
لاختبار وظيفة T714 فعليًا، مهندس الباحثون خلايا دموية فأرية للتعبير عن NPM‑ALK، ثم قللوا من مستوى STAT3 الطبيعي فيها واستبدلوه إما بالنسخة الطبيعية أو بنسخة متحولة اُستبدِل فيها T714 بحيث لا يمكن وسمها. أصبح STAT3 الطبيعي مُعدَّلًا بشكل صحيح عند موقعي التحكم الرئيسيين، وانتقل إلى نواة الخلية وشغّل جينات مرتبطة بالسرطان مثل Cyclin D1 وجينات عائلة Pim. بالمقابل، حصل الطفرة عند T714 على وسم واحد فقط من الأوسمة الاعتيادية، وبقيت في الغالب خارج النواة وفشلت في تنشيط هذه الجينات. نتيجة لذلك، نمت الخلايا الحاملة للSTAT3 المتحور بوتيرة أبطأ، وانقسمت أقل، ولم تكتسب نفس التحرر من إشارات النمو الذي يوفره عادة NPM‑ALK.
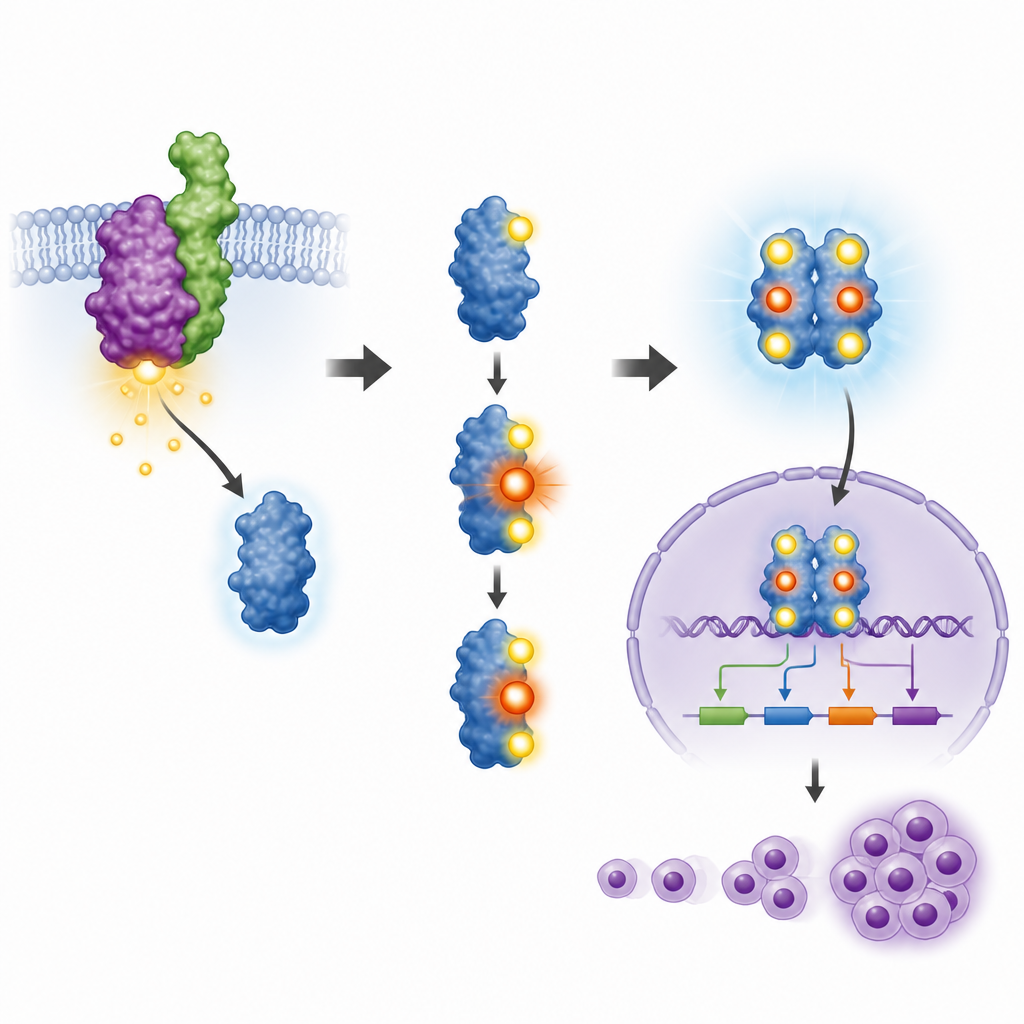
من مزرعة الخلايا إلى أورام في الفئران الحية
تساءل الفريق بعد ذلك ما إذا كان هذا الموقع الفردي على STAT3 يؤثر أيضًا في نمو الأورام في الحيوانات الحية. حقنوا الخلايا المهندسة مختلفة التكوين تحت جلد الفئران. تكوَّنت أورام كبيرة لدى الخلايا التي تحوي NPM‑ALK وSTAT3 الطبيعي وأدت إلى تضخّم كبد الطيور والطحال لدى الحيوانات، معبرة عن مرض عدواني. عند قمع STAT3، انخفض نمو الورم بشكل حاد. أعاد إدخال STAT3 الطبيعي جزءًا كبيرًا من القدرة على تشكيل الأورام، بينما لم يُعد إدخال الطفرة عند T714 هذه القدرة. كانت الأورام في الفئران التي تلقت خلايا تحتوي على البروتين المتحوّر أصغر بكثير وكانت أحجام الأعضاء قريبة من الطبيعي. ربطت هذه النتائج الوسم الفسفاتي الصغير عند T714 بالقوة المسببة للسرطان في هذا النموذج.
ما دلالة ذلك على علاجات السرطان المستقبلية
تشير النتائج مجتمعة إلى أن T714 يعمل كمفتاح تفعيل علوي لـ STAT3 في الخلايا المدفوعة بـ NPM‑ALK، مسهِّلًا تغييرات لاحقة تسمح لـ STAT3 بدخول النواة وتشغيل جينات النمو. للمختصين غير المتخصصين، يعني هذا أنه بدلًا من استهداف الأزرار الظاهرة الرئيسية في مسار السرطان فقط، قد يكون من الممكن أيضًا أن نركّز على مفتاح أولي مخفي يُهيئ النظام للتفعيل. قد توفر الأدوية المصممة لمنع وسم STAT3 عند T714، أو منع الإنزيم الذي يقوم بهذه الخطوة، وسيلة جديدة لكبح إشارة النمو المفرطة في ALCL وربما في سرطانات أخرى تعتمد على بروتينات انصهارية مماثلة.
الاستشهاد: Lin, X., Yao, Y., Moriwaki, Y. et al. A critical role for STAT3 Thr714 phosphorylation in NPM-ALK-driven tumorigenesis. Sci Rep 16, 15005 (2026). https://doi.org/10.1038/s41598-026-44867-w
الكلمات المفتاحية: STAT3, NPM-ALK, اللمفوما كبيرة الخلايا اللانمطية, فوسفorylation, تكوّن الأورام