Clear Sky Science · ru
scTWAS: мощная статистическая платформа для ассоциативных исследований транскриптома на уровне одиночных клеток
Почему изучение одиночных клеток может изменить медицину
Большинство генетических исследований болезней напоминают прослушивание толпы: слышен общий шум, но упускается то, что говорит каждый человек. В этой работе показано, как настроить «уши» на отдельные голоса. Авторы представляют scTWAS — новый подход, связывающий различия в ДНК с болезнями через изучение активности генов в конкретных типах клеток и даже в более тонких подтипах, используя данные одно-клеточного секвенирования РНК. Такой более чёткий обзор выявляет, какие именно клетки — и какие гены в них — являются движущими силами состояний, таких как заболевания крови, аутоиммунные болезни и болезнь Альцгеймера.
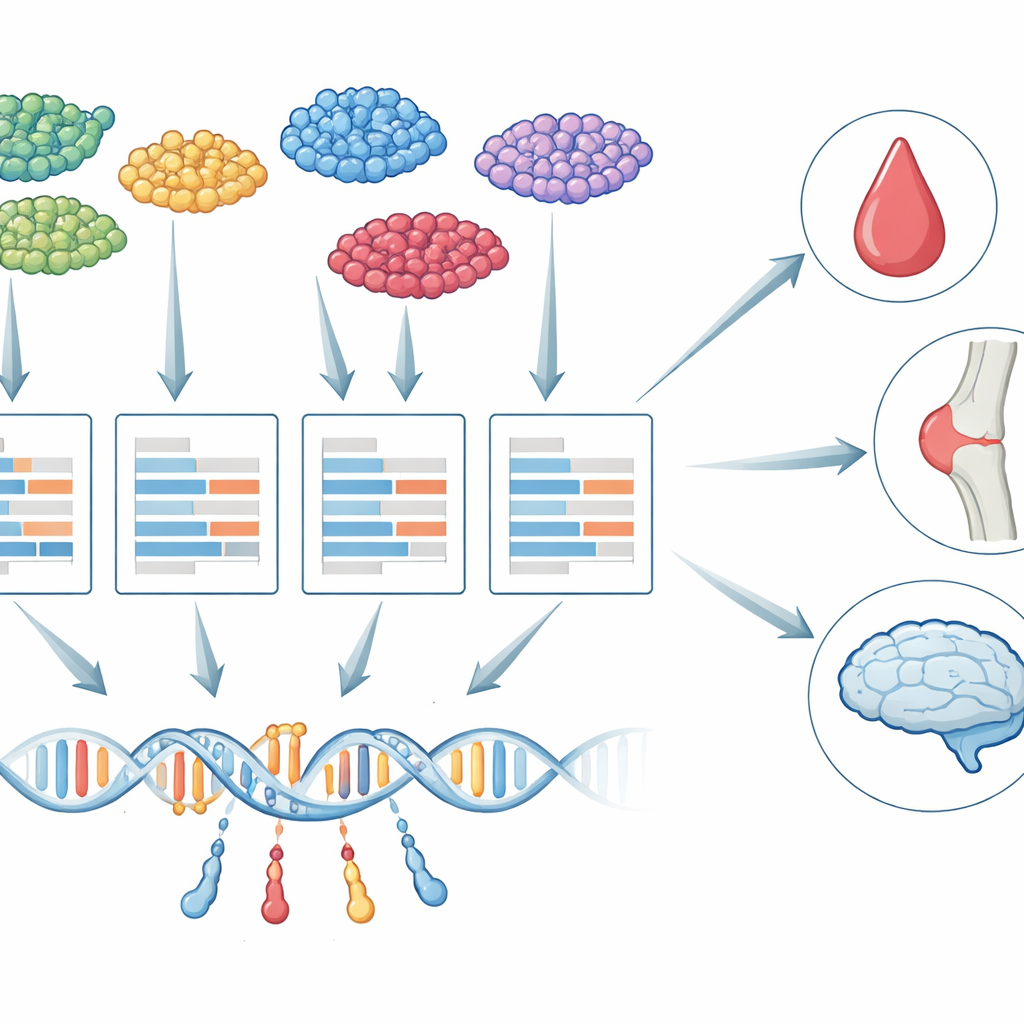
От сплошных тканей к одиночным клеткам
В течение более десяти лет исследователи использовали метод, называемый ассоциативными исследованиями по транскриптомному профилю (TWAS), для связи генетических вариантов с заболеваниями. TWAS работает в два этапа: сначала он изучает, как изменения в ДНК влияют на активность генов, затем проверяет, связана ли генетически спрогнозированная активность каждого гена с признаком, например количеством тромбоцитов или риском деменции. До сих пор почти все работы по TWAS опирались на «bulk» образцы тканей, где РНК от многих типов клеток смешана вместе. Такое смешение скрывает важные различия: генетическое регулирование гена в микроглии мозга, например, может сильно отличаться от того же гена в нейроне, и лишь некоторые из этих клеток действительно могут иметь значение для конкретного заболевания.
Проблема шумных данных одиночных клеток
Новые масштабные одно-клеточные исследования РНК теперь позволяют измерять тысячи отдельных клеток у каждого человека, по многим людям. Но эти данные шумные: счёты разрежены (много нулей), сильно зависят от технических особенностей эксперимента и значительно варьируют от клетки к клетке даже при одинаковой биологии. Ранее попытки подставить данные одиночных клеток в TWAS использовали произвольные приёмы нормализации, заимствованные из методов для bulk-РНК, в надежде, что они усмирят шум. Авторы показывают, что такие упрощения могут искажать истинные генетические эффекты на активность генов, приводя к менее точным предсказаниям и меньшему числу обнаруженных связей «ген—болезнь», особенно в редких или труднодоступных типах клеток.
Как scTWAS очищает сигнал
scTWAS решает эти задачи, явно разделяя биологию и ошибки измерения. Сначала он агрегирует счёты одиночных клеток у каждого человека по типам клеток в «псевдо-bulk» профиль, уменьшая разреженность при сохранении идентичности типа клетки. Затем используется двухслойная статистическая модель: один слой описывает, как варианты ДНК и базовые характеристики, такие как возраст, влияют на истинную скрытую активность гена у человека в данном типе клетки; второй слой моделирует, как секвенатор превращает эту активность в шумные счёты, включая эффект различной глубины секвенирования. Подбирая параметры модели с помощью специализированного алгоритма взвешенной регрессии, scTWAS снижает вклад самых шумных образцов и точнее оценивает генетически регулируемую экспрессию каждого гена в каждом типе клетки.
Нахождение генов болезни там, где они действительно действуют
После обучения этих моделей предсказания по типам клеток, scTWAS интегрирует их в крупные исследования ассоциаций по всему геному, чтобы протестировать связи генов с признаками. В моделируемых данных, имитирующих реальные одно-клеточные эксперименты, scTWAS последовательно превосходил существующие методы по точности предсказаний и мощности обнаружения, с особенно большими приращениями для редких типов клеток, где данных меньше всего. Применение платформы к иммунным клеткам показало, что scTWAS выявляет существенно больше генов, связанных с 29 показателями крови, а также с ревматоидным артритом, волчанкой и астмой. Многие из этих сигналов указывают на конкретные типы иммунных клеток — например, определённые подмножества моноцитов или Т-клеток — как на основную «сцену», где те или иные гены влияют на риск болезни, и некоторые ассоциации были полностью пропущены при анализе bulk-крови.
Заглядывая в подтипы мозговых клеток при Альцгеймере
scTWAS становится ещё более информативным в мозге. Используя данные одноядерного секвенирования от сотен донорских образцов человеческого мозга, авторы построили модели предсказания для шести основных типов мозговых клеток и 75 более тонких подтипов. Затем они сопоставили эти модели с генетическими данными по болезни Альцгеймера, чтобы отобразить, где на клеточном уровне вероятнее всего действуют гены риска. Некоторые гены проявляют активность во многих типах клеток, что указывает на широкую роль в мозге, в то время как другие показывают поразительную специфичность. Например, известный ген риска MS4A6A демонстрирует сильную ассоциацию только в подтипе микроглии, связанном с переработкой липидов, а PPP1R37 ассоциируется лишь в воспалительном подтипе микроглии рядом с хорошо известной областью риска APOE. Такие закономерности указывают на то, что специфические состояния микроглии являются ключевыми звеньями в том, как отдельные генетические варианты повышают риск Альцгеймера.

Что это значит для будущих терапий
Для неспециалиста главный вывод таков: место, где действует ген, может быть так же важно, как и то, что делает ген. Перенеся TWAS от смешанных тканей к точным типам и подтипам клеток и аккуратно смоделировав особенности измерений одиночных клеток, scTWAS выявляет связи «ген—болезнь», которые ранее были невидимы. Эта более чёткая карта помогает исследователям сосредоточиться на точных популяциях клеток и путях, которые следует нацеливать для разработки новых лекарств или вмешательств — от формирования крови и иммунитета до иммунных клеток мозга при болезни Альцгеймера.
Цитирование: Lin, Z., Su, C. scTWAS: a powerful statistical framework for single-cell transcriptome-wide association studies. Nat Commun 17, 3853 (2026). https://doi.org/10.1038/s41467-026-70374-7
Ключевые слова: геномика одиночных клеток, картирование генетического риска, иммунные клетки, болезнь Альцгеймера, статистическая генетика