Clear Sky Science · nl
scTWAS: een krachtig statistisch kader voor transcriptoom-brede associatiestudies op enkelcelniveau
Waarom kijken naar individuele cellen de geneeskunde kan veranderen
De meeste genetische ziekteonderzoeken werken alsof je naar een menigte luistert: je hoort een algemene lawaai, maar mist wat ieder individu zegt. Dit artikel laat zien hoe we onze oren op afzonderlijke stemmen kunnen afstemmen. De auteurs introduceren scTWAS, een nieuwe manier om DNA-varianten aan ziekten te koppelen door te kijken naar genactiviteit in specifieke celtypen en zelfs fijnere celsubtypen, met behulp van single-cell RNA-sequencinggegevens. Die scherpere blik onthult welke exacte cellen — en welke genen in die cellen — aandoeningen aandrijven zoals bloedziekten, auto-immuunaandoeningen en de ziekte van Alzheimer.
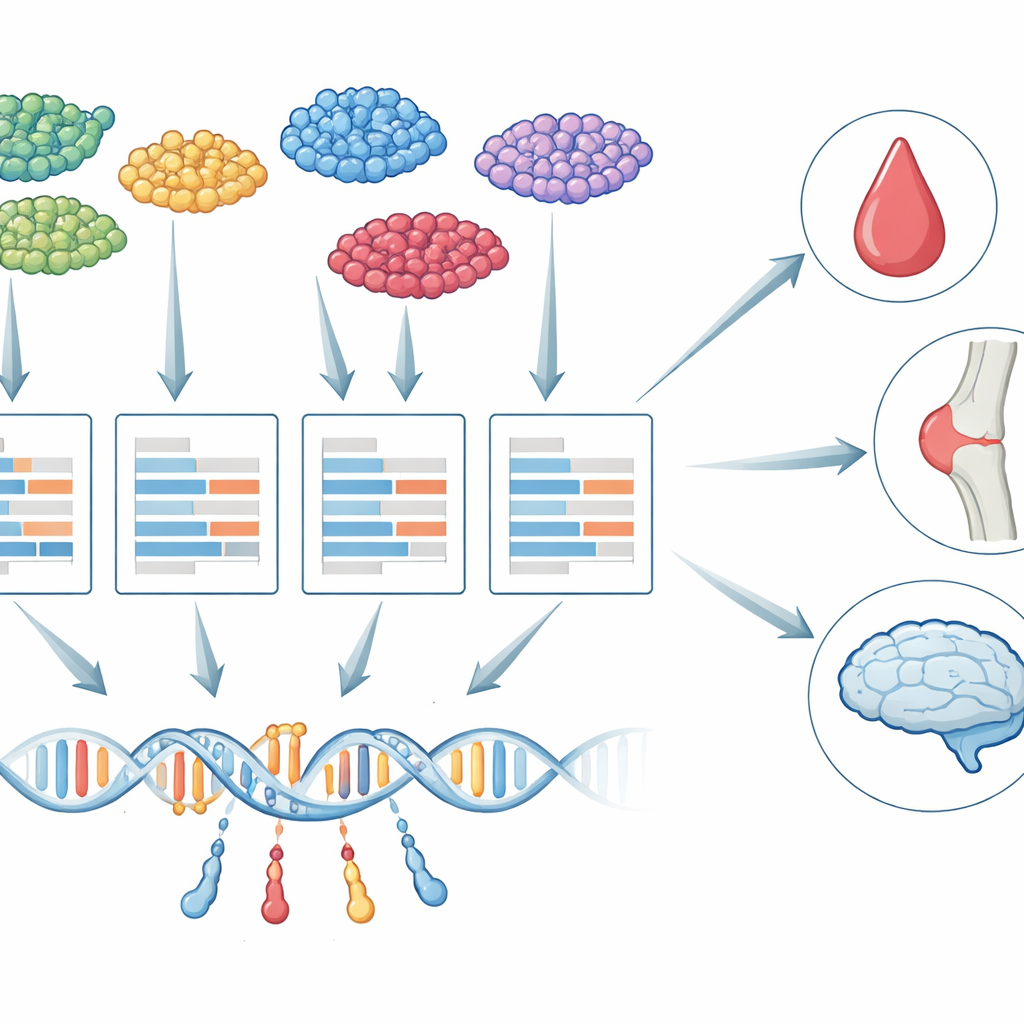
Van bulkweefsel naar individuele cellen
Meer dan tien jaar gebruiken onderzoekers een strategie genaamd transcriptoom-brede associatiestudies (TWAS) om genetische varianten aan ziekten te koppelen. TWAS werkt in twee stappen: eerst leert het hoe DNA-veranderingen genactiviteit beïnvloeden, en vervolgens test het of de genetisch voorspelde activiteit van elk gen samenhangt met een eigenschap zoals bloedplaatjestelling of dementierisico. Tot nu toe berust vrijwel al het TWAS-werk op “bulk” weefselmonsters, waarbij RNA van veel celtypen wordt samengevoegd. Die vermenging verbergt belangrijke verschillen: de genetische controle van een gen in een microgliale cel in de hersenen kan bijvoorbeeld sterk afwijken van hetzelfde gen in een neuron, en slechts sommige van die cellen kunnen daadwerkelijk relevant zijn voor een bepaalde ziekte.
Het probleem van rumoerige single-cell-gegevens
Nieuw bevolkingsbreed single-cell RNA-sequencing maakt het nu mogelijk duizenden individuele cellen per persoon te meten, over veel mensen heen. Maar deze gegevens zijn rommelig: tellingen zijn schaars (veel nullen), sterk beïnvloed door technische eigenaardigheden van het experiment, en variëren sterk van cel tot cel zelfs wanneer de biologische situatie gelijk is. Eerdere pogingen om single-cell-gegevens in TWAS te gebruiken, pasten ad-hoc normalisatietrucs toe uit bulk-RNA-methoden in de hoop die ruis te temmen. De auteurs tonen aan dat dergelijke shortcuts de werkelijke genetische effecten op genactiviteit kunnen vervormen, wat leidt tot zwakkere voorspellingen en minder ontdekte gen–ziekte koppelingen, vooral in zeldzame of moeilijk te karakteriseren celtypen.
Hoe scTWAS het signaal schoonmaakt
scTWAS pakt deze uitdagingen aan door expliciet biologie te scheiden van meetfouten. Eerst aggregeert het single-cell-tellinggegevens per persoon en celtype tot een “pseudo-bulk” profiel, waardoor schaarste vermindert terwijl de celtype-identiteit behouden blijft. Vervolgens gebruikt het een tweelagen statistisch model: de ene laag beschrijft hoe DNA-varianten en basiskenmerken zoals leeftijd de werkelijke onderliggende genactiviteit van een persoon in een bepaald celtype beïnvloeden; de andere laag modelleert hoe de sequencer die activiteit omzet in rumoerige tellingen, inclusief het effect van variërende sequencing-diepte. Door dit model te passen met een gespecialiseerde gewogen regressie-algoritme, weegt scTWAS de luidruchtigste monsters minder zwaar en schat het de genetisch gereguleerde expressie voor elk gen in elk celtype nauwkeuriger.
Ziektegenen vinden op de plek waar ze echt werken
Zodra deze celtype-specifieke predictiemodellen zijn getraind, plugt scTWAS ze in grote genome-wide associatiestudies om op gen–eigenschap-koppelingen te testen. In gesimuleerde data die echte single-cell-experimenten nabootsen, presteerde scTWAS consequent beter dan bestaande methoden in zowel voorspellingsnauwkeurigheid als statistische kracht, met bijzonder grote winst voor zeldzame celtypen waar data het schaarst zijn. Toegepast op immuuncellen laten de auteurs zien dat scTWAS aanzienlijk meer genen identificeert die geassocieerd zijn met 29 bloedkenmerken en met reumatoïde artritis, lupus en astma. Veel van deze signalen wijzen op specifieke immuunceltypen — zoals bepaalde monocyten- of T-celsubsets — als het belangrijkste toneel waarop bepaalde genen het ziekterisico beïnvloeden, en sommige associaties werden volledig gemist door bulk-bloedanalyses.
Kijken naar hersencelsubtypen bij Alzheimer
scTWAS wordt nog onthullender in de hersenen. Met single-nucleus-gegevens van honderden geschonken menselijke hersenen bouwden de auteurs predictiemodellen voor zes grote hersenceltypen en 75 fijnere subtypen. Ze combineerden deze vervolgens met genetische gegevens over de ziekte van Alzheimer om in kaart te brengen waar, op cellulaire resolutie, risicogenen waarschijnlijk actief zijn. Sommige genen komen in veel celtypen voor, wat duidt op brede rollen in de hersenen, terwijl andere opvallend specifiek zijn. Bijvoorbeeld, een bekend risicogen, MS4A6A, toont een sterke associatie alleen in een ziektegerelateerd microgliaal subtype gekoppeld aan lipideverwerking, en PPP1R37 is alleen geassocieerd in een inflammatoir microgliaal subtype dicht bij het bekende APOE-risicogebied. Deze patronen wijzen op onderscheiden microgliale toestanden als sleutelfactoren in hoe bepaalde genetische varianten het Alzheimer-risico aansturen.

Wat dit betekent voor toekomstige therapieën
Voor niet-specialisten is de belangrijkste boodschap dat waar een gen werkt net zo belangrijk kan zijn als wat het gen doet. Door TWAS te verplaatsen van samengevoegde weefsels naar precieze celtypen en subtypen, en door zorgvuldig de eigenaardigheden van single-cell-metingen te modelleren, onthult scTWAS gen–ziekteverbindingen die eerder onzichtbaar waren. Deze scherpere kaart helpt onderzoekers zich te richten op de exacte celpopulaties en routes die als doelwit dienen voor nieuwe geneesmiddelen of interventies, van bloedvorming en immuniteit tot de immuuncellen van de hersenen bij de ziekte van Alzheimer.
Bronvermelding: Lin, Z., Su, C. scTWAS: a powerful statistical framework for single-cell transcriptome-wide association studies. Nat Commun 17, 3853 (2026). https://doi.org/10.1038/s41467-026-70374-7
Trefwoorden: single-cell genomics, genetic risk mapping, immune cells, Alzheimer’s disease, statistical genetics