Clear Sky Science · it
scTWAS: un potente quadro statistico per studi di associazione trascrittomica a singola cellula
Perché osservare le singole cellule può cambiare la medicina
La maggior parte degli studi genetici sulle malattie funziona come ascoltare una folla: si ode un boato complessivo ma non si colgono le parole di ciascuna persona. Questo articolo mostra come sintonizzare le nostre orecchie sulle singole voci. Gli autori presentano scTWAS, un nuovo metodo per collegare le differenze del DNA alle malattie osservando l'attività genica in tipi cellulari specifici e in sottotipi ancora più precisi, utilizzando dati di sequenziamento dell'RNA a singola cellula. Questa visione più nitida rivela quali cellule esatte — e quali geni al loro interno — stanno guidando condizioni come i disturbi del sangue, le malattie autoimmuni e la malattia di Alzheimer.
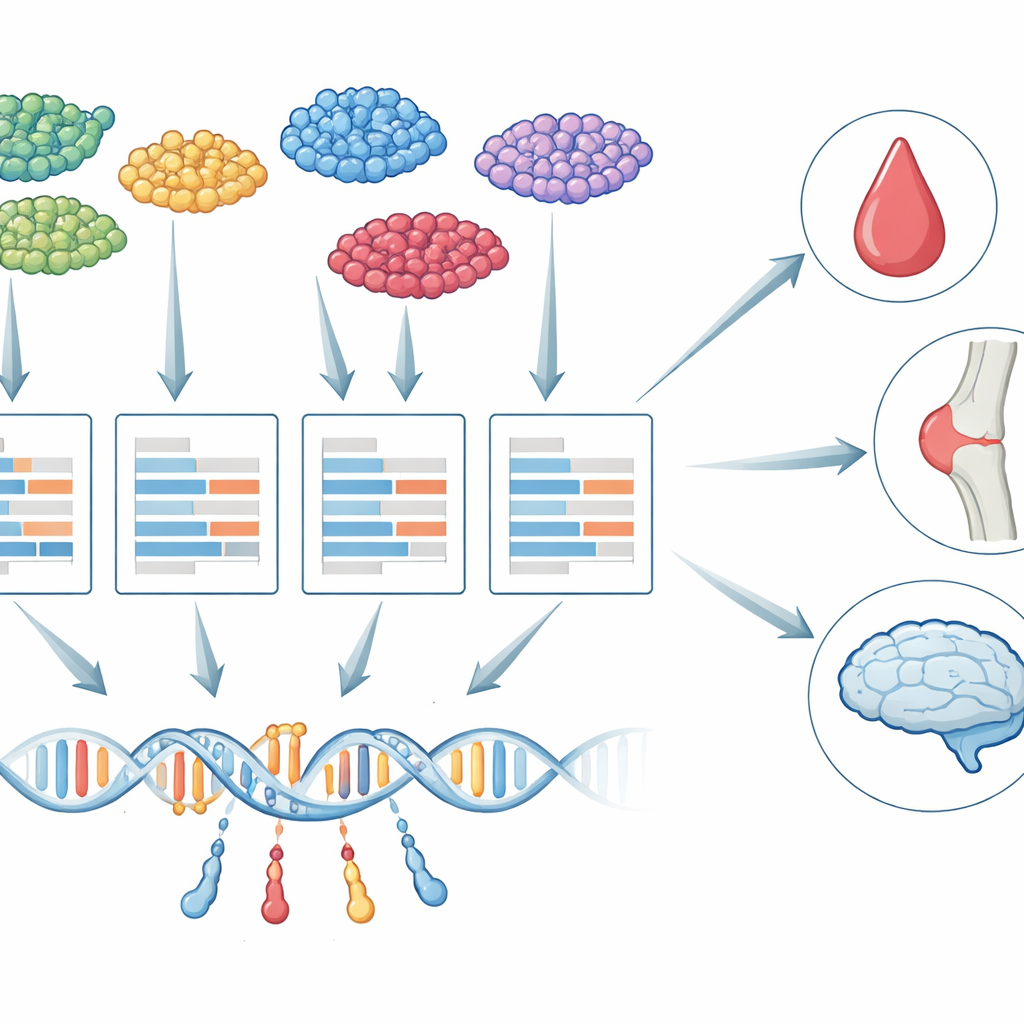
Dal tessuto omogeneo alle singole cellule
Per più di un decennio i ricercatori hanno usato una strategia chiamata studi di associazione trascrittomica (TWAS) per collegare varianti genetiche alle malattie. TWAS funziona in due fasi: prima apprende come le variazioni del DNA influenzano l'attività genica, poi testa se l'attività genica prevista geneticamente di ciascun gene è legata a un fenotipo come il numero di piastrine o il rischio di demenza. Finora, quasi tutto il lavoro TWAS si è basato su campioni di tessuto “bulk”, in cui l'RNA di molti tipi cellulari è mescolato. Questa mescolanza nasconde differenze importanti: il controllo genetico di un gene in una microglia nel cervello, per esempio, può essere molto diverso rispetto allo stesso gene in un neurone, e solo alcuni di quei tipi cellulari possono essere rilevanti per una data malattia.
Il problema dei dati a singola cellula rumorosi
Il nuovo sequenziamento dell'RNA a singola cellula su scala di popolazione ora rende possibile misurare migliaia di cellule individuali per persona, attraverso molti individui. Ma questi dati sono disordinati: i conteggi sono sparsi (molti zeri), fortemente influenzati da artefatti tecnici dell'esperimento e variano molto da cellula a cellula anche quando la biologia è la stessa. I tentativi precedenti di inserire i dati a singola cellula in TWAS hanno usato trucchi di normalizzazione ad hoc presi in prestito dai metodi per il bulk, sperando che queste fasi contenessero il rumore. Gli autori dimostrano che tali scorciatoie possono distorcere i veri effetti genetici sull'attività genica, portando a previsioni più deboli e a meno associazioni gene–malattia scoperte, in particolare nei tipi cellulari rari o difficili.
Come scTWAS pulisce il segnale
scTWAS affronta queste sfide separando esplicitamente la biologia dall'errore di misura. Innanzitutto aggrega i conteggi a singola cellula all'interno di ciascuna persona e tipo cellulare in un profilo “pseudo-bulk”, riducendo la sparsità mantenendo l'identità del tipo cellulare. Poi utilizza un modello statistico a due livelli: un livello descrive come le varianti del DNA e caratteristiche di base come l'età influenzano la vera attività genica sottostante di una persona in un dato tipo cellulare; l'altro livello modella come la macchina di sequenziamento trasforma quell'attività in conteggi rumorosi, incluso l'effetto della diversa profondità di sequenziamento. Adattando questo modello con un algoritmo di regressione ponderata specializzato, scTWAS declassa i campioni più rumorosi e stima in modo più accurato l'espressione regolata geneticamente per ciascun gene in ogni tipo cellulare.
Trovare i geni della malattia dove agiscono davvero
Una volta addestrati questi modelli di previsione specifici per tipo cellulare, scTWAS li integra in ampi studi di associazione genome-wide per testare i legami gene–fenotipo. Nei dati simulati che mimano esperimenti reali a singola cellula, scTWAS ha costantemente superato i metodi esistenti sia in accuratezza di previsione sia in potenza statistica, con guadagni particolarmente ampi per i tipi cellulari rari dove i dati sono più scarsi. Applicando il quadro alle cellule immunitarie, gli autori mostrano che scTWAS identifica un numero sostanzialmente maggiore di geni associati a 29 caratteristiche del sangue e a artrite reumatoide, lupus e asma. Molti di questi segnali evidenziano tipi cellulari immunitari particolari — come specifici sottogruppi di monociti o cellule T — come il palcoscenico principale su cui certi geni influenzano il rischio di malattia, e alcune associazioni sono state del tutto trascurate dalle analisi su sangue bulk.
Scrutare i sottotipi cellulari cerebrali nell’Alzheimer
scTWAS diventa ancora più rivelatore nel cervello. Utilizzando dati da nuclei singoli di centinaia di cervelli umani donati, gli autori hanno costruito modelli di previsione per sei principali tipi cellulari cerebrali e 75 sottotipi più fini. Li hanno poi combinati con dati genetici sulla malattia di Alzheimer per mappare dove, a risoluzione cellulare, i geni di rischio sono probabilmente attivi. Alcuni geni compaiono in molti tipi cellulari, suggerendo ruoli ampi nel cervello, mentre altri sono sorprendentemente specifici. Per esempio, un gene di rischio noto, MS4A6A, mostra una forte associazione solo in un sottotipo di microglia associato alla malattia e legato alla gestione dei lipidi, e PPP1R37 è associato solo in un sottotipo microgliale infiammatorio vicino alla nota regione di rischio APOE. Questi schemi indicano stati microgliali distinti come attori chiave nei meccanismi con cui certe varianti genetiche aumentano il rischio di Alzheimer.

Cosa significa per le terapie future
Per un non specialista, il messaggio principale è che il luogo in cui un gene agisce può essere importante quanto ciò che il gene fa. Spostando il TWAS dai tessuti mescolati a tipi cellulari e sottotipi precisi, e modellando con cura le peculiarità delle misurazioni a singola cellula, scTWAS scopre connessioni gene–malattia precedentemente invisibili. Questa mappa più nitida aiuta i ricercatori a individuare le popolazioni cellulari e le vie esatte da mirare con nuovi farmaci o interventi, dalla formazione del sangue e l'immunità fino alle cellule immunitarie del cervello nella malattia di Alzheimer.
Citazione: Lin, Z., Su, C. scTWAS: a powerful statistical framework for single-cell transcriptome-wide association studies. Nat Commun 17, 3853 (2026). https://doi.org/10.1038/s41467-026-70374-7
Parole chiave: genomica a singola cellula, mappatura del rischio genetico, cellule immunitarie, malattia di Alzheimer, genetica statistica