Clear Sky Science · ar
scTWAS: إطار إحصائي قوي لدراسات الارتباط في المجموع الكلي للنسخ على مستوى الخلية المفردة
لماذا قد يغيّر النظر إلى الخلايا المفردة الطب
تعمل معظم الدراسات الجينية للأمراض مثل الاستماع إلى حشد: تسمع ضجيجاً إجمالياً لكنها تفقد ما يقوله كل فرد بمفرده. تُبيّن هذه الورقة كيف يمكن ضبط آذاننا لسماع الأصوات الفردية. يقدم المؤلفون scTWAS، طريقة جديدة لربط اختلافات الحمض النووي بالأمراض من خلال فحص نشاط الجينات في أنواع خلايا محددة وحتى في فئات فرعية أدق من الخلايا، باستخدام بيانات تسلسل الحمض النووي الريبوزي على مستوى الخلية المفردة. هذا النظر الأدق يكشف أي الخلايا بالضبط — وأي الجينات داخلها — هي التي تقود حالات مثل اضطرابات الدم والأمراض المناعية الذاتية ومرض ألزهايمر.
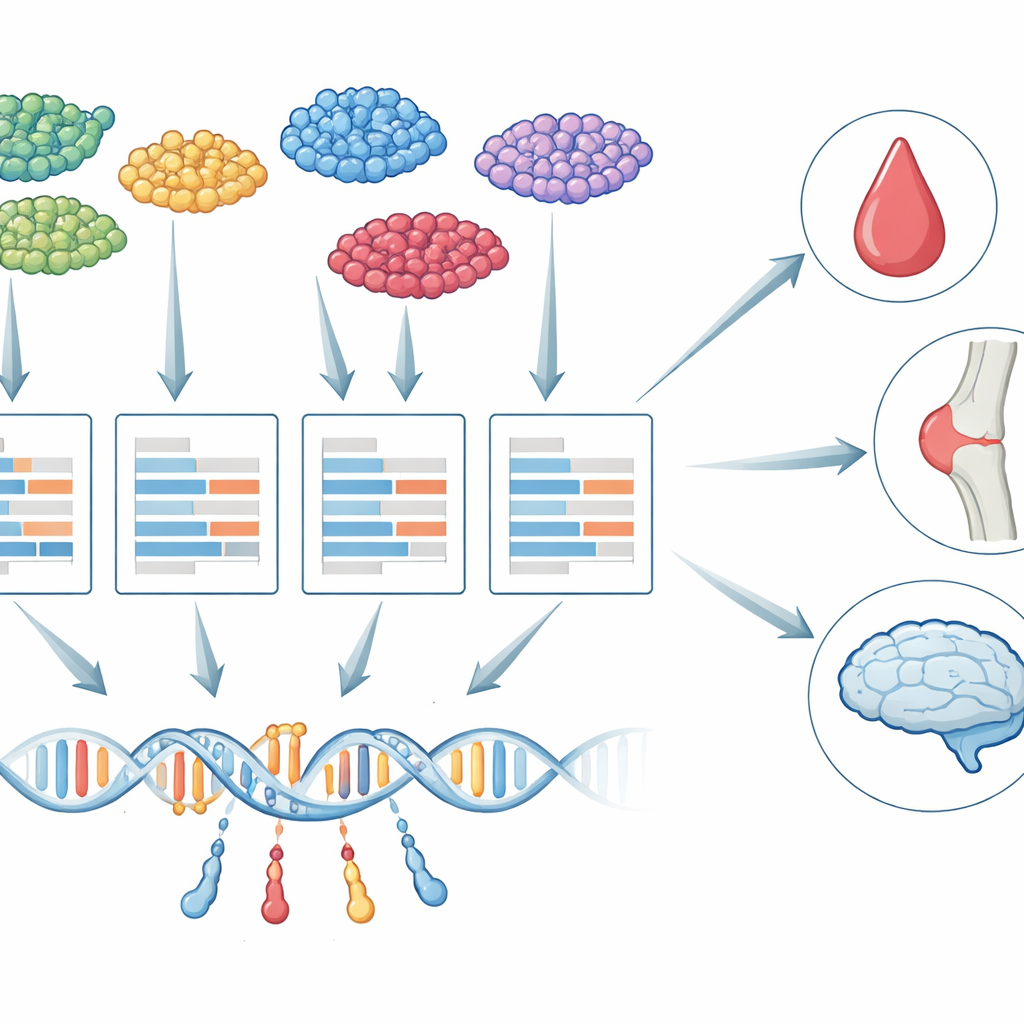
من الأنسجة المجمعة إلى الخلايا المفردة
على مدار أكثر من عقد من الزمن، استخدم الباحثون استراتيجية تُسمى دراسات الارتباط على مستوى المجموع الكلي للنسخ (TWAS) لربط المتغيرات الجينية بالأمراض. تعمل TWAS على خطوتين: أولاً تتعلم كيف تؤثر تغييرات الحمض النووي على نشاط الجينات، ثم تختبر ما إذا كان النشاط المتوقع وراثياً لكل جين مرتبطاً بصفة مثل عدد الصفيحات أو خطر الخرف. حتى الآن، اعتمدت معظم أعمال TWAS على عينات الأنسجة "المجمعة"، حيث يتم خلط الحمض النووي الريبوزي من أنواع خلايا عديدة معاً. هذا الخلط يخفي اختلافات مهمة: قد يكون التحكم الجيني في جين ما داخل خلية ميكروغليا في الدماغ مختلفاً جداً عن نفس الجين في خلية عصبية، وربما تكون فقط بعض هذه الخلايا هي المهمة فعلاً لمرض معين.
مشكلة الضجيج في بيانات الخلية المفردة
تجعل بيانات تسلسل الحمض النووي الريبوزي على مستوى الخلية المفردة على نطاق السكان من الممكن الآن قياس آلاف الخلايا الفردية لكل شخص، عبر كثير من الأشخاص. لكن هذه البيانات فوضوية: العدّادات متفرقة (العديد من القيم صفر)، وتتأثر بشدة بشوائب تقنية في التجربة، وتختلف كثيراً من خلية لأخرى حتى عندما تكون البيولوجيا متماثلة. المحاولات السابقة لدمج بيانات الخلية المفردة داخل TWAS استخدمت حيل تطبيع ارتجالية مستعارة من طرق الأنسجة المجمعة، على أمل أن تكبح هذه الخطوات الضجيج. يظهر المؤلفون أن مثل هذه الطرق المختصرة يمكن أن تشوّه التأثيرات الجينية الحقيقية على نشاط الجين، مما يؤدي إلى تنبؤات أضعف وعدد أقل من الروابط المعلنة بين الجين والمرض، لا سيما في أنواع الخلايا النادرة أو الصعبة.
كيف ينقّي scTWAS الإشارة
يتعامل scTWAS مع هذه التحديات بفصل البيولوجيا بوضوح عن خطأ القياس. أولاً، يجمع عدّادات الخلايا المفردة داخل كل شخص ونوع خلية إلى ملف تعريف "شبه مجمع"، مما يقلّل التفرّق مع الحفاظ على هوية نوع الخلية. ثم يستخدم نموذجاً إحصائياً ذو طبقتين: تصف طبقة كيف تؤثر المتغيرات الجينية وخصائص أساسية مثل العمر على النشاط الحقيقي الكامن للجين لدى شخص ما في نوع خلية معين؛ وتُحدّد الطبقة الأخرى كيف يحول جهاز التسلسل ذلك النشاط إلى عدّادات مضطربة، بما في ذلك تأثير اختلاف عمق التسلسل. عبر ملاءمة هذا النموذج بخوارزمية انحدار موزونة متخصصة، يقلل scTWAS وزن العيّنات الأكثر ضجيجاً ويقدّر بدقة أكبر التعبير المنظم وراثياً لكل جين في كل نوع خلية.
العثور على جينات الأمراض حيث تعمل فعلاً
بمجرد تدريب نماذج التنبؤ الخاصة بكل نوع خلية، يدمج scTWAS هذه النماذج في دراسات الارتباط الواسعة عبر الجينوم لاختبار روابط الجين والصفة. في بيانات محاكاة تحاكي تجارب الخلية المفردة الحقيقية، تفوق scTWAS باستمرار على الطرق الموجودة من حيث دقة التنبؤ والقوة، مع مكاسب كبيرة بشكل خاص لأنواع الخلايا النادرة حيث تكون البيانات أكثر ندرة. بتطبيق الإطار على الخلايا المناعية، يُظهر المؤلفون أن scTWAS يحدد عدداً أكبر بكثير من الجينات المرتبطة بـ 29 سمة دموية وبالالتهاب المفصلي الروماتويدي والذئبة والربو. تبرز العديد من هذه الإشارات أنواع خلايا مناعية معينة — مثل مجموعات فرعية محددة من الخلايا الوحيدة أو الخلايا التائية — كساحة رئيسية تعمل عليها جينات معينة لتؤثر في خطر المرض، وبعض الارتباطات فُقدت تماماً في تحليلات الدم المجمعة.
التعمق في الفئات الفرعية لخلايا الدماغ في مرض ألزهايمر
يصبح scTWAS أكثر كشفاً في الدماغ. باستخدام بيانات نوى مفردة من مئات الأدمغة البشرية المتبرع بها، بنى المؤلفون نماذج تنبؤ لستة أنواع خلوية دماغية رئيسية و75 فئة فرعية أدق. ثم جمعوا هذه النماذج مع بيانات جينية لمرض ألزهايمر لرسم خريطة على مستوى الخلية أين من المرجح أن تعمل جينات الخطر. يظهر بعض الجينات عبر العديد من أنواع الخلايا، مما يوحي بأدوار واسعة في الدماغ، بينما يكون البعض الآخر محدداً بشكل لافت. على سبيل المثال، يُظهر جين خطر معروف، MS4A6A، ارتباطاً قوياً فقط في فئة ميكروغليا مرتبطة بالمرض وتتعلق بالتعامل مع الدهون، ويرتبط PPP1R37 فقط في فئة ميكروغليا التهابية قريبة من منطقة الخطر المعروفة APOE. تشير هذه الأنماط إلى حالات ميكروغليا متميزة كعوامل رئيسية في كيفية دفع متغيرات جينية معينة لخطر ألزهايمر.

ماذا يعني هذا للعلاجات المستقبلية
بالنسبة لغير المتخصص، الرسالة الرئيسية أن المكان الذي يعمل فيه الجين قد يكون مهماً بقدر ما يفعل الجين نفسه. عبر نقل TWAS من الأنسجة المخلوطة إلى أنواع وخلايا فرعية دقيقة، وعن طريق نمذجة شوائب قياسات الخلية المفردة بعناية، يكشف scTWAS اتصالات بين الجين والمرض كانت غير مرئية سابقاً. تساعد هذه الخريطة الأدق الباحثين على التركيز على تجمعات الخلايا والمسارات الدقيقة التي ينبغي استهدافها لتطوير أدوية أو تدخلات جديدة، من تكون الدم والمناعة إلى خلايا الجهاز المناعي في الدماغ المرتبطة بمرض ألزهايمر.
الاستشهاد: Lin, Z., Su, C. scTWAS: a powerful statistical framework for single-cell transcriptome-wide association studies. Nat Commun 17, 3853 (2026). https://doi.org/10.1038/s41467-026-70374-7
الكلمات المفتاحية: علم الجينوم على مستوى الخلية المفردة, رسم خرائط المخاطر الجينية, الخلايا المناعية, مرض ألزهايمر, الوراثة الإحصائية