Clear Sky Science · ja
scTWAS: 単一細胞トランスクリプトーム全域関連解析のための強力な統計フレームワーク
なぜ単一細胞を観ることが医療を変えるのか
従来の多くの遺伝学的疾病研究は群衆のざわめきを聴くようなもので、全体の騒音は捉えるものの個々の声は聞き取れません。本論文は個々の声に耳を澄ます方法を示します。著者らは scTWAS を導入し、単一細胞RNAシーケンシングデータを用いて特定の細胞型やさらに細かな細胞亜型における遺伝的差異と疾病を結びつけます。その鮮明な視点により、血液疾患、自己免疫疾患、アルツハイマー病などの原因となる正確な細胞群と、その内部で働く遺伝子が明らかになります。
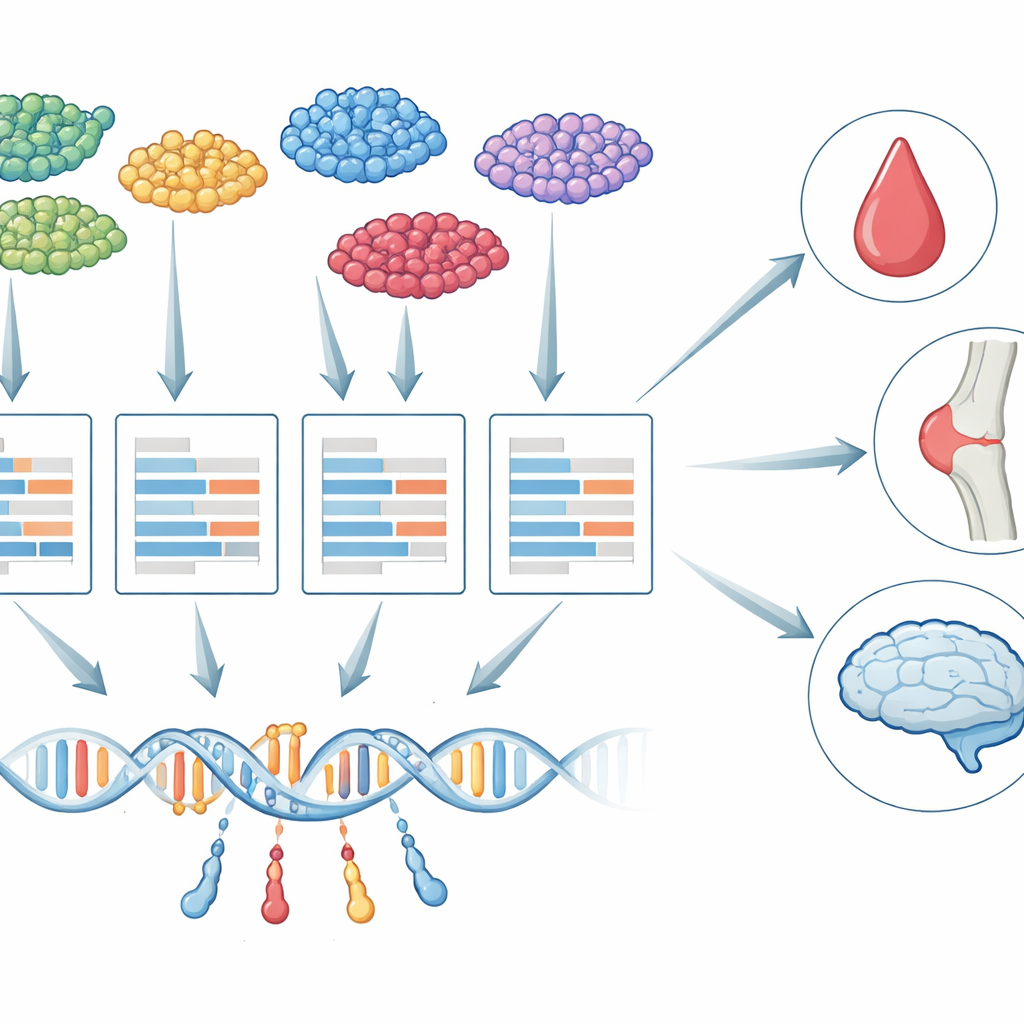
バルク組織から単一細胞へ
過去十年以上にわたり、研究者はトランスクリプトーム全域関連解析(TWAS)という手法を用いて遺伝変異と疾病を結びつけてきました。TWAS は二段階で動作します。まずDNA変化が遺伝子発現にどう影響するかを学習し、次に各遺伝子の遺伝的に予測された発現が血小板数や認知症リスクといった表現型に結びつくかを検定します。これまでほとんどのTWASは「バルク」組織サンプル、すなわち多数の細胞型のRNAが混ざり合った試料に依存してきました。その混合は重要な差異を隠します。たとえば脳のミクログリアにおけるある遺伝子の遺伝的制御はニューロンにおける同じ遺伝子と大きく異なり、ある疾病にとって本当に重要な細胞は限られているかもしれません。
ノイジーな単一細胞データの問題点
最近の集団規模の単一細胞RNAシーケンシングにより、各個人から数千の個々の細胞を測定できるようになりました。しかしこれらのデータは荒れており、カウントはまばらで(多くがゼロ)、実験の技術的要因に強く影響され、生物学的に同じであっても細胞ごとに大きくばらつきます。初期の試みでは、単一細胞データをTWASに流用する際にバルクRNAの正規化トリックを流用してノイズを抑えようとしましたが、著者らはそのような近道が遺伝的効果の実像を歪め、予測性能を低下させ、特に稀少または取り扱いの難しい細胞型で遺伝子—疾患の結びつきの発見を減らすことを示しています。
scTWAS が信号を浄化する方法
scTWAS は生物学的変動と測定誤差を明示的に分離することでこれらの課題に対処します。まず、各人ごと・細胞型ごとに単一細胞カウントを集約して「疑似バルク」プロファイルを作り、スパース性を低減しつつ細胞型の同一性を保ちます。次に二層の統計モデルを用います。第一層はDNA変異や年齢などの基本的な特徴が特定の細胞型における個人の真の基底的な遺伝子活性にどう影響するかを記述し、第二層はシーケンサーがその活性をどのようにノイジーなカウントに変換するか(シーケンス深度のばらつきの影響を含む)をモデル化します。このモデルを特殊な重み付き回帰アルゴリズムで適合させることで、scTWAS は最もノイジーなサンプルの影響を下げ、各遺伝子・各細胞型について遺伝的に制御される発現をより正確に推定します。
遺伝子が実際に働く場所を見つける
これらの細胞型特異的な予測モデルを学習した後、scTWAS はそれらを大規模なゲノムワイド関連解析に組み込み、遺伝子—形質の結びつきを検定します。実際の単一細胞実験を模したシミュレーションデータでは、scTWAS は既存手法を一貫して上回り、予測精度と検出力の双方で特に稀少な細胞型において大きな利得を示しました。本フレームワークを免疫細胞に適用すると、scTWAS は29の血液形質や関節リウマチ、ループス、喘息に関連する遺伝子を大幅に多く同定しました。これらのシグナルの多くは特定の単球やT細胞のサブセットなど、特定の免疫細胞型を主要な舞台として強調しており、一部の関連はバルク血液解析では完全に見落とされていました。
アルツハイマー病で脳の細胞亜型を覗く
scTWAS は脳領域でさらに示唆に富みます。数百の献体脳から得た単核(single-nucleus)データを用いて、著者らは6つの主要な脳細胞型と75のより細かな亜型について予測モデルを構築しました。これらをアルツハイマー病の遺伝データと組み合わせることで、リスク遺伝子が細胞レベルでどこで作用しているかをマップしました。ある遺伝子は多くの細胞型に広く現れ脳内で広範な役割を示唆する一方、他は非常に特異的です。例えば既知のリスク遺伝子 MS4A6A は脂質処理に関連する疾患関連ミクログリア亜型でのみ強い関連を示し、PPP1R37 は有名な APOE リスク領域近傍の炎症性ミクログリア亜型でのみ関連していました。これらのパターンは、特定のミクログリア状態がいくつかの遺伝的変異がアルツハイマー病リスクを駆動する主要な要因であることを示唆します。

将来の治療への示唆
専門外の読者にとっての主なメッセージは、遺伝子がどこで働くかがその遺伝子の機能と同じくらい重要であり得るという点です。TWAS を混合組織から正確な細胞型や亜型へと移し、単一細胞測定の癖を注意深くモデル化することで、scTWAS はこれまで見えなかった遺伝子—疾患の結びつきを明らかにします。このより鮮明な地図は、血液形成や免疫からアルツハイマー病における脳の免疫細胞に至るまで、新薬や介入のターゲットとすべき正確な細胞集団や経路に研究者が絞り込むのに役立ちます。
引用: Lin, Z., Su, C. scTWAS: a powerful statistical framework for single-cell transcriptome-wide association studies. Nat Commun 17, 3853 (2026). https://doi.org/10.1038/s41467-026-70374-7
キーワード: 単一細胞ゲノミクス, 遺伝的リスクマッピング, 免疫細胞, アルツハイマー病, 統計遺伝学