Clear Sky Science · pl
scTWAS: potężne ramy statystyczne dla badań skojarzeń transkryptomowych na poziomie pojedynczych komórek
Dlaczego badanie pojedynczych komórek może zmienić medycynę
Większość badań genetycznych chorób przypomina słuchanie tłumu: słychać ogólny ryk, ale przegapia się, co mówi każdy z osobna. Ten artykuł pokazuje, jak nastroić nasze ucho na poszczególne głosy. Autorzy wprowadzają scTWAS — nową metodę łączenia różnic w DNA z chorobami poprzez analizę aktywności genów w konkretnych typach komórek, a nawet w ich podtypach, wykorzystując dane z pojedynczych komórek (single-cell RNA sequencing). To ostrzejsze spojrzenie ujawnia, które dokładnie komórki — i które geny w ich obrębie — napędzają schorzenia takie jak zaburzenia krwi, choroby autoimmunologiczne czy choroba Alzheimera.
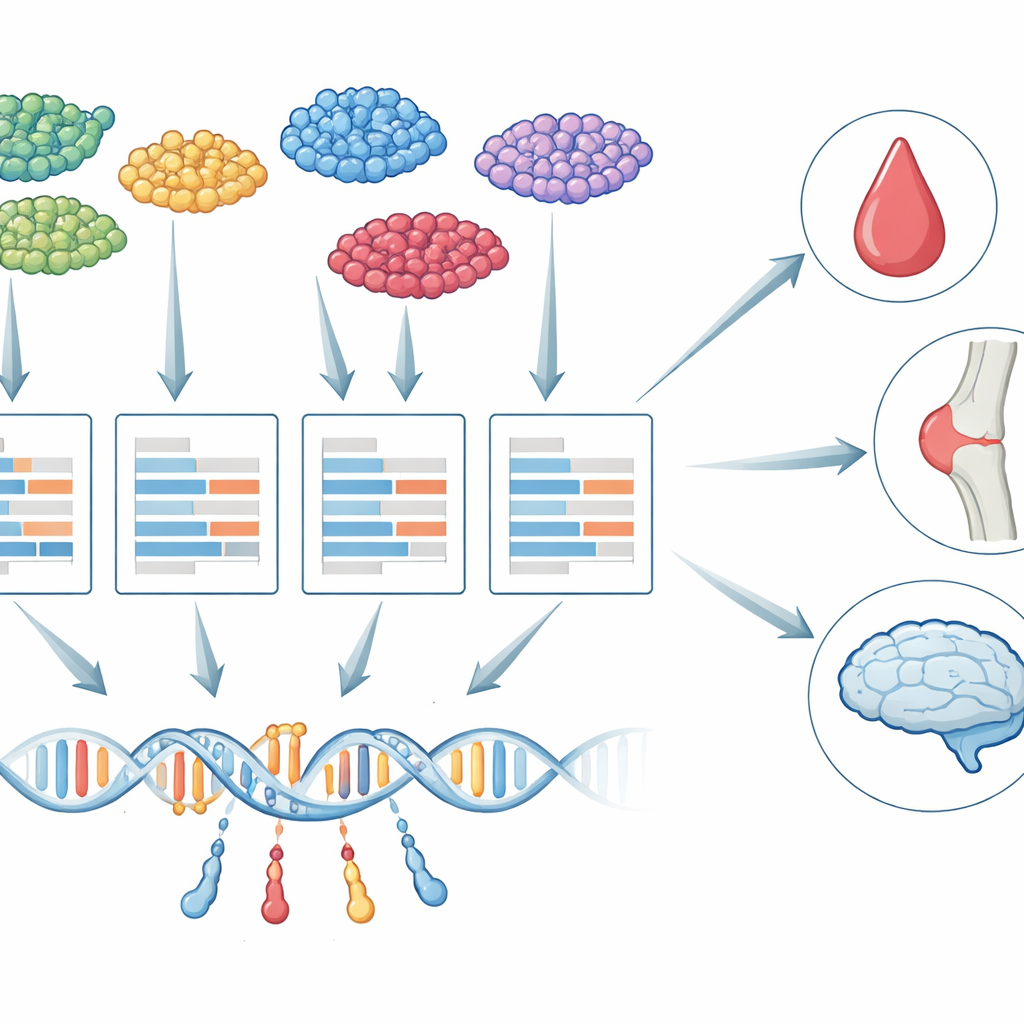
Od tkanek zbiorczych do pojedynczych komórek
Przez ponad dekadę badacze stosowali strategię zwaną badaniami skojarzeń transkryptomowych (TWAS), aby łączyć warianty genetyczne z chorobami. TWAS działa w dwóch krokach: najpierw uczy, jak zmiany w DNA wpływają na aktywność genów, następnie sprawdza, czy genetycznie przewidywana aktywność danego genu wiąże się z cechą taką jak liczba płytek krwi czy ryzyko demencji. Do tej pory niemal wszystkie prace TWAS opierały się na próbkach „zbiorczych” (bulk), gdzie RNA z wielu typów komórek jest zmieszane. To mieszanie ukrywa istotne różnice: kontrola genetyczna danego genu w mikrogleju mózgu może być bardzo odmienna od tej samej funkcji w neuronie, i tylko niektóre z tych komórek mogą rzeczywiście mieć znaczenie dla danej choroby.
Problem hałaśliwych danych z pojedynczych komórek
Nowa populacyjna skala sekwencjonowania RNA pojedynczych komórek umożliwia pomiar tysięcy pojedynczych komórek na osobę, w wielu osobach. Te dane są jednak zabałaganione: liczby odczytów są rzadkie (wiele zer), silnie wpływają na nie techniczne zawirowania eksperymentu i znacznie różnią się między komórkami, nawet gdy biologicznie są podobne. Wcześniejsze próby włączenia danych single-cell do TWAS używały doraźnych trików normalizacyjnych zapożyczonych z metod dla próbek zbiorczych, licząc, że oswoją one szum. Autorzy pokazują, że takie skróty mogą zniekształcać prawdziwe efekty genetyczne na aktywność genów, prowadząc do słabszych predykcji i mniejszej liczby wykrytych powiązań gen–choroba, szczególnie w rzadkich lub trudnych typach komórek.
Jak scTWAS oczyszcza sygnał
scTWAS stawia czoła tym wyzwaniom, wyraźnie oddzielając biologiczne sygnały od błędów pomiarowych. Najpierw agreguje odczyty z pojedynczych komórek w obrębie każdej osoby i typu komórek do profilu „pseudo-bulk”, zmniejszając rzadkość danych przy zachowaniu tożsamości typu komórki. Następnie wykorzystuje dwuwarstwowy model statystyczny: jedna warstwa opisuje, jak warianty DNA i podstawowe cechy, takie jak wiek, wpływają na prawdziwą, ukrytą aktywność genu danej osoby w określonym typie komórki; druga warstwa modeluje, jak maszyna sekwencjonująca przekształca tę aktywność w zaszumione odczyty, uwzględniając m.in. zmienną głębokość sekwencjonowania. Dopasowując ten model za pomocą wyspecjalizowanego algorytmu regresji ważonej, scTWAS obniża wagę najbardziej zaszumionych próbek i dokładniej estymuje genetycznie regulowaną ekspresję każdego genu w każdym typie komórki.
Odnajdywanie genów chorób tam, gdzie naprawdę działają
Gdy modele predykcyjne specyficzne dla typów komórek są wytrenowane, scTWAS włącza je do dużych badań asocjacyjnych (GWAS), aby testować powiązania gen–cecha. W symulowanych danych odwzorowujących rzeczywiste eksperymenty single-cell, scTWAS konsekwentnie przewyższał istniejące metody zarówno pod względem dokładności predykcji, jak i mocy statystycznej, z szczególnie dużymi zyskami w przypadku rzadkich typów komórek, gdzie dane są najuboższe. Zastosowanie ram do komórek układu odpornościowego pokazało, że scTWAS identyfikuje znacząco więcej genów związanych z 29 cechami krwi oraz z reumatoidalnym zapaleniem stawów, toczniem i astmą. Wiele z tych sygnałów wskazuje konkretne typy komórek odpornościowych — na przykład określone podzbiory monocytów lub limfocytów T — jako główną scenę, na której niektóre geny wpływają na ryzyko choroby; niektóre skojarzenia były całkowicie niewidoczne w analizach zbiorczych krwi.
Zajrzeć do podtypów komórek mózgu w chorobie Alzheimera
scTWAS staje się jeszcze bardziej odkrywcze w mózgu. Korzystając z danych z pojedynczych jąder komórkowych (single-nucleus) z setek darowanych ludzkich mózgów, autorzy zbudowali modele predykcyjne dla sześciu głównych typów komórek mózgowych i 75 drobniejszych podtypów. Połączyli je z danymi genetycznymi dotyczącymi choroby Alzheimera, aby zmapować, gdzie na poziomie komórkowym geny ryzyka najprawdopodobniej działają. Niektóre geny pojawiają się w wielu typach komórek, sugerując szerokie role w mózgu, podczas gdy inne są wyraźnie specyficzne. Na przykład znany gen ryzyka MS4A6A wykazuje silne skojarzenie tylko w podtypie mikrogleju związanym z metabolizmem lipidów, a PPP1R37 jest powiązany jedynie w zapalnym podtypie mikrogleju w pobliżu dobrze znanego regionu ryzyka APOE. Te wzorce wskazują, że odmienne stany mikrogleju są kluczowymi graczami w tym, jak niektóre warianty genetyczne zwiększają ryzyko Alzheimera.

Co to oznacza dla przyszłych terapii
Dla osoby niebędącej specjalistą główne przesłanie jest takie, że miejsce działania genu może być równie ważne jak jego funkcja. Przenosząc TWAS z „zblendowanych” tkanek do precyzyjnych typów i podtypów komórek oraz starannie modelując specyfikę pomiarów single-cell, scTWAS odkrywa powiązania gen–choroba, które wcześniej były niewidoczne. Ta ostrzejsza mapa pomaga badaczom skupić się na dokładnych populacjach komórek i szlakach, które powinny być celem nowych leków lub interwencji — od powstawania krwi i odporności po komórki odpornościowe mózgu w chorobie Alzheimera.
Cytowanie: Lin, Z., Su, C. scTWAS: a powerful statistical framework for single-cell transcriptome-wide association studies. Nat Commun 17, 3853 (2026). https://doi.org/10.1038/s41467-026-70374-7
Słowa kluczowe: genomika pojedynczych komórek, mapowanie ryzyka genetycznego, komórki układu odpornościowego, choroba Alzheimera, genetyka statystyczna