Clear Sky Science · pl
Badanie granic osadzeń wstępnie wytrenowanych modeli w komputerowym projektowaniu białek: studium przypadku przewidywania zdolności wektorów AAV
Dlaczego drobne zmiany w białkach wirusów mają znaczenie
Terapia genowa często opiera się na nieszkodliwych wirusach, takich jak wirus adeno-związany (AAV), które przenoszą terapeutyczne geny do naszych komórek. Uczynienie tych „pojazdów dostawczych” bezpieczniejszymi i bardziej skutecznymi zwykle wymaga zmiany zaledwie kilku cegiełek w bardzo długiej osłonie białkowej. W tym badaniu postawiono pozornie proste pytanie: gdy ważne zmiany są tak drobne i lokalne, czy dzisiejsze potężne narzędzia sztucznej inteligencji potrafią je dostrzec na tyle dobrze, by wspierać lepsze projekty?
Jak komputery czytają „zdania” białkowe
Nowoczesne projektowanie białek często wykorzystuje głębokie modele uczące, które traktują sekwencje aminokwasów nieco jak zdania w języku. Narzędzia takie jak ProtBERT i ESM2 uczą się zamieniać każde białko w pakiet liczb, zwany osadzeniem (embeddingiem), który podsumowuje wzorce obserwowane w milionach naturalnych białek. Te wstępnie wytrenowane osadzenia są atrakcyjne, ponieważ uchwycają bogate informacje o strukturze i funkcji bez potrzeby przeprowadzania nowych eksperymentów. Jednak w przeważającej mierze zostały zbudowane do rozumienia całych białek, a nie rzadkich, lecz kluczowych mutacji, które inżynierowie biologiczni wprowadzają w niewielkim fragmencie.
Testowanie AI na rzeczywistym narzędziu terapii genowej
Autorzy użyli AAV2, szeroko badanej odmiany wektora terapii genowej, jako rygorystycznego przypadku testowego. Zewnętrzna powłoka AAV2, czyli kapsyd, to długie białko złożone z 735 aminokwasów, podczas gdy inżynierowie zwykle zmieniają tylko krótki fragment liczący około 20 do 50 pozycji, by zmodyfikować zachowanie wirusa w organizmie. Zespół przeanalizował ponad 293 000 eksperymentalnie zmierzonych wariantów, których mutacje ograniczały się do okna długości 28 aminokwasów. Każdy wariant został oznaczony jako wytwarzający zdolne do zakażenia cząstki wirusa lub jako niezdolny. Ten duży, starannie opisany zbiór danych pozwolił badaczom sprawdzić, jak różne sposoby kodowania sekwencji — tradycyjne kodowania one-hot i kilka odmian osadzeń ProtBERT i ESM2 — sprawdzają się, gdy sygnał biologiczny pochodzi z bardzo małego regionu.
Co surowe osadzenia przeoczają, a gdzie wciąż pomagają
Pierwsze analizy w badaniu dotyczyły podejść niesuperwizowanych, w których algorytmy grupują sekwencje według podobieństwa, nie dysponując informacją o tym, które działają. Tutaj ogólne osadzenia na poziomie sekwencji z modeli językowych dawały sensowne grupowania zgodne ze sposobem projektowania sekwencji, ale nie rozdzielały wyraźnie wariantów zdolnych od niezdolnych. Tradycyjne kodowania one-hot częściej grupowały białka według długości, cechy, która okazała się tylko słabo powiązana ze zdolnością do wytwarzania funkcjonalnych cząstek. Gdy badacze przeszli do zadań nadzorowanych — jawnego trenowania modeli do przewidywania zdolności — okazało się, że osadzenia na poziomie poszczególnych aminokwasów, które uśredniają informacje po wszystkich resztach, zazwyczaj przewyższały ogólne osadzenia sekwencji. Co zaskakujące, skompresowana wersja prostego kodowania one-hot nieco wyprzedziła wstępnie wytrenowane osadzenia pod względem ogólnej dokładności, zwłaszcza w połączeniu z sieciami neuronowymi.
Dlaczego wzorce mutacji trudno dostrzec
Aby zrozumieć te mieszane wyniki, autorzy zbadali, które warianty były zgodnie klasyfikowane przez wszystkie modele, a które je myliły. Sekwencje łatwe do sklasyfikowania niemal zawsze były zdolne i wykazywały wyraźną strefę „zakazu”: udane warianty zwykle unikały mutacji w zakopanym segmencie strukturalnym między określonymi pozycjami lub ograniczały je do subtelnych podstawień. Trudne przypadki natomiast wyglądały powierzchownie podobnie pod względem rozmieszczenia i liczby mutacji, ale okazywały się niezdolne. Zespół zbudował następnie syntetyczne przykłady, w których rozproszył lub skoncentrował mutacje wzdłuż całego białka. Stwierdzono, że standardowe osadzenia zaczynały wyraźnie rozdzielać grupy dopiero wtedy, gdy zmieniono setki pozycji — znacznie więcej niż praktyczne lub typowe w rzeczywistych kampaniach inżynieryjnych. Wskazuje to, że ogólnego przeznaczenia osadzenia białkowe są stosunkowo mało wrażliwe na rzadkie lub silnie lokalizowane mutacje, które często decydują o powodzeniu projektowanych białek.
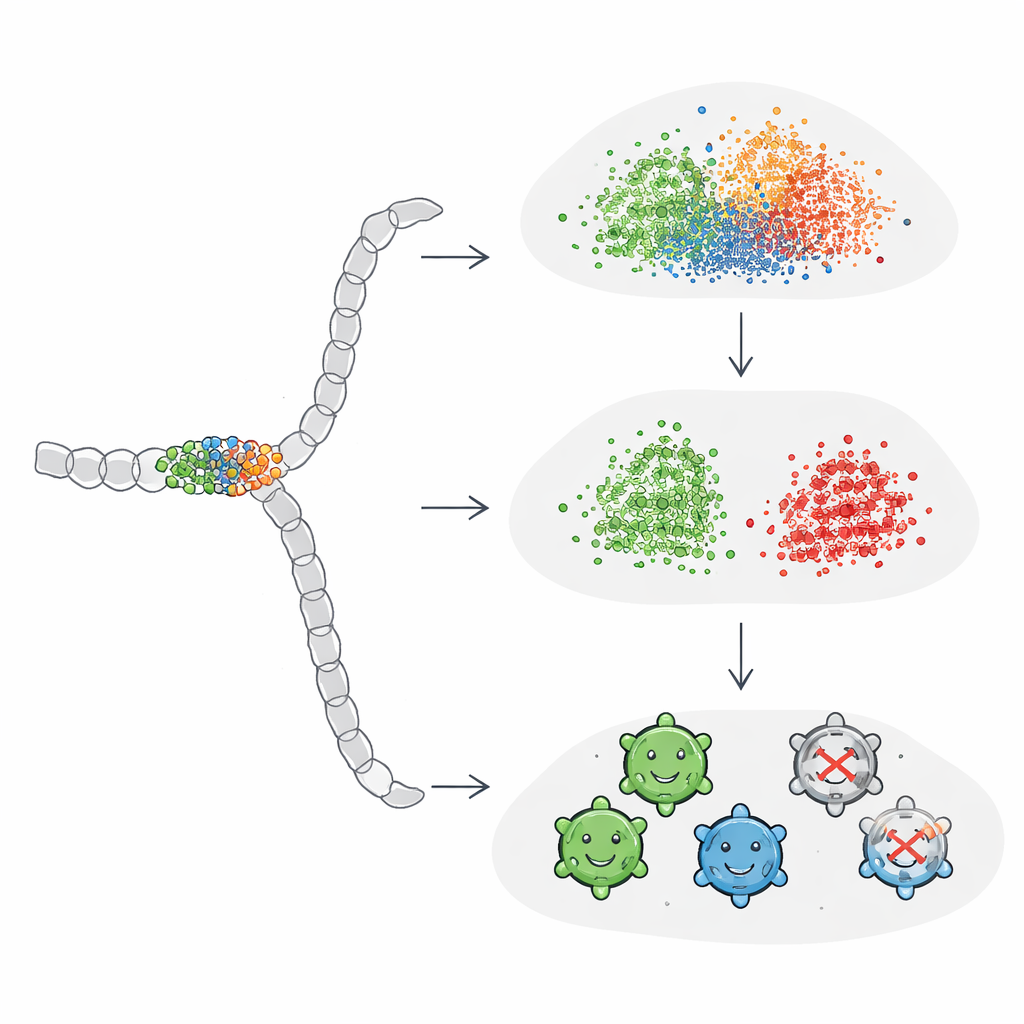
Strojenie AI, by skupiała się na tym, co ważne
Następnie badacze sprawdzili, czy mogą „nauczyć” ProtBERT i ESM2, by przywiązywały większą wagę do małego okna mutacyjnego, dostrajając modele bezpośrednio przy użyciu etykiet dotyczących zdolności AAV. Do każdego modelu dołączyli prostą warstwę klasyfikacyjną i trenowali cały system end-to-end. Po dostrojeniu wydajność poprawiła się do poziomu równego lub przekraczającego najlepsze modele oparte na one-hot, a powstałe osadzenia w wizualizacjach wreszcie wykazywały wyraźne rozdzielenie sekwencji zdolnych od niezdolnych. Co ciekawe, najbardziej skorzystały ogólne osadzenia sekwencji: kierowane informacją specyficzną dla zadania, nauczyły się wzmacniać wpływ kluczowych pozycji zamiast pozwalać, by tonęły w pozostałej części sekwencji.
Co to znaczy dla przyszłego projektowania białek
Dla czytelników zainteresowanych tym, jak AI ukształtuje kolejne generacje terapii genowych i enzymów, przesłanie jest zniuansowane, ale optymistyczne. Gotowe modele języka białkowego, choć potężne, mogą przeoczyć drobne zmiany, które często decydują, czy zaprojektowane białko działa. Proste kodowania i redukcja wymiarów wciąż mają swoje miejsce w takich zadaniach. Jednak przez dostrajanie tych modeli na wysokiej jakości danych eksperymentalnych — nawet gdy mutacji jest niewiele i są ściśle skupione — badacze mogą przeorientować je na fragmenty sekwencji, które mają największe znaczenie. W praktyce praca ta sugeruje, że łączenie dużych wstępnie wytrenowanych modeli z retreningiem specyficznym dla zadania oferuje solidną ścieżkę do bardziej niezawodnego, komputerowo wspomaganego projektowania wektorów wirusowych i innych projektowanych białek.
Cytowanie: Rodrigues, A.F., Ferraz, L., Balbi, L. et al. Exploring the limits of pre-trained embeddings in machine-guided protein design: a case study on predicting AAV vector viability. Sci Rep 16, 10974 (2026). https://doi.org/10.1038/s41598-026-45458-5
Słowa kluczowe: modele języka białkowego, projektowanie kapsydów AAV, wektory terapii genowej, osadzenia białkowe, komputerowo wspomagane projektowanie białek