Clear Sky Science · ar
استكشاف حدود التمثيلات المسبقة التدريب في تصميم البروتين بتوجيه آلي: دراسة حالة حول التنبؤ بصلاحية ناقلات AAV
لماذا تغييرات طفيفة في بروتينات الفيروسات مهمة
غالبًا ما يعتمد العلاج الجيني على فيروسات غير ضارة، مثل الفيروس المرتبط بالأدينو (AAV)، لنقل الجينات العلاجية إلى خلايانا. عادة ما يتطلب جعل هذه "مركبات التوصيل" الفيروسية أكثر أمانًا وفعالية تعديل عدد قليل من الوحدات البنائية في غلاف بروتيني طويل جدًا. تطرح هذه الدراسة سؤالًا يبدو بسيطًا: عندما تكون التغييرات المهمة صغيرة ومحلية جدًا، هل يمكن لأدوات الذكاء الاصطناعي القوية الحالية رؤيتها بدقة كافية لتوجيه تصميمات أفضل؟
كيف تقرأ الحواسيب "جمل" البروتين
يستخدم تصميم البروتين الحديث غالبًا نماذج تعلم عميق تعامل سلاسل الأحماض الأمينية قليلاً كما تعامل الجمل في اللغة. تتعلم أدوات مثل ProtBERT وESM2 تحويل كل بروتين إلى حزمة أرقام، تُدعى تمثيلاً (embedding)، تلخص الأنماط التي رأتْها عبر ملايين البروتينات الطبيعية. تحظى هذه التمثيلات المسبقة التدريب بجاذبية لأنها تلتقط معلومات غنية عن البنية والوظيفة دون الحاجة إلى تجارب جديدة. لكنها بُنيت أساسًا لفهم البروتينات بأكملها، وليس الطفرات النادرة ولكن الحاسمة التي يُدخلها المهندسون الحيويون في رقعة صغيرة فقط.
اختبار الذكاء الاصطناعي على عامل شائع في العلاج الجيني
استخدم المؤلفون AAV2، ناقلًا واسع الدراسة في العلاج الجيني، كحالة اختبار صارمة. غلاف AAV2 الخارجي، أو الكابسيد، هو بروتين طويل مكون من 735 حمضًا أمينيًا، ومع ذلك عادة ما يغيّر المهندسون جزءًا قصيرًا يتراوح بين 20 و50 موقعًا لتعديل سلوك الفيروس في الجسم. حلّل الفريق أكثر من 293000 متغير مُقاس تجريبيًا، حيث اقتصرّت الطفرات على نافذة طولها 28 حمضًا أمينيًا. وُسْمَ كل متغير إما على أنه ينتج جُسيمات فيروسية قابلة للحياة أو يفشل في ذلك. أتاح هذا المجموع الكبير والموسوم بعناية للباحثين فحص كيف تعمل طرق ترميز السلاسل المختلفة—الترميزات التقليدية ذات الشكل الواحد (one-hot) وعدة نكهات من تمثيلات ProtBERT وESM2—عندما تأتي الإشارة البيولوجية من منطقة صغيرة جدًا.
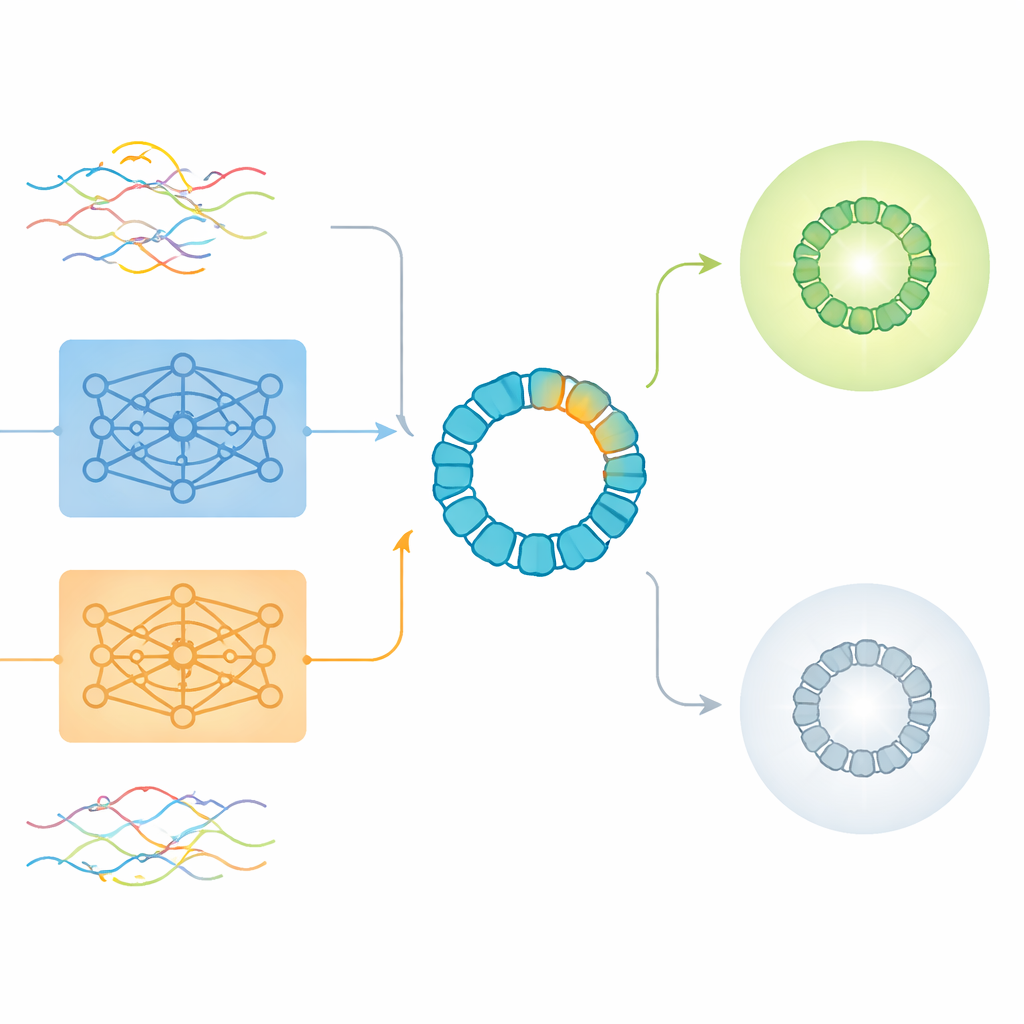
ما الذي تغفلُه التمثيلات الخام وأين لا تزال مفيدة
نظرت الدراسة أولاً إلى تحليلات غير مراقبة، حيث تقوم الخوارزميات ببساطة بتجميع السلاسل حسب التشابه دون أن تُخبر أي منها فعّالة. هنا، أنتجت التمثيلات العالمية على مستوى السلسلة من نماذج اللغة تجميعات معقولة وفقًا لكيفية تصميم السلاسل، لكنها لم تفصل بوضوح بين المتغيرات القابلة للحياة وتلك غير القابلة. بينما ميّزت الترميزات التقليدية بنمط one-hot البروتينات بحسب الطول، وهي خاصية تبين أنها مرتبطة بصلاحية الفيروس بشكل ضعيف فقط. عندما اتجه الباحثون إلى مهام مراقبة—تدريب نماذج صراحةً للتنبؤ بالصلاحية—وجدوا أن التمثيلات على مستوى الحمض الأميني، التي تجمع معلومات عبر كل البقايا، تفوقت عمومًا على التمثيلات العالمية للسلسلة. ومن المدهش أن نسخة مضغوطة من ترميز one-hot البسيط تفوقت قليلًا على التمثيلات المسبقة التدريب في الدقة الإجمالية، خاصة عند استخدامها مع الشبكات العصبية.
لماذا أنماط الطفرات صعبة الاكتشاف
لفهم هذه النتائج المتباينة، فحص المؤلفون المتغيرات التي اتّفقت عليها كل النماذج والتي أربكتها باستمرار. كانت السلاسل السهلة التصنيف شبه دائمًا قابلة للحياة وأظهرت "منطقة عدم دخول" واضحة: تميل المتغيرات الناجحة إلى تجنب الطفرات في جزء هيكلي مدفون بين مواقع محددة، أو تقتصر على بدائل طفيفة. في المقابل، بدت الحالات الصعبة متشابهة سطحيًا في مواضع وعدد الطفرات لكنها كانت غير قابلة للحياة. ثم أنشأ الفريق أمثلة تركيبية نشروا أو ركزوا فيها الطفرات على طول البروتين كله. وجدوا أن التمثيلات القياسية لم تبدأ في فصل المجموعات بوضوح إلا عندما تم تغيير مئات المواقع—وهو أكثر بكثير مما هو عملي أو نموذجي في حملات الهندسة الحيوية الواقعية. يشير هذا إلى أن تمثيلات البروتين العامة الحسنة ليست حساسة بما فيه الكفاية للطفرات النادرة أو المحلية بشدة التي غالبًا ما تصنع أو تفشل البروتينات المهندَسة.
تعديل الذكاء الاصطناعي للتركيز على المهم
استكشف الباحثون بعد ذلك ما إذا كان بإمكانهم "تعليم" ProtBERT وESM2 إيلاء اهتمام أقرب لنافذة الطفرات الصغيرة عن طريق تحسين النماذج مباشرة على تسميات صلاحية AAV. أضافوا طبقة تصنيف بسيطة إلى كل نموذج ودربوا النظام بأكمله من الطرف إلى الطرف. بعد التحسين، تحسّن الأداء ليضاهي أو يتجاوز أفضل النماذج المبنية على one-hot، وأظهرت التمثيلات الناتجة أخيرًا فصلًا واضحًا بين السلاسل القابلة وغير القابلة للحياة في رسوم التصور. ومن المثير للاهتمام أن التمثيلات العالمية للسلسلة استفادت أكثر من هذه العملية: فعند توجيهها بتغذية راجعة مخصصة للمهمة، تعلمت تضخيم تأثير المواضع الحاسمة بدل أن تُطغى من قِبل بقية السلسلة.
ما الذي يعنيه هذا لمستقبل تصميم البروتين
للقراء المهتمين بكيف سيشكل الذكاء الاصطناعي الجيل القادم من علاجات الجينات والإنزيمات، الرسالة متباينة لكنها متفائلة. نماذج لغة البروتين الجاهزة للاستخدام، مهما كانت قوية، يمكن أن تغفل التغييرات الدقيقة التي غالبًا ما تحدد ما إذا كان البروتين المصمم يعمل. لا تزال الترميزات البسيطة وتقليل الأبعاد فعّالة في مثل هذه الحالات. ومع ذلك، من خلال تحسين هذه النماذج على بيانات تجريبية عالية الجودة—حتى عندما تكون الطفرات قليلة ومتماسكة—يمكن للباحثين إعادة توجيهها نحو أجزاء السلسلة الأكثر أهمية. عمليًا، تشير هذه الدراسة إلى أن الجمع بين نماذج ضخمة مدربة مسبقًا وإعادة تدريب مخصصة للمهمة يوفر مسارًا قويًا نحو تصميم أكثر موثوقية بتوجيه الآلة لناقلات الفيروسات وبروتينات مهندَسة أخرى.
الاستشهاد: Rodrigues, A.F., Ferraz, L., Balbi, L. et al. Exploring the limits of pre-trained embeddings in machine-guided protein design: a case study on predicting AAV vector viability. Sci Rep 16, 10974 (2026). https://doi.org/10.1038/s41598-026-45458-5
الكلمات المفتاحية: نماذج لغة البروتين, تصميم غلاف AAV, نواقل العلاج الجيني, تمثيلات البروتين العددية, هندسة البروتين بتوجيه الآلة