Clear Sky Science · he
חקר מגבלות ההטמעות המאומנות מראש בעיצוב חלבונים במחשב: מקרה מבחן בחיזוי תפקודיות וקטורי AAV
למה שינויים זעירים בחלבוני וירוס חשובים
תרפיית גנים נשענת לעתים קרובות על וירוסים בלתי מזיקים, כמו וירוס אסוציאציית אדנו (AAV), כדי לשנע גנים טיפוליים אל תוך התאים שלנו. הפיכת אותם "כלי משלוח" ויראליים לבטוחים ויעילים יותר בדרך כלל דורשת כיוונון של רק כמה אבני בניין במעטפת חלבונית ארוכה מאוד. המחקר הזה שואל שאלה שנראית פשוטה: כשהשינויים החשובים הם כל כך זעירים ומקומיים, האם כלי הבינה המלאכותית החזקים של ימינו באמת מסוגלים לזהות אותם היטב מספיק כדי להנחות עיצובים טובים יותר?
איך מחשבים "קוראים" משפטים חלבוניים
עיצוב חלבונים מודרני משתמש לעיתים קרובות במודלים של למידה עמוקה שמתייחסים לרצפי חומצות אמינו קצת כמו למשפטים בשפה. כלים כגון ProtBERT ו-ESM2 לומדים להמיר כל חלבון לחבילה של מספרים, שנקראת הטמעה (embedding), המסכמת דפוסים שראו על פני מיליוני חלבונים טבעיים. ההטמעות המאומנות מראש מושכות כי הן מקיפות מידע עשיר על מבנה ותפקוד ללא צורך בניסויים חדשים. עם זאת, הן נבנו בעיקר כדי להבין חלבונים בשלמותם, לא את המוטציות הנדירות אך הקריטיות שמכניסים מהנדסי הביו רק באזור קטן.
בדיקת הבינה המלאכותית על כלי עבודה אמיתי של תרפיית גנים
המחברים השתמשו ב-AAV2, וקטור תרפיה שנחקר נרחב, כמקרה מבחן קפדני. מעטפת החיצונית של AAV2, או הקפסיד, היא חלבון ארוך של 735 חומצות אמינו, אך מהנדסים בדרך כלל משנים רק מקטע קצר של כ-20 עד 50 עמדות כדי לשנות את התנהגות הוירוס בגוף. הצוות ניתח יותר מ-293,000 וריאנטים שנמדדו ניסויית, שבהם המוטציות הוגבלו לחלון של 28 חומצות אמינו. לכל וריאנט תוייג האם הוא מייצר חלקיקי וירוס ברי-קיום או נכשל בכך. מערך נתונים גדול ומסומן זה אפשר לחוקרים לבחון כיצד דרכי קידוד שונות של רצפים — קידוד one-hot מסורתי וכמה וריאנטים של הטמעות ProtBERT ו-ESM2 — מתפקדות כאשר האות הביולוגי מגיע מאזור מאוד קטן.
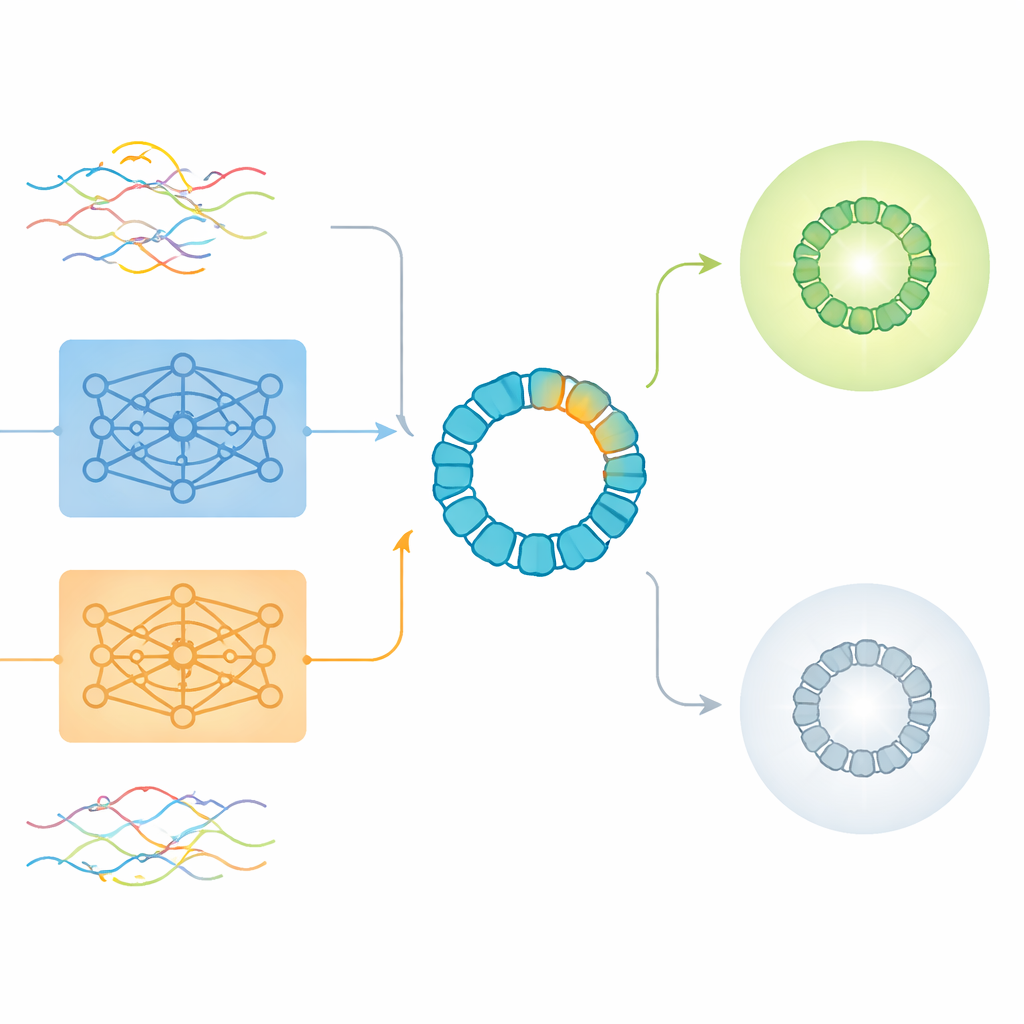
מה שההטמעות הגולמיות מפספסות ואיפה הן עדיין עוזרות
המחקר תחילה בחן ניתוחים לא מפוקחים, שבהם האלגוריתמים פשוט מקבצים רצפים לפי דמיון מבלי לקבל מידע על אילו מהם עובדים. כאן, הטמעות גלובליות ברמת הרצף מהמודלים הלשוניים יצרו קיבוצי־תקינות סבירים לפי אופן העיצוב של הרצפים, אך הן לא הפרידו בצורה ברורה בין וריאנטים ברי-קיום ללא-ברי-קיום. קידודי one-hot המסורתיים נטו במקום זאת לקבץ חלבונים לפי אורך, תכונה שהתבררה כקשורה רק באופן חלש לתפקוד. כשהחוקרים פנו למשימות מפוקחות — אימון מודלים במפורש לחיזוי תפקודיות — הם מצאו שהטמעות ברמת חומצת האמינו, שממוצעות על פני כל שאריות החומצות, בדרך כלל עלו על הטמעות גלובליות של רצף. במפתיע, עם זאת, גרסה מדחוסה של קידוד one-hot פשוט קטנה היטב עקפה במעט את ההטמעות המאומנות מראש בדיוק הכללי, במיוחד כאשר שולבה עם רשתות נוירונים.
למה דפוסי המוטציה קשים לזיהוי
כדי להבין תוצאות מעורבות אלו, המחברים בחנו אילו וריאנטים כל המודלים הסכימו לגביהם ואילו בלבלו בעקביות. רצפים שקל לסווג היו כמעט תמיד ברי-קיום והראו אזור "אסור" ברור: וריאנטים מוצלחים נטו להימנע ממוטציות בחלק מבני שקוע בין מיקומים מסוימים, או להגביל אותן להחלפות עדינות. לעומת זאת, מקרים קשים נראו מבחוץ דומים במיקום ומספר המוטציות שלהם אך נמצאו כלא ברי-קיום. הצוות בנה דוגמאות סינתטיות שבהן פרסו או ריכזו מוטציות לאורך כל החלבון. הם מצאו שהטמעות סטנדרטיות התחילו להפריד קבוצות בצורה נקייה רק כאשר שונו מאות עמדות — הרבה יותר ממה שמעשי או טיפוסי בקמפיינים של הנדסה ביולוגית. זה מעיד שההטמעות הכלליות רגישות פחות לשינויים דלילים או ממוקדים מאוד שעשויים לקבוע בפועל את גורל החלבון המהונדס.
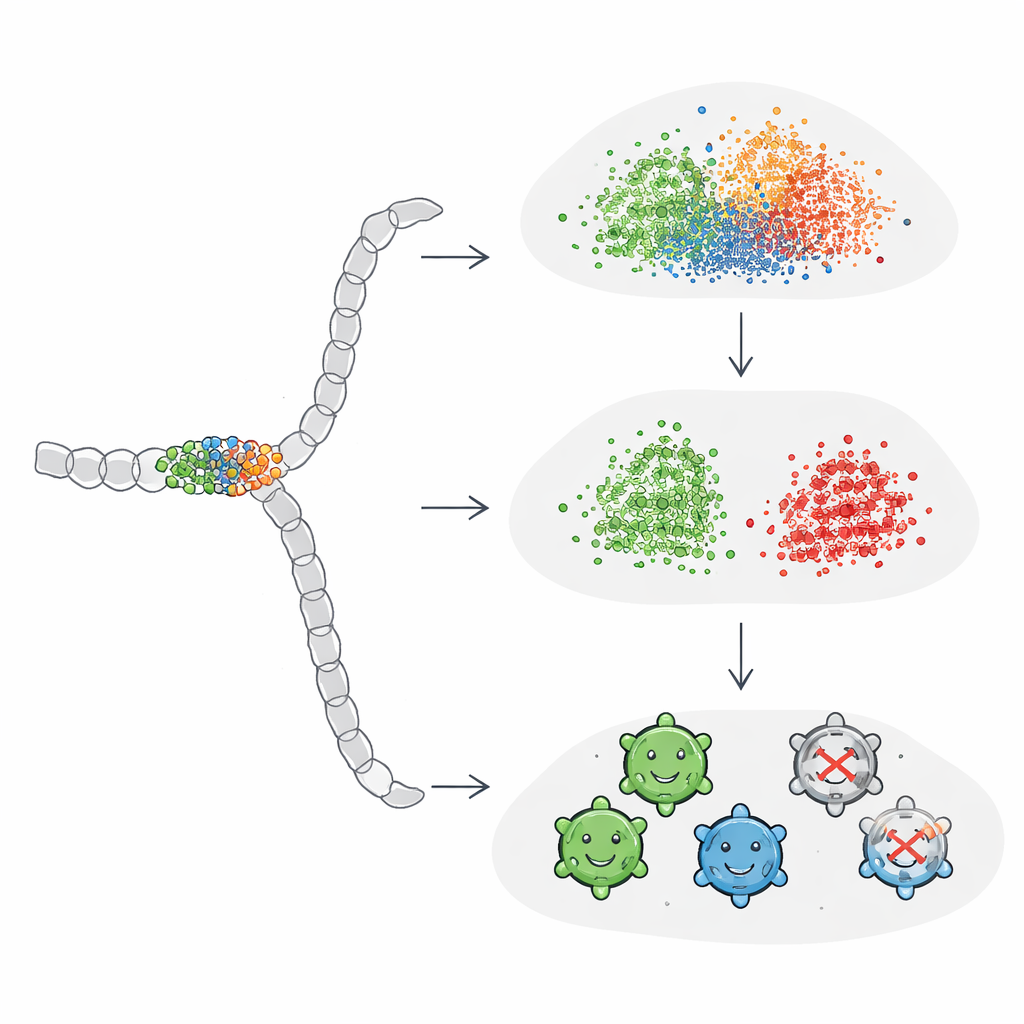
כוונון הבינה המלאכותית להתמקד במה שחשוב
החוקרים אחר כך חקרו האם אפשר "ללמד" את ProtBERT ו-ESM2 לשים לב טוב יותר לחלון המוטציות הקטן על ידי כוונון עדין (fine-tuning) של המודלים ישירות על תוויות התפקודיות של AAV. הם הוסיפו לכל מודל שכבת סיווג פשוטה ואימנו את המערכת כולה מקצה לקצה. לאחר הכוונון, הביצועים השתפרו כדי להתאים או לעלות על מיטב הדגמים המבוססים על one-hot, וההטמעות שהתוצאה הראתה סוף-סוף הפרדה ברורה בין רצפים ברי-קיום ללא-ברי-קיום בגרפים חזותיים. מעניין כי ההטמעות הגלובליות של רצף הרוויחו הכי הרבה מתהליך זה: לאחר שקיבלו משוב ספציפי למשימה, הן למדו להגביר את השפעת המיקומים הקריטיים במקום לתת להם לטבוע ברעש של שאר הרצף.
מה משמעות זה לעיצוב חלבונים בעתיד
לקרוא המעוניינים בדרך שבה בינה מלאכותית תעצב את דור הבא של תרפיות גנים ואנזימים, המסר מעודן אך אופטימי. מודלים לשפת חלבונים כך שהם יוצאים מהקופסה, חזקים ככל שיהיו, עלולים לפספס את השינויים העדינים שמקבעים לעתים קרובות אם חלבון מתפקד. קידודים פשוטים והקטנת ממדיות עדיין מחזיקים מעמד בהקשרים כאלה. עם זאת, על ידי כוונון עדין של מודלים גדולים על נתונים ניסיוניים איכותיים — גם כאשר המוטציות מעטות ומצומצמות — חוקרים יכולים למקד אותם מחדש על החלקים של הרצף שחשובים ביותר. במונחים פרקטיים, עבודה זו מציעה ששילוב של מודלים גדולים מאומנים מראש עם אימון חוזר ספציפי למשימה מספק מסלול יציב לעיצוב מונחה־מחשב מהימן יותר של וקטורי וירוס וחלבונים מהונדסים אחרים.
ציטוט: Rodrigues, A.F., Ferraz, L., Balbi, L. et al. Exploring the limits of pre-trained embeddings in machine-guided protein design: a case study on predicting AAV vector viability. Sci Rep 16, 10974 (2026). https://doi.org/10.1038/s41598-026-45458-5
מילות מפתח: מודלים לשפת חלבונים, עיצוב קופסית AAV, וקטורי גן תרפיה, הטמעות חלבוניים, הנדסת חלבונים מונחית מחשב