Clear Sky Science · nl
De grenzen van voorgetrainde embeddings in machine-gestuurd proteïneontwerp verkennen: een casestudy over het voorspellen van AAV-vectorlevensvatbaarheid
Waarom kleine veranderingen in virale eiwitten ertoe doen
Gentherapie maakt vaak gebruik van onschadelijke virussen, zoals adeno-geassocieerde virus (AAV), om therapeutische genen in onze cellen te brengen. Het veiliger en effectiever maken van deze virale “bezorgvoertuigen” vereist meestal het aanpassen van slechts een paar bouwstenen in een zeer lange eiwitmantel. Deze studie stelt een schijnbaar eenvoudige vraag: wanneer de belangrijke veranderingen zo klein en lokaal zijn, kunnen de krachtige AI-tools van vandaag ze dan daadwerkelijk goed genoeg waarnemen om beter ontwerp te sturen?
Hoe computers eiwit-"zinnen" lezen
Modern eiwitontwerp maakt vaak gebruik van deep learning-modellen die aminozuursequenties een beetje behandelen als zinnen in een taal. Hulpmiddelen zoals ProtBERT en ESM2 leren elk eiwit om te zetten in een bundel getallen, een embedding, die patronen samenvat die ze hebben gezien in miljoenen natuurlijke eiwitten. Deze voorgetrainde embeddings zijn aantrekkelijk omdat ze rijke informatie over structuur en functie vastleggen zonder nieuwe experimenten te vereisen. Maar ze zijn grotendeels gebouwd om hele eiwitten te begrijpen, niet de zeldzame maar cruciale mutaties die bio-ingenieurs in slechts een klein stukje aanbrengen.
AI testen op een echte werkpaard voor gentherapie
De auteurs gebruikten AAV2, een veel bestudeerde vector voor gentherapie, als een strenge casus. De buitenste schaal van AAV2, of capsid, is een lang eiwit van 735 aminozuren, maar ingenieurs wijzigen meestal slechts een korte stretch van ongeveer 20 tot 50 posities om het gedrag van het virus in het lichaam te veranderen. Het team analyseerde meer dan 293.000 experimenteel gemeten varianten waarvan de mutaties waren beperkt tot een venster van 28 aminozuren. Elke variant werd geclassificeerd als óf het produceren van levensvatbare virusdeeltjes óf het falen daarin. Deze grote, zorgvuldig geannoteerde dataset stelde de onderzoekers in staat te onderzoeken hoe verschillende manieren om sequenties te coderen—traditionele one-hot-encoderingen en meerdere varianten van ProtBERT- en ESM2-embeddings—presteerden wanneer het biologische signaal uit een zeer klein gebied kwam.
Wat ruwe embeddings missen en waar ze nog steeds helpen
De studie keek eerst naar onbewaakte analyses, waarbij algoritmen sequenties simpelweg groeperen op overeenkomsten zonder te weten welke werken. Hier produceerden globale sequentie-embeddings van de taalmodellen redelijke groeperingen op basis van hoe de sequenties waren ontworpen, maar ze scheidden levensvatbare van niet-levensvatbare varianten niet duidelijk. Traditionele one-hot-encoderingen groeperen eiwitten eerder op lengte, een eigenschap die uiteindelijk slechts zwak gerelateerd bleek aan levensvatbaarheid. Toen de onderzoekers overstapten naar bewaakte taken—expliciet modellen trainen om levensvatbaarheid te voorspellen—vonden ze dat aminozuurniveau-embeddings, die informatie over alle residuen gemiddeld weergeven, over het algemeen beter presteerden dan globale sequentie-embeddings. Verrassend genoeg overtrof in algemene nauwkeurigheid een gecomprimeerde versie van eenvoudige one-hot-encodering de voorgetrainde embeddings lichtjes, vooral wanneer gebruikt met neurale netwerken.
Waarom mutatiepatronen moeilijk te zien zijn
Om deze gemengde resultaten te begrijpen, onderzochten de auteurs welke varianten alle modellen eensgezind classificeerden en welke hen consequent in de war brachten. Gemakkelijk te classificeren sequenties waren bijna altijd levensvatbaar en toonden een duidelijk "no-go"-gebied: succesvolle varianten vermeden doorgaans mutaties in een begraven structureel segment tussen bepaalde posities, of beperkten zich tot subtiele substituties. Moeilijke gevallen daarentegen leken oppervlakkig vergelijkbaar qua locatie en aantal mutaties, maar bleken niet-levensvatbaar. Het team bouwde vervolgens synthetische voorbeelden waarbij ze mutaties verspreidden of concentreerden over het gehele eiwit. Ze ontdekten dat standaardembeddings pas groepen duidelijk begonnen te scheiden wanneer honderden posities werden gewijzigd—veel meer dan praktisch of typisch is in echte bio-engineeringcampagnes. Dit duidt erop dat generalistische eiwit-embeddings relatief ongevoelig zijn voor de spaarzame of sterk gelokaliseerde mutaties die vaak het verschil maken bij ontworpen eiwitten.
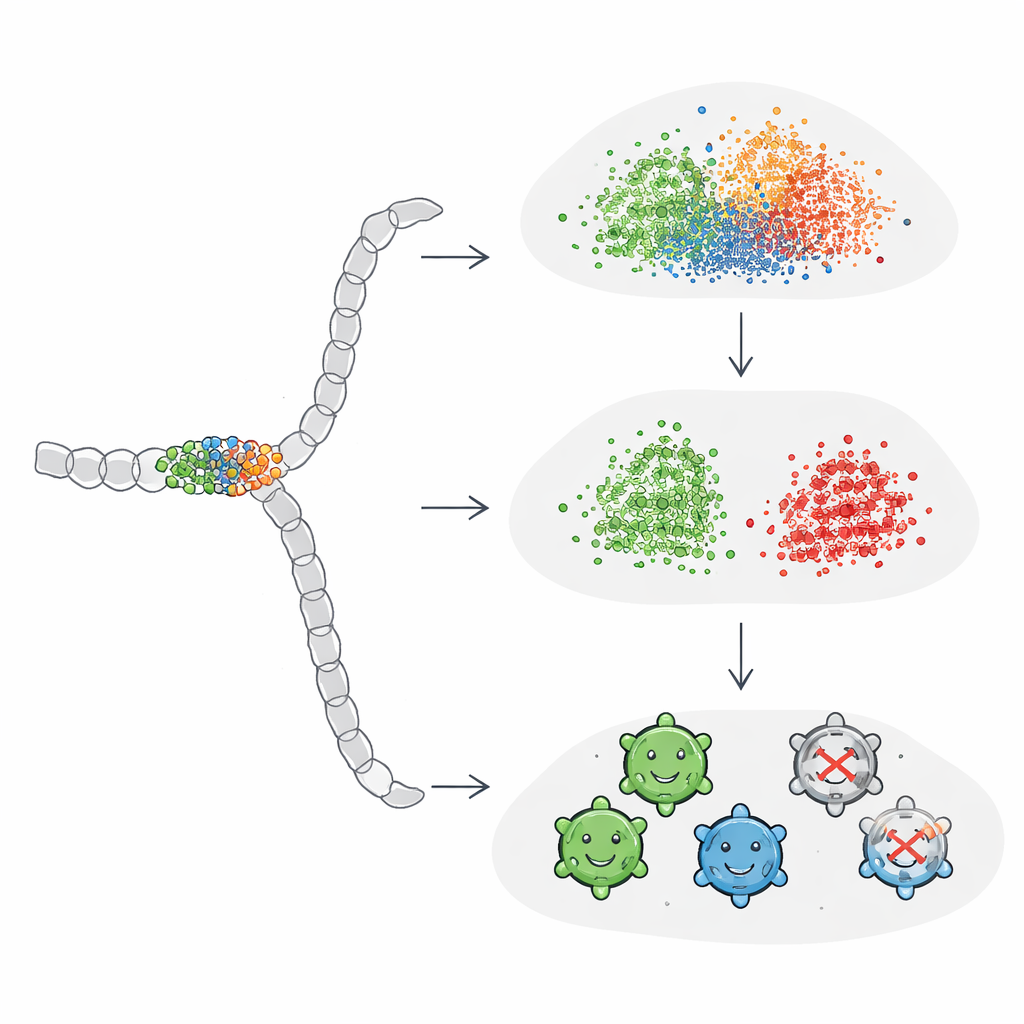
AI afstemmen om op het juiste te focussen
De onderzoekers onderzochten vervolgens of ze ProtBERT en ESM2 konden "leren" om meer aandacht te besteden aan het kleine mutatievenster door de modellen direct bij te stellen op de AAV-levensvatbaarheidslabels. Ze voegden een eenvoudige classificatielaag toe aan elk model en trainden het hele systeem end-to-end. Na fine-tuning verbeterde de prestatie tot gelijk of beter dan de beste one-hot-gebaseerde modellen, en de resulterende embeddings toonden eindelijk een duidelijke scheiding tussen levensvatbare en niet-levensvatbare sequenties in visualisatieplots. Interessant genoeg profiteerden globale sequentie-embeddings het meest van dit proces: eenmaal geleid door taak-specifieke feedback leerden ze de invloed van de cruciale posities te versterken in plaats van ze te laten verdrinken in de rest van de sequentie.
Wat dit betekent voor toekomstig eiwitontwerp
Voor lezers die geïnteresseerd zijn in hoe AI de volgende generatie gentherapieën en enzymen zal vormen, is de boodschap genuanceerd maar hoopvol. Out-of-the-box eiwittaalsystemen, hoe krachtig ook, kunnen de fijnmazige veranderingen over het hoofd zien die vaak bepalen of een ontworpen eiwit werkt. Simpele encoderingen en dimensiereductie houden zich in zulke settings nog steeds goed staande. Toch kunnen onderzoekers door deze modellen af te stemmen op hoogwaardige experimentele gegevens—even wanneer mutaties weinig en nauw geclusterd zijn—ze opnieuw richten op de delen van de sequentie die het meest van belang zijn. In praktische termen suggereert dit werk dat het combineren van grote voorgetrainde modellen met taak-specifieke bijscholing een robuuste weg biedt naar betrouwbaardere, machine-gestuurde ontwerpen van virale vectoren en andere ontworpen eiwitten.
Bronvermelding: Rodrigues, A.F., Ferraz, L., Balbi, L. et al. Exploring the limits of pre-trained embeddings in machine-guided protein design: a case study on predicting AAV vector viability. Sci Rep 16, 10974 (2026). https://doi.org/10.1038/s41598-026-45458-5
Trefwoorden: eiwittaalmodellen, AAV-capsideontwerp, vectoren voor gentherapie, eiwit-embeddings, machine-gestuurde eiwitengineering