Clear Sky Science · ja
FNIP2–SERCA2b 軸を標的にすることで運動失調毛細血管拡張症の代謝・ミトコンドリア障害が改善される
DNAの番人がエネルギー管理も担うとき
運動失調毛細血管拡張症は、運動障害、免疫低下、がんのリスク増加を引き起こす希少な遺伝性疾患として知られています。本研究は、患者で欠損しているATMタンパク質がDNAの保護に加えて、細胞が糖をエネルギーとして利用する方法を統括する重要な調整役であることを示しています。ATMが失われると、細胞はDNA損傷に悩まされるだけでなく、ブドウ糖の扱いにも問題をきたし、過剰なグリコーゲンが蓄積してミトコンドリアが燃料不足に陥ります。本研究は、このエネルギーのバランスを部分的に回復できる新たな分子スイッチを指し示しています。
希少疾患におけるエネルギーの問題
研究者たちは運動失調毛細血管拡張症の患者由来の皮膚細胞と健常者由来の細胞を用いて解析を始めました。広範な代謝物プロファイリングと酸素消費測定により、AT細胞は慢性的な酸化ストレス状態にあり、燃料の消費が非効率であることが明らかになりました。解糖系の主要な段階とミトコンドリアでの下流のエネルギー産生サイクルの両方が低下していました。その結果、AT細胞は代替燃料を求めるかのようにタンパク質や核酸を通常より多く分解していました。これらの欠損は単一の既知酵素欠損の再現にとどまらず、ATM欠失がより広範なシステムレベルの代謝障害を引き起こしていることを示しています。
糖が行き止まりの貯蔵に変わるとき
生細胞内で標識したブドウ糖の流れを追跡すると、AT細胞では流入した糖のうち主要なエネルギー経路を通る割合が減少していることが分かりました。代わりに、グリコーゲン代謝に関連する分解産物が蓄積していました。顕微鏡観察により、分岐したブドウ糖の貯蔵形態であるグリコーゲンがAT線維芽細胞、そこからリプログラミングした幹細胞、さらには心臓や小脳を含む患者組織において大量に蓄積していることが確認されました。運動制御に重要な小脳の神経細胞では異常なグリコーゲン沈着と、グリコーゲン合成酵素の増加が観察されました。このパターンは、ミトコンドリアが燃料を効率的に処理できない場合に、余剰のブドウ糖が貯蔵へと回され、それが脳や心臓など脆弱な臓器に負担をかける可能性を示唆しています。
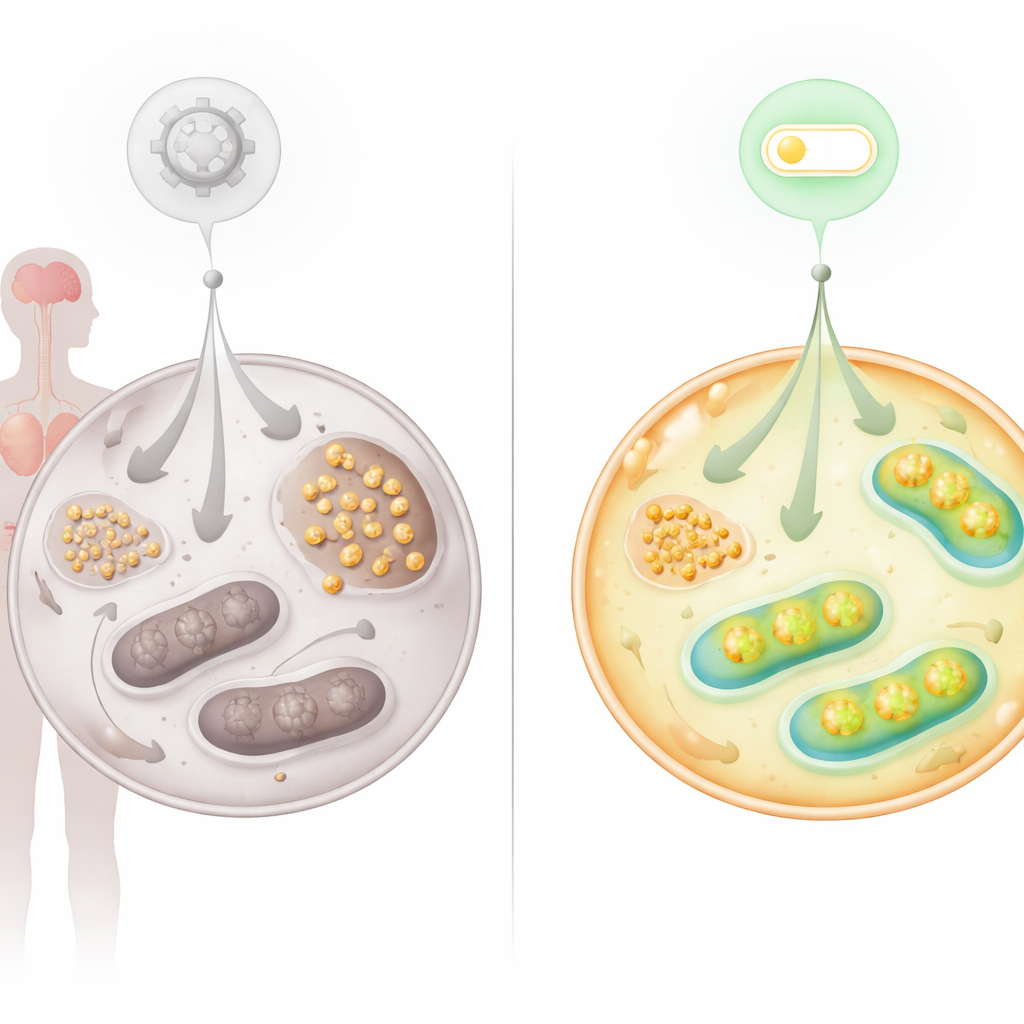
新たなスイッチの発見:FNIP2–SERCA2b 軸
代謝異常がミトコンドリアの不調を強く示唆したため、チームはミトコンドリア活性を増減させることが知られているタンパク質に着目しました。彼らは栄養およびレドックスストレスに応答するのを助けるFNIP1の近縁であるFNIP2に注目しました。AT細胞でFNIP2をサイレンシングすると、グリコーゲンの蓄積が劇的に減少し、時間経過でコロニー形成能が回復し、通常これらの細胞を悩ませる早期老化が遅延しました。詳細な生体エネルギー解析は、AT細胞でFNIP2を阻害すると解糖の促進、ミトコンドリア呼吸とATP産生の増加が起こり、糖の利用が健常細胞に過剰に作用することなく正常に近づくことを示しました。
カルシウムがもたらす救済の信号
FNIP2がどのようにこの制御を行うかを理解するため、著者らは小胞体(ER)とミトコンドリア間のカルシウム取り扱いに注目しました。彼らはFNIP2がER膜にあるカルシウムポンプSERCA2bに強く結合することを発見しました。細胞ベースのアッセイでは、FNIP2を除去するとERのカルシウム取り込みが著しく低下し、より多くのカルシウムが細胞質に残ることが示されました。増えた細胞質カルシウムはミトコンドリアの酵素や呼吸を刺激できます。電子顕微鏡所見では、AT細胞は形の歪んだミトコンドリアと異常に密で広範なER–ミトコンドリア接触領域を示しており、これらは酸化ストレスに関連する特徴です。注目すべきことに、FNIP2抑制はミトコンドリアの形状を正常化するだけでなく、より典型的なER–ミトコンドリア接触パターンを回復させ、エネルギー管理の改善と一致しました。
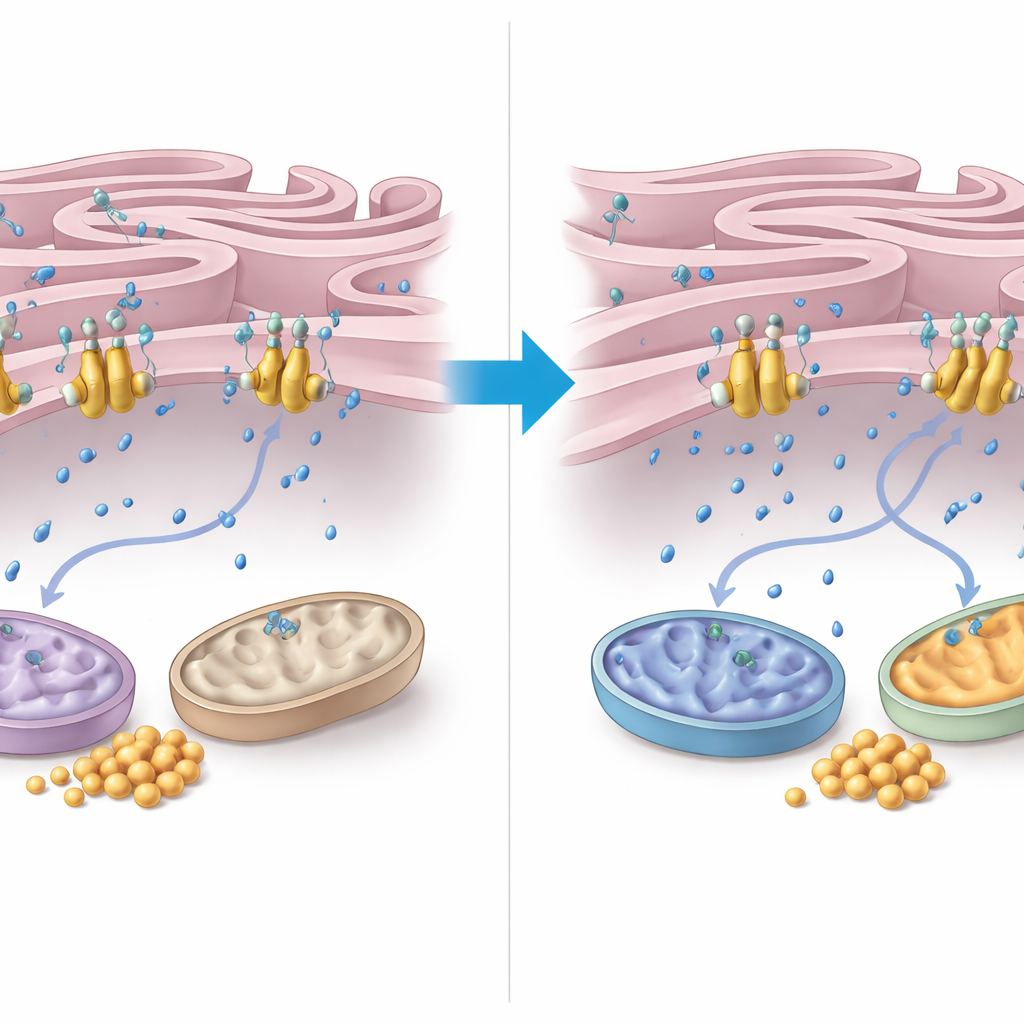
患者にとっての意義
総じて、本研究は運動失調毛細血管拡張症を単なるDNA修復障害としてだけでなく、細胞内の燃料管理不全を伴う疾患として再定義します。ATMがないとブドウ糖はエネルギーに十分に使われず、ミトコンドリアは機能不全に陥り、重要な臓器の細胞にグリコーゲンが詰まります。FNIP2の働きを弱めることで、SERCA2bカルシウムポンプへの過度な刺激が和らげられ、細胞質カルシウムが適度に上昇してミトコンドリア活動が回復し、より多くのブドウ糖を燃やしてグリコーゲン蓄積を抑えられます。本研究は細胞および組織サンプルで行われたものであるものの、FNIP2–SERCA2b 経路を代謝改善と細胞生存の向上を目指す治療戦略の有望な標的として特定しています。
引用: Vinciguerra, M., El Kharef, C., Bruhn, C. et al. Targeting the FNIP2-SERCA2b axis improves metabolic and mitochondrial defects in Ataxia Telangiectasia. Cell Death Dis 17, 290 (2026). https://doi.org/10.1038/s41419-026-08507-5
キーワード: 運動失調毛細血管拡張症, 細胞代謝, ミトコンドリア, カルシウムシグナル伝達, グリコーゲン蓄積