Clear Sky Science · ar
استهداف محور FNIP2‑SERCA2b يحسّن العيوب الأيضية والميتوحيوية في الترنح الشعيري
عندما يدير حارس الحمض النووي في الخلية أيضاً الطاقة
الترنح الشعيري معروف بشكل أساسي كمرض جيني نادر يسبب اضطرابات في الحركة وضعفاً مناعياً ومخاطر للإصابة بالسرطان. تُظهر هذه الدراسة أن البروتين ATM المفقود في هؤلاء المرضى، إلى جانب دوره في حماية الحمض النووي، يعمل أيضاً كمنظم رئيسي لكيفية استخدام الخلايا للسكر لإنتاج الطاقة. عند فقدان ATM، لا تعاني الخلايا فحسب من تلف الحمض النووي، بل تفشل أيضاً في التعامل مع الجلوكوز؛ فتتكدس بالجلايكوجين الزائد وتترك ميتوكوندرياتها محرومة من الوقود. يشير العمل إلى مفتاح جزيئي جديد يمكن تبديله لاستعادة هذا التوازن الطاقي جزئياً.
خلل في الطاقة في مرض نادر
بدأ الباحثون بخلايا جلدية مأخوذة من مرضى بالترنح الشعيري ومن متطوعين أصحاء. باستخدام تحليل واسع للمتقلبات الأيضية وقياسات استهلاك الأكسجين، وجدوا أن خلايا AT تعيش في حالة إجهاد أكسدي مزمن وتستغل الوقود بشكل غير فعّال. كانت خطوات مفتاحية من تحلل السكر (السكّرية التحللية) والدورة المولدة للطاقة في الميتوكوندريا كلاهما بطيئتين. ونتيجة لذلك، قامت خلايا AT بتحليل البروتينات والأحماض النووية أكثر من المعتاد، كما لو أنها تبحث عن مصادر وقود بديلة. لم تكن هذه العيوب مجرد إعادة لتقصير إنزيمي معروف واحد، مما يدل على أن فقدان ATM يسبب فشلاً أيضياً أوسع وعلى مستوى النظام.
عندما يتحول السكر إلى مخزون مسدود
تتبّع الجلوكوز الموسوم داخل الخلايا الحية أظهر أن جزءاً أقل من السكر الداخل يمر عبر مسارات الطاقة الرئيسية في خلايا AT. وبدلاً من ذلك، تراكمت نواتج التحلل المرتبطة بتمثيل الجلايكوجين. أكدت المجهرية أن الجلايكوجين — شكل متفرّع لتخزين الجلوكوز — تراكم بكثافة في الخلايا الليفية لمرضى AT، وفي الخلايا الجذعية المعاد برمجتها من تلك الخلايا الليفية، وفي أنسجة من مرضى AT، بما في ذلك القلب والمخيخ. أظهرت الخلايا العصبية في المخيخ، الضرورية للتحكم الحركي، رواسب جلايكوجين غير طبيعية ومستويات مرتفعة من الإنزيم المسؤول عن تصنيع الجلايكوجين. يشير هذا النمط إلى أنه عندما تعجز الميتوكوندريا عن معالجة الوقود بكفاءة، تحول الخلايا فائض الجلوكوز إلى مخزون، مما قد يضغط بدوره على أعضاء حساسة مثل الدماغ والقلب.
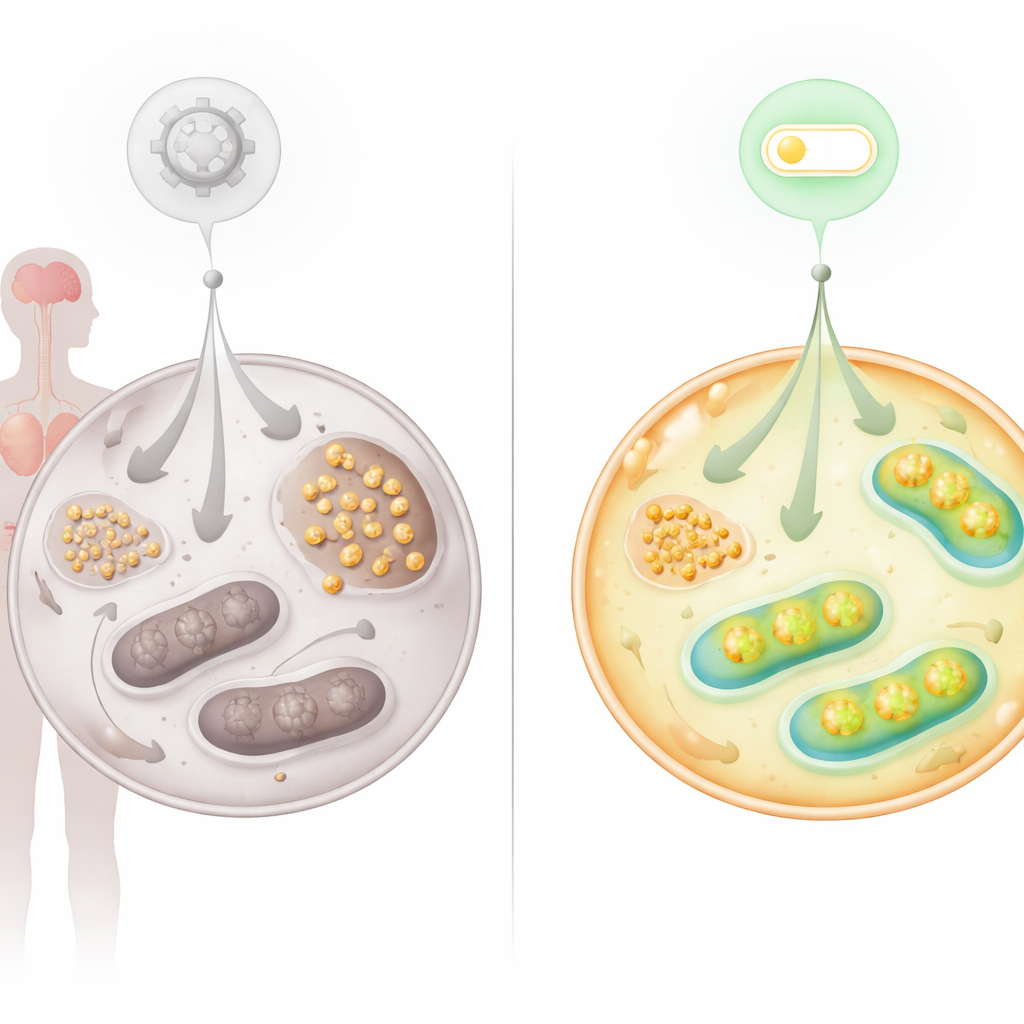
اكتشاف مفتاح جديد: محور FNIP2–SERCA2b
بما أن المشاكل الأيضية أشارت بقوة إلى ميتوكوندريا معطلة، نظر الفريق إلى بروتينات معروفة بضبط نشاط الميتوكوندريا صعوداً وهبوطاً. ركزوا على FNIP2، قريبة FNIP1، التي تساعد الخلايا على الاستجابة لإجهاد المغذيات والأكسدة. أدى إسكات FNIP2 في خلايا AT إلى تقليل تراكم الجلايكوجين بشكل كبير واستعادتها القدرة على تكوين مستعمرات على مدى الزمن، مؤجلاً الشيخوخة المبكرة التي تصيب هذه الخلايا عادة. أظهرت اختبارات الطاقة الدقيقة أن منع FNIP2 في خلايا AT عزز التحلل السكري وزاد من تنفس الميتوكوندريا وإنتاج ATP، مقرباً استهلاك الجلوكوز إلى المستويات الطبيعية دون تجاوز التصحيح في الخلايا السليمة.
كيف ينقل الكالسيوم إشارة الإنقاذ
لفهم كيفية ممارسة FNIP2 لهذا التحكم، ركز المؤلفون على معالجة الكالسيوم بين الشبكة الإندوبلازمية والميتوكوندريا. اكتشفوا أن FNIP2 يرتبط بقوة بمضخة الكالسيوم في غشاء الشبكة الإندوبلازمية المسماة SERCA2b. في تجارب خلوية، أدى إزالة FNIP2 إلى تقليل حاد في امتصاص الشبكة الإندوبلازمية للكالسيوم، ما يعني بقاء كمية أكبر من الكالسيوم في السيتوبلازم المحيط. يمكن لهذا الكالسيوم الإضافي أن ينشط إنزيمات الميتوكوندريا ويزيد التنفس الميتوكوندري. كشفت الميكروسكوب الإلكتروني أن خلايا AT تملك ميتوكوندريا مشوهة ومناطق تلامس بين الشبكة الإندوبلازمية والميتوكوندريا ضيقة وواسعة بشكل غير عادي — سمات مرتبطة بالإجهاد التأكسدي. ومن اللافت أن كبت FNIP2 لم يقتصر على تطبيع شكل الميتوكوندريا فحسب، بل أعاد أيضاً أنماط التلامس بين الشبكة الإندوبلازمية والميتوكوندريا إلى نمط أكثر طبيعية، متسقاً مع إدارة طاقية صحية أكثر.
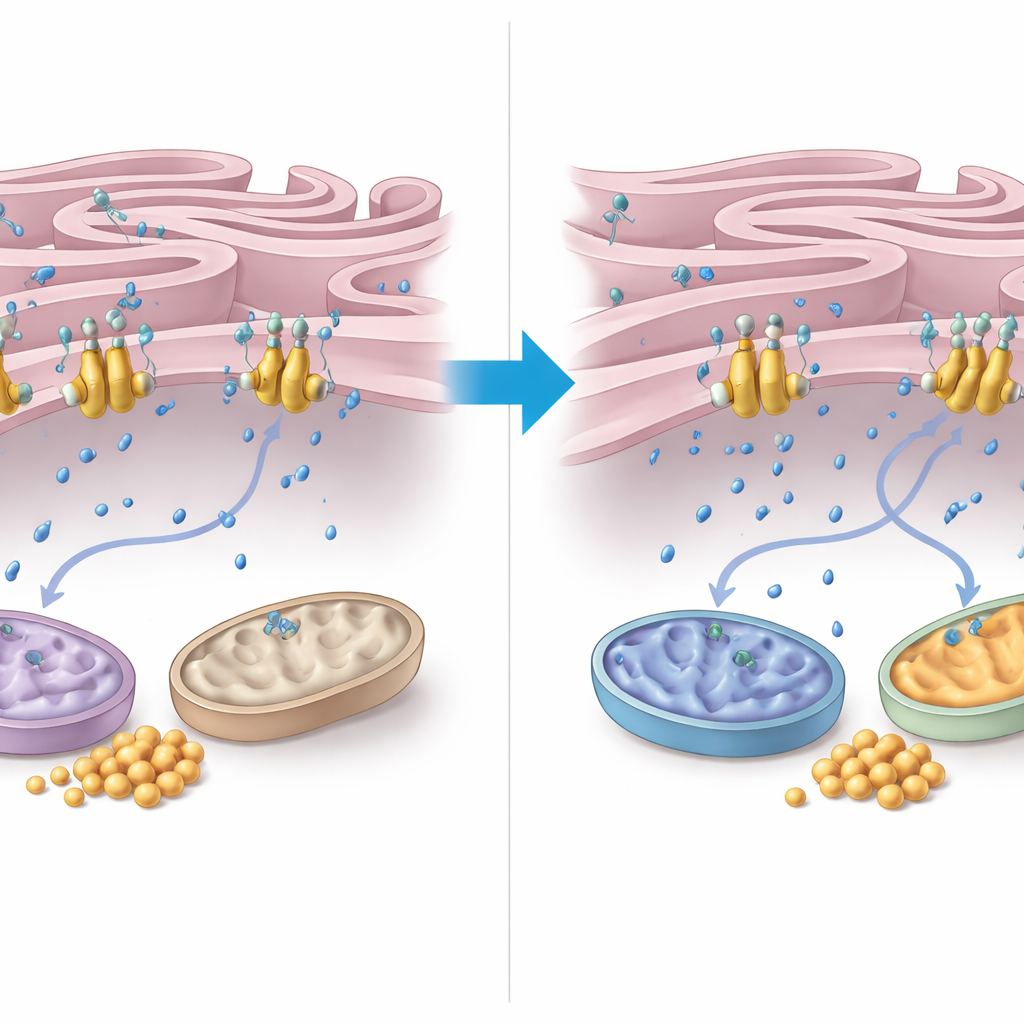
ما الذي يعنيه هذا للمرضى
تُعيد هذه النتائج، مجتمعة، تصوير الترنح الشعيري ليس فقط كاضطراب لإصلاح الحمض النووي بل أيضاً كمرض ناجم عن سوء إدارة وقود الخلية. من دون ATM، يُستَخدم الجلوكوز أقل لإنتاج الطاقة، وتؤدي الميتوكوندريا أداءً أدنى، ويتسبب الجلايكوجين في انسداد الخلايا في أعضاء حيوية. عبر تخفيف عمل FNIP2 — وبالتالي تقليل تحفيزه لمضخة الكالسيوم SERCA2b — يمكن للخلايا زيادة الكالسيوم السيتوبلازمي بما يكفي لإحياء نشاط الميتوكوندريا، وحرق المزيد من الجلوكوز، والحد من تراكم الجلايكوجين. بينما أُجريت هذه الدراسة في خلايا وعينات نسيجية، فإنها تحدد محور FNIP2–SERCA2b كهدف واعد لعلاجات تهدف إلى تحسين الأيض وبقاء الخلايا لدى الأشخاص الذين يعيشون مع هذا المرض المعقد.
الاستشهاد: Vinciguerra, M., El Kharef, C., Bruhn, C. et al. Targeting the FNIP2-SERCA2b axis improves metabolic and mitochondrial defects in Ataxia Telangiectasia. Cell Death Dis 17, 290 (2026). https://doi.org/10.1038/s41419-026-08507-5
الكلمات المفتاحية: الترنح الشعيري, تمثيل الخلايا للطاقة, الميتوكوندريا, إشارات الكالسيوم, تراكم الجلايكوجين