Clear Sky Science · he
פגיעה בציר FNIP2–SERCA2b משפרת ליקויים מטבוליים ומיטוכונדריאליים באטקסיה טלנגיאקטזיה
כאשר שומר ה-DNA של התא גם מנהל את האנרגיה
אטקסיה טלנגיאקטזיה מוכרת בעיקר כמחלה גנטית נדירה הגורמת לבעיות בתנועה, לחולשת מערכת החיסון ולהגברת סיכון לסרטן. המחקר הזה מראה שבלעדיות לחלבון ה-ATM החסר בחולים אלה, הוא לא רק שומר על ה-DNA — אלא גם משמש כמנהל מרכזי של האופן שבו תאים משתמשים בסוכר לאנרגיה. כאשר ATM נפגע, תאים לא רק מתקשים בתיקון נזקי DNA — הם גם מטפלים בגלקוז בצורה לקויה: מצטברת בהם כמות עודפת של גליקוגן והמיטוכונדריות שלהם נסמכות על דלק מועט. העבודה מצביעה על מתג מולקולרי חדש שניתן להפוך כדי לשחזר חלקית את מאזן האנרגיה הזה.
בעיות אנרגיה במחלה נדירה
החוקרים התחילו בתאים עור שנלקחו מאנשים עם אטקסיה טלנגיאקטזיה וממתנדבים בריאים. באמצעות פרופיל מטבוליטים רחב ומדידות צריכת חמצן מצאו שתאי AT חיים במצב של דחק חמצוני כרוני ושריפת דלק לקויה. שלבים מרכזיים בפירוק הסוכר (גליקוליזה) והמעגל התאי לייצור אנרגיה במיטוכונדריה היו שניהם מאטים. כתוצאה מכך, תאי AT פירקו חלבונים וחומר גנטי יותר מהרגיל, כאילו הם מחפשים דלקים חלופיים. ליקויים אלה אינם פשוט העתקה של חסר באנזים בודד ידוע, מה שמרמז שאובדן ATM גורם לכישלון מטבולי ברמת מערכת רחבה יותר.
כאשר הסוכר הופך למחסן ללא מוצא
מעקב אחר גלוקוז מסומן בתוך תאים חיים הראה שחלק קטן יותר מהסוכר הנכנס עבר דרך מסלולי האנרגיה המרכזיים בתאי AT. במקום זאת, מוצרי פירוק הקשורים למטבוליזם של גליקוגן הצטברו. מיקרוסקופיה אישרה שגליקוגן — צורת אגירה מסועפת של גלוקוז — נבנה בכמויות גדולות בפיברובלסטים של AT, בתאים סטרמליים שעברו תכנות מחדש מהפיברובלסטים האלה, וברקמות מחולי AT, כולל הלב והצרבלום. תאי עצב בצרבלום, החיוניים לשליטה בתנועה, הראו משקעים בלתי רגילים של גליקוגן ורמות מוגברות של האנזים שמייצר גליקוגן. התבנית הזו מצביעה על כך שכאשר המיטוכונדריות אינן יכולות לעבד דלק ביעילות, תאים מנתבים גלוקוז עודף לאגירה — מה שעלול להעמיס על אברים פגיעים כמו מוח ולב.
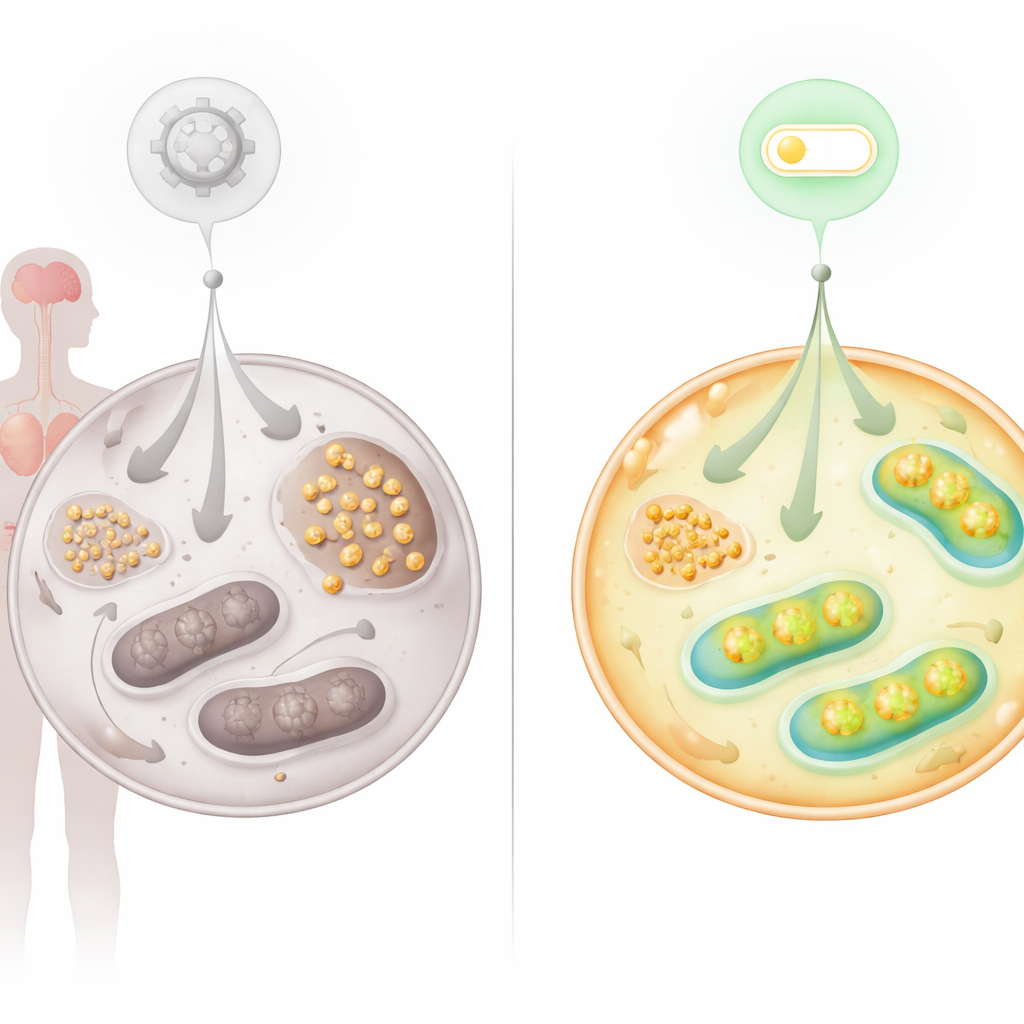
גילוי מתג חדש: ציר FNIP2–SERCA2b
מכיוון שהבעיות המטבוליות רמזו בעוצמה על מיטוכונדריות פגומות, הצוות בחן חלבונים הידועים בוויסות פעילות מיטוכונדריאלית. הם התמקדו ב-FNIP2, בן משפחה של FNIP1, שעוזר לתאים להגיב לסטרס תזונתי ותחמצוני. השתקת FNIP2 בתאי AT הפחיתה באופן דרמטי את הצטברות הגליקוגן ושיחזרה את יכולתם ליצור מושבות לאורך זמן, מה שעיכב את ההזדקנות המוקדמת שמאפיינת תאים אלה. בדיקות ביואנרגטיות מפורטות הראו שהחסימה של FNIP2 בתאי AT שיפרה את הגליקוליזה והגדילה את הנשימה המיטוכונדריאלית וייצור ה-ATP, מה שהקריב את ניצול הגלוקוז קרוב יותר לנורמה מבלי לתקן יתר על המידה בתאים בריאים.
כיצד סידן מעביר את אות החילוץ
כדי להבין כיצד FNIP2 מפעיל שליטה זו, המחברים בחנו את הטיפול בסידן בין הרשתית התוך-תאית (ER) למיטוכונדריה. הם גילו ש-FNIP2 נקשר בחוזקה למשאבת סידן בממברנת ה-ER שנקראת SERCA2b. בניסויים תאיים, הסרת FNIP2 הפחיתה בחדות את קליטת הסידן ב-ER, כלומר יותר סידן נותר בציטוזול הסובב. סידן נוסף זה יכול לעורר אנזימי מיטוכונדריה ונשימה. מיקרוסקופ אלקטרונים הראה שתאי AT מכילים מיטוכונדריות משוחות ואזורי מגע בין ER למיטוכונדריה שהם צמודים ונדירים במידה חריגה — תכונות המקושרות לדחק חמצוני. באופן בולט, דיכוי FNIP2 לא רק הנרמל את צורת המיטוכונדריה אלא גם שחזר דפוסי מגע בין ER למיטוכונדריה הנוטים יותר לנורמה, בהתאמה לניהול אנרגיה בריא יותר.
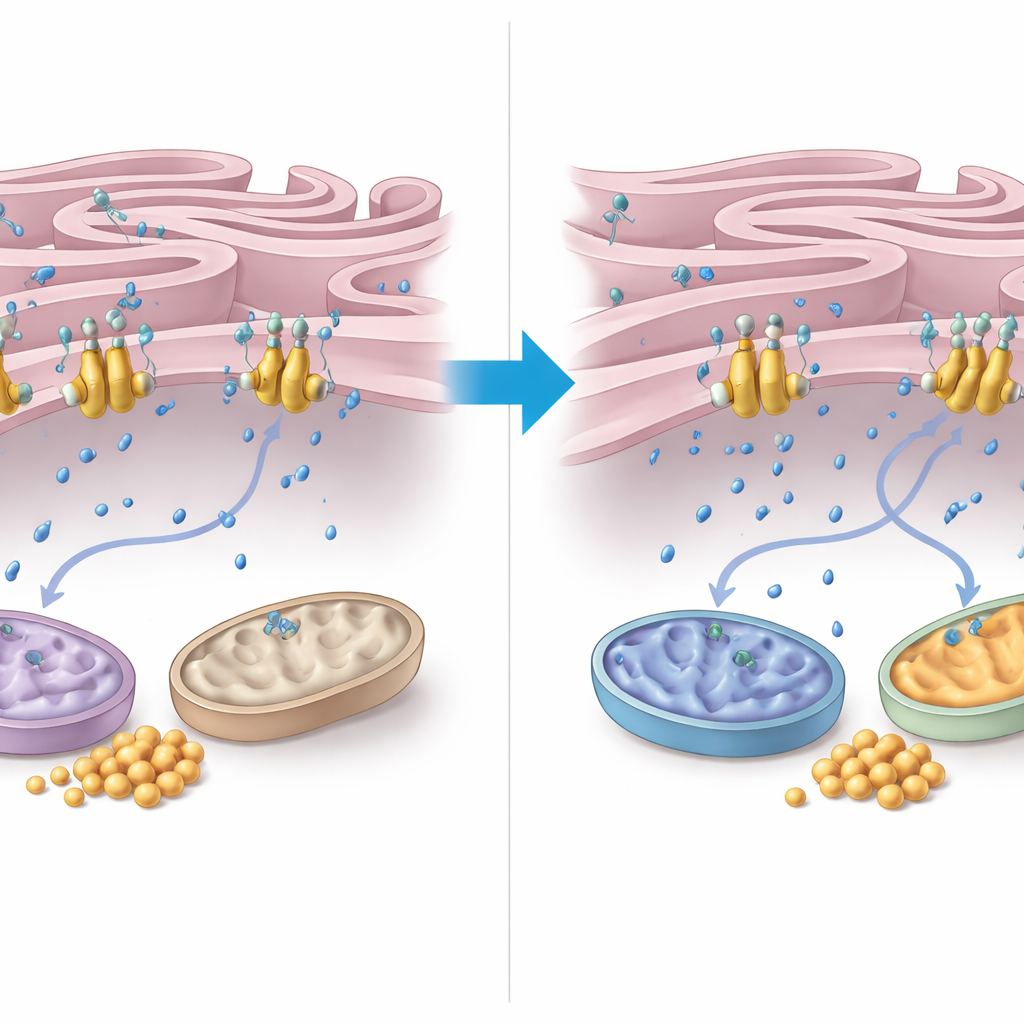
מה משמעות הדבר עבור החולים
במכלול, הממצאים משנים את התפיסה של אטקסיה טלנגיאקטזיה — לא רק כהפרעה בתיקון DNA אלא גם כמחלה של ניהול דלק תאית לקוי. ללא ATM, גלוקוז מנוצל פחות לאנרגיה, המיטוכונדריות מתפקדות פחות בגלוי וגליקוגן חוסם תאים באיברים קריטיים. על ידי הורדת פעילות FNIP2 — ובכך הקלה על גירוי משאבת הסידן SERCA2b — תאים יכולים להעלות מעט את רמת הסידן הציטוזולי כדי להפיח פעילות מיטוכונדריאלית, לשרוף יותר גלוקוז ולמנוע הצטברות גליקוגן. אמנם העבודה בוצעה בתאים ובמדגמי רקמה, אך היא מזהה את נתיב FNIP2–SERCA2b כיעד מבטיח לפיתוח טיפולים שמטרתם לשפר את המטבוליזם וההישרדות התאית בקרב אנשים החיים עם מצב מורכב זה.
ציטוט: Vinciguerra, M., El Kharef, C., Bruhn, C. et al. Targeting the FNIP2-SERCA2b axis improves metabolic and mitochondrial defects in Ataxia Telangiectasia. Cell Death Dis 17, 290 (2026). https://doi.org/10.1038/s41419-026-08507-5
מילות מפתח: אטקסיה טלנגיאקטזיה, מטבוליזם תאית, מיטוכונדריה, איתות סידן, הצטברות גליקוגן