Clear Sky Science · zh
细菌抗生素外排泵过渡态抑制剂的分子机制
为何阻止细菌“泵”能拯救抗生素
抗生素耐药性常常并非因为药物无法作用于其靶点,而是因为细菌积极地将其泵出。这项研究以原子级细节揭示了一种新设计的化合物如何卡住一种重要的细菌泵,并使现有抗生素再次发挥强效。理解这一分子“楔子”的工作原理,可能为联合疗法打开大门,从而恢复我们面临失去风险的药物效力。
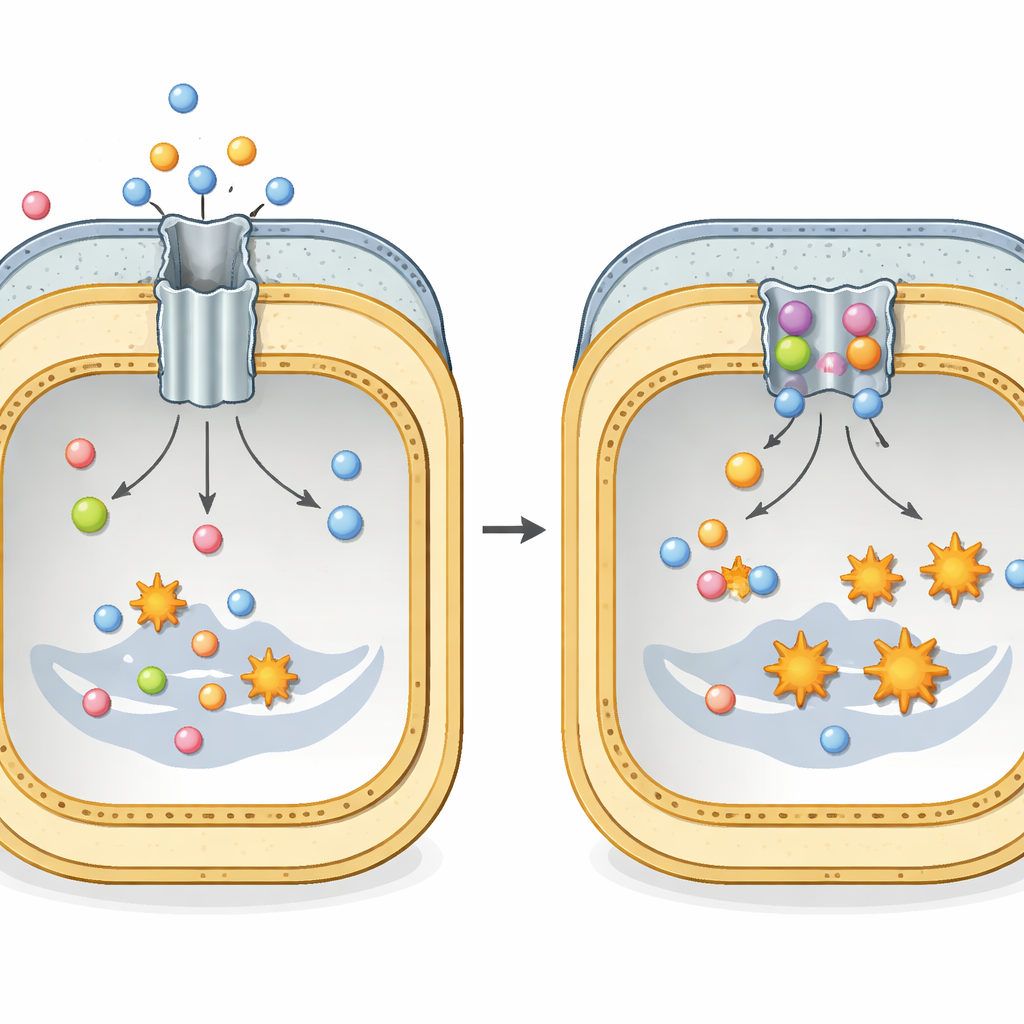
抗生素的隐秘逃生通道
许多危险的革兰氏阴性菌,如Escherichia coli和Klebsiella pneumoniae,依赖一种叫做 AcrAB–TolC 的大型蛋白质复合体来抵御抗生素治疗。该复合体跨越整个细胞包膜,像一条带有内端马达的通道。内膜部分称为 AcrB,识别各种药物和其他有毒分子,并利用细胞能量将它们排到细胞外。每个 AcrB 单元由三个重复部分构成,持续在三种构象之间循环——松结合、紧结合和向外开放——产生一种蠕动式运动,将抗生素在其造成持久损害前推动出去。
设计更智能的分子楔子
药物开发者长期尝试阻断该泵,但以往的大多数抑制剂结合在一个宽大油腻的口袋中,该口袋也会吸引许多其他分子,导致溶解性差及副作用。作者在以往工作的基础上,将注意力转向一种新的化合物家族——吡啶基哌嗪,它们嵌入 AcrB 跨膜部分更为专门的区域。借助高分辨率结构数据,他们重新设计了化学骨架,使其与位于泵正常转运质子通路上的两个带负电的氨基酸(D408 和 E947)形成更强的接触。通过添加一个位置精确的苄胺侧链,他们得到了一种新化合物 BDM91531,其结合紧密度比前代提高约五十倍,并在极低浓度下增强多种抗生素的活性。
在半行程中锁死泵
X 射线晶体学和单颗粒冷冻电镜精确展示了 BDM91531 如何使泵失效。该化合物位于一个延伸的空腔中,夹在一个 AcrB 亚单位内的若干跨膜螺旋之间。由于 BDM91531 带有两个正电荷,它与口袋深处的 D408 和接近胞质缘的 E947 形成强盐桥。这两个接触点像桥一样将抑制剂悬挂在泵的内壁与细胞内侧之间。被锁定后,该化合物使该亚单位陷入开放与松结合构象之间的一个中间状态——这种瞬态构象在泵的正常循环中通常只短暂出现。由于三个亚单位必须以同步方式轮换它们的状态,锁死其中一个就会使整个机械停摆,从而停止药物外排。
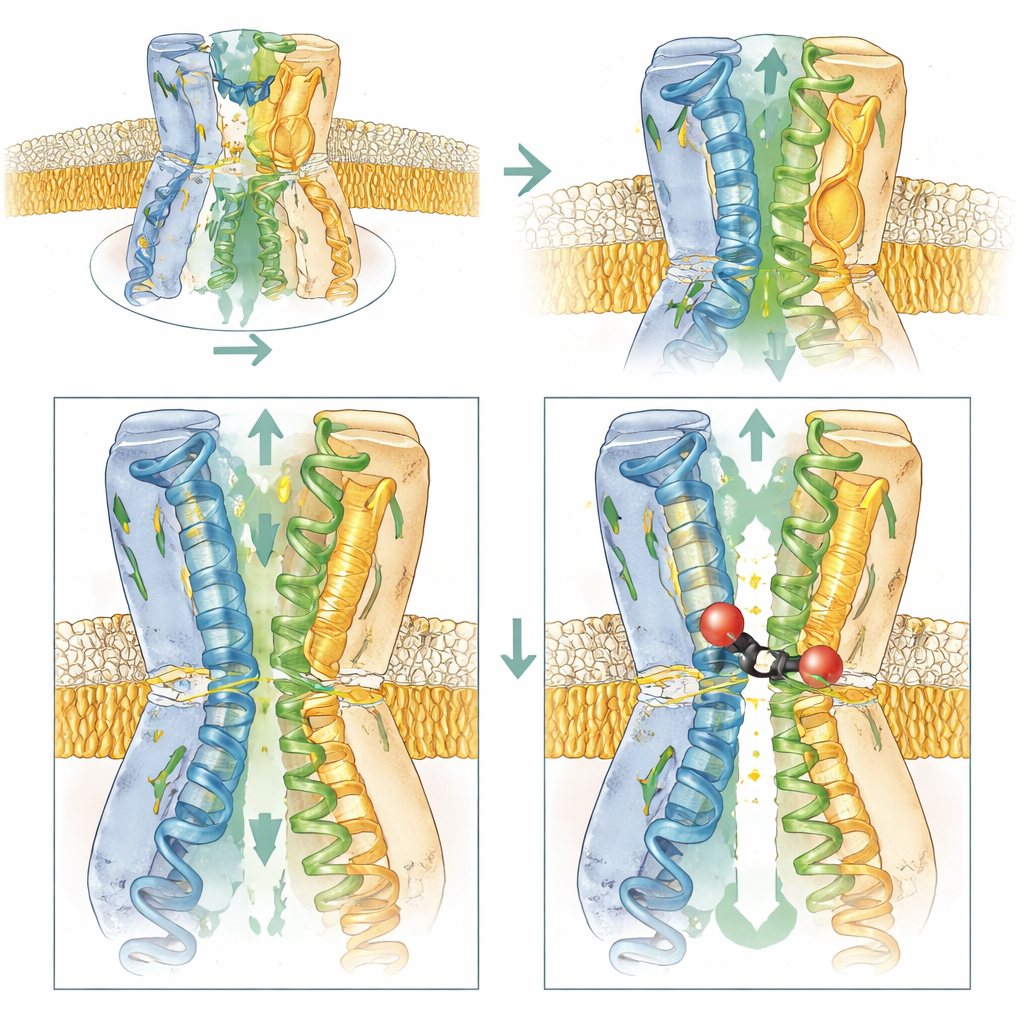
给入口带电以拉入抑制剂
研究团队结合生物物理测量、细菌生长实验和计算模拟,探查 AcrB 哪些部分对 BDM91531 的作用最为重要。去掉 D408 的负电荷会完全消除结合,证实了其关键作用。改变 E947 或附近的酸性残基 D951 会使细菌对抑制剂的敏感性降低,而在邻近位点重新引入负电荷则能恢复甚至增强敏感性。这表明,这些酸性残基除了作为锚点外,还通过吸引带正电的抑制剂从胞质进入结合口槽,帮助将其吸入。相反,移除这些电荷或使入口区更中性,会降低抑制剂的进入和结合。
通过针对运动而非药物本身复活抗生素
通俗地说,BDM91531 的作用机制是在恰当时刻卡住细菌泵的一个运动部件,阻止机器完成其循环并将抗生素困在细胞内,使其能发挥作用。由于在阻断泵所需剂量下该抑制剂本身并不杀死细菌,它最好被视为与现有药物联合使用的助推剂。这项工作提供的结构和机制见解明确指出了应针对泵的哪些特征来设计更好的阻断剂,从而提高新的佐剂疗法的前景,使某些顽固感染对抗生素重新敏感。
引用: Börnsen, C., Müller, R.T., Vieira Da Cruz, A. et al. Molecular mechanism of transition-state inhibitors of bacterial antibiotic efflux pumps. npj Antimicrob Resist 4, 35 (2026). https://doi.org/10.1038/s44259-026-00207-6
关键词: 抗生素耐药性, 外排泵抑制剂, AcrB, 革兰氏阴性菌, 基于结构的药物设计