Clear Sky Science · he
המנגנון המולקולרי של מעכבים במצב מעבר למשאבות הוצאת אנטיביוטיקה חיידקיות
מדוע עצירת "משאבות" חיידקיות עשויה להציל אנטיביוטיקה
עמידות לאנטיביוטיקה לעיתים קרובות נובעת לא מפני שהתרופות לא פוגעות במטרותיהן, אלא מפני שחיידקים מפנים אותן החוצה באמצעות הוצאה פעילה. במחקר זה נחשף, ברזולוציה אטומית, כיצד תרכובת שתוכננה לאחרונה תקעה משאבה חיידקית מרכזית והחזירה את האפקטיביות של אנטיביוטיקות קיימות. הבנת אופן הפעולה של ה"טריז" המולקולרי הזה יכולה לפתוח את הדלת לטיפולי שילוב שישיבו לשימוש תרופות שאנו בסכנת אובדן שלהן.
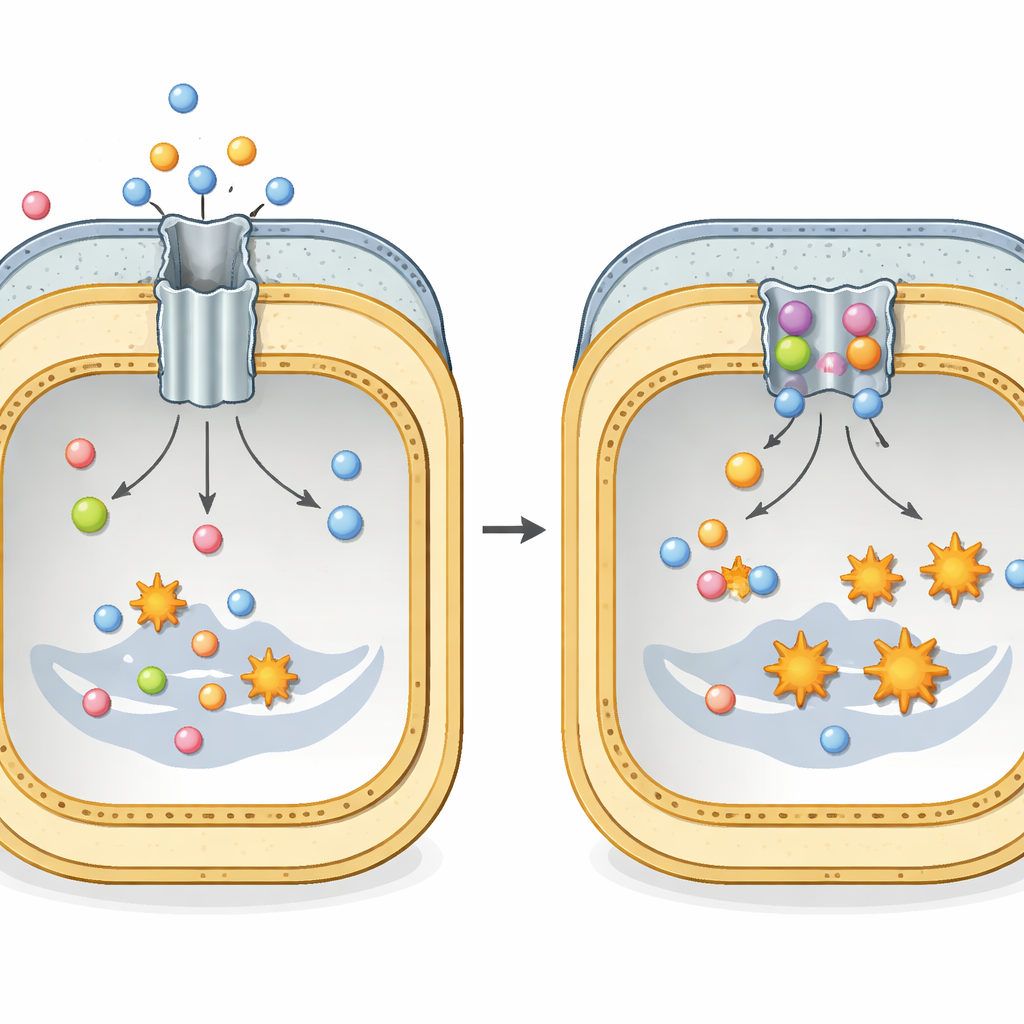
מנהרה נסתרת למנוסת אנטיביוטיקה
חיידקי גרם-שליליים מסוכנים רבים, כגון Escherichia coli ו-Klebsiella pneumoniae, נסמכים על קומפלקס חלבוני גדול הנקרא AcrAB–TolC כדי לשרוד טיפול אנטיביוטי. קומפלקס זה חוצה את מעטפת התא כולה ופועל כמו מנהרה עם מנוע בקצה הפנימי. החלק שברשת הממברנה הפנימית, הנקרא AcrB, מזהה מגוון רחב של תרופות ומולקולות רעילות אחרות ומשתמש באנרגיה תאית להוציאן החוצה. כל יחידת AcrB מוקמת משלושה חלקים חוזרים המחזיקים מחזור מתמיד של שלוש צורות — קשירה רופפת, קשירה הדוקה, ופתיחה החוצה — היוצרות תנועה פריסטלטית שדוחפת אנטיביוטיקה החוצה לפני שיוכלו לגרום נזק מתמשך.
עיצוב "טריז" מולקולרי חכם יותר
מפתחי תרופות ניסו זמן רב לחסום משאבה זו, אך מרבית המעכבים מוקדמים נקשרו בכיס שומני גדול שמושך גם מולקולות רבות אחרות, מה שהוביל לבעיות מסיסות ותופעות לוואי. בהתבסס על עבודות קודמות, המחברים התמקדו במקום זאת במשפחת תרכובות חדשה יותר הנקראת פירידילפיפרזינים, הנכנסות לאזור מיוחד יותר בעומק החלק החוצה-ממברנה של AcrB. בהנחיית נתוני מבנה ברזולוציה גבוהה הם תכננו מחדש את שלד המולקולה כדי ליצור אינטראקציות חזקות יותר עם שתי חומצות אמינו בעלות מטען שלילי (D408 ו-E947) השוכנות לאורך המסלול שבו המשאבה בדרך כלל מעבירה פרוטונים. על ידי הוספת שרשרת צד בנזילאמין ממוקמת בקפידה, הם יצרו תרכובת חדשה, BDM91531, שנקשרת בערך פי חמישים יותר חזק מקודמתה ומגבירה את הפעילות של מספר אנטיביוטיקות בריכוזים נמוכים מאוד.
הקפאת המשאבה באמצע המהלך
קריסטלוגרפיית קרני רנטגן ומיקרוסקופיית קריו-אלקטרון חד-חלקיקית הראו בדיוק כיצד BDM91531 משביתת את המשאבה. התרכובת יושבת במערה מוארכת בין כמה הליקסים החוצים את הממברנה בתוך תת-יחידת AcrB אחת. מאחר ש-BDM91531 נושאת שני מטענים חיוביים, היא יוצרת גשרים מלוחים חזקים עם D408 עמוק בכיס ועם E947 סמוך לשפה הציטופלזמית. שתי נקודות המגע הללו תלו את המעכב כמו גשר בין הקיר הפנימי של המשאבה לבין פנים התא. נעולה במקומה, התרכובת לוכדת את תת-היחידה במצב חצי-דרך בין הקונפורמציות הפתוחה והרופפת — צורה חולפת שהמשאבה עוברת רק לזמן קצר. מאחר שעל שלוש תת-היחידות להסתובב דרך מצבן בסינכרון, הקפאת אחת מהן מעכבת את המכונה כולה ומפסיקה את הוצאת התרופות.
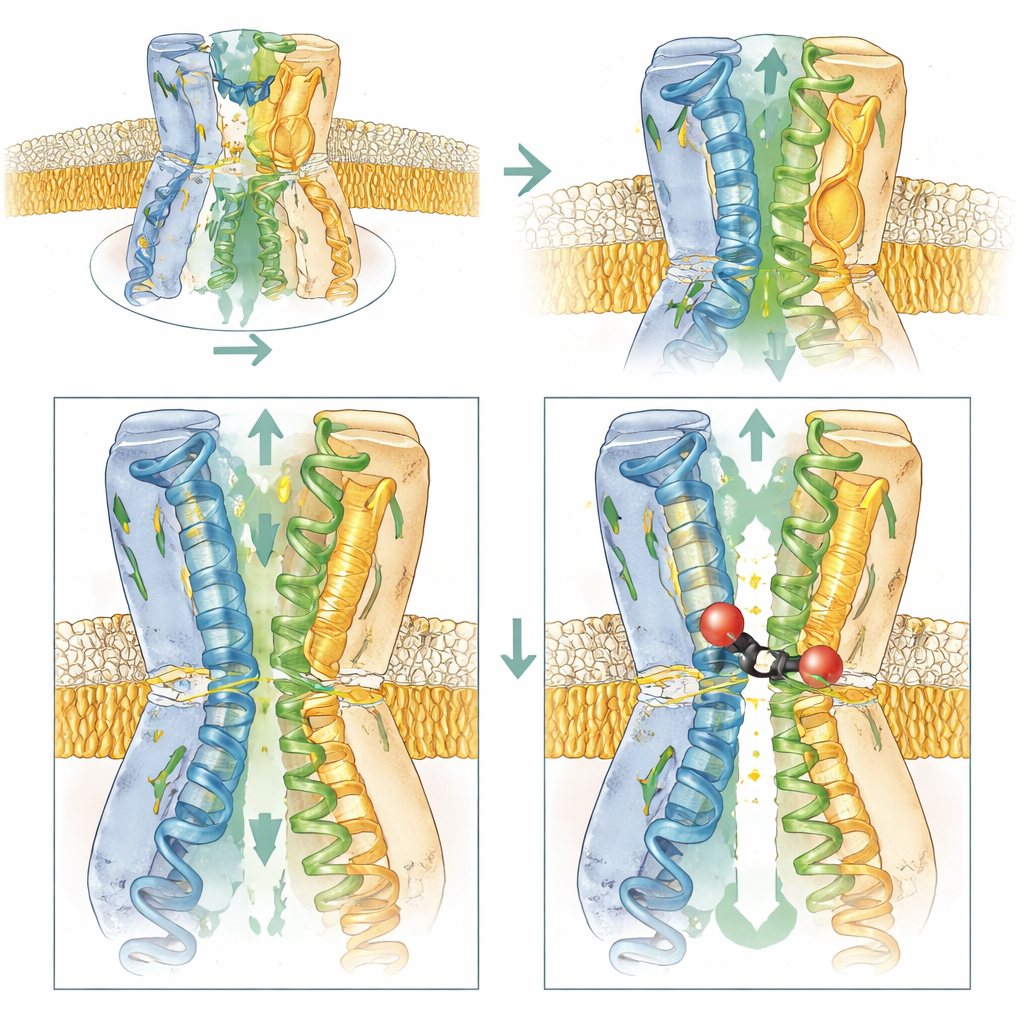
טעינת הכניסה כדי למשוך את המעכב פנימה
הצוות שילב מדידות ביו-פיזיקליות, מבחני גדילה חיידקיים וסימולציות ממוחשבות כדי לבחון אילו אזורים ב-AcrB חשובים יותר לפעולת BDM91531. הסרת המטען השלילי ב-D408 ביטלה את הקשירה לחלוטין, מה שאישר את תפקידה המרכזי. שינוי ב-E947 או בחומצת חומצה סמוכה, D951, הפחית את רגישות החיידקים למעכב, בעוד שהחזרת מטענים שליליים בעמדות שכנות השיבה או אף הגברה של הרגישות. ממצאים אלה מראים שלהוציא מתפקידה כנקודות עגינה, שאריות חומציות אלה מסייעות למשוך את המעכב החיובי מהציטופלזמה לתוך חריץ הכניסה של כיס הקשירה. בניגוד לכך, שינויים שהסירו מטענים אלה או שעשו את אזור הכניסה ניטרלי יותר הפחיתו גם את הגישה וגם את הקשירה.
השבת אנטיביוטיקה על ידי מטרה בתנועה, לא בתרופה
במונחים פשוטים, BDM91531 פועל על ידי תקיעת חלק נייד של משאבה חיידקית ברגע המדויק, מונע מהמכונה להשלים את מחזור הפעולה ולוכד את האנטיביוטיקה בתוך התא שם היא יכולה להשפיע. מכיוון שהמעכב לא הורג חיידקים בפני עצמו במינונים הדרושים לחסימת המשאבה, יש להתייחס אליו כחיזוק לשילוב עם תרופות קיימות. התובנות המבניות והמכניסטיות מהעבודה מדגישות בדיוק אילו תכונות של המשאבה יש למקד כדי לתכנן חסמים טובים אף יותר, ומעלות את האפשרות לטיפולי עזר חדשים שישיבו את עוצמת האנטיביוטיקות נגד חלק מהזיהומים העיקשים ביותר שלנו.
ציטוט: Börnsen, C., Müller, R.T., Vieira Da Cruz, A. et al. Molecular mechanism of transition-state inhibitors of bacterial antibiotic efflux pumps. npj Antimicrob Resist 4, 35 (2026). https://doi.org/10.1038/s44259-026-00207-6
מילות מפתח: עמידות לאנטיביוטיקה, מעכב משאבת הוצאה, AcrB, חיידקי גרם-שליליים, עיצוב תרופות מונחה מבנה