Clear Sky Science · es
Mecanismo molecular de inhibidores del estado de transición de bombas de eflujo bacterianas de antibióticos
Por qué detener las “bombas” bacterianas podría salvar los antibióticos
La resistencia a los antibióticos a menudo surge no porque los fármacos dejen de alcanzar sus dianas, sino porque las bacterias los expulsan activamente. Este estudio revela, con detalle atómico, cómo un compuesto recién diseñado atasca una bomba bacteriana importante y devuelve la eficacia a antibióticos existentes. Entender cómo funciona esta “cuña” molecular podría abrir la puerta a terapias combinadas que revivan fármacos que estamos en peligro de perder.
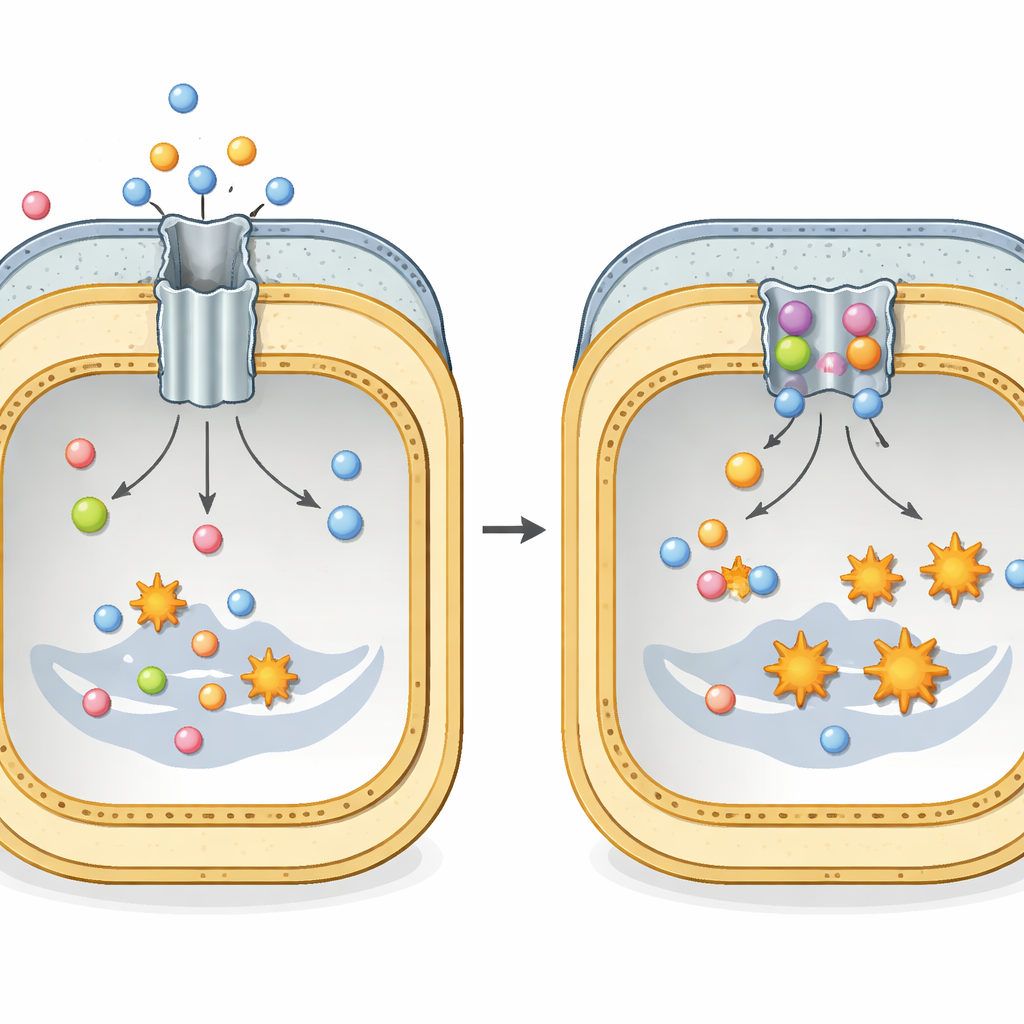
Un túnel de escape oculto para los antibióticos
Muchas bacterias Gram negativas peligrosas, como Escherichia coli y Klebsiella pneumoniae, dependen de un gran ensamblaje proteico llamado AcrAB–TolC para sobrevivir al tratamiento antibiótico. Este ensamblaje atraviesa toda la envoltura celular y funciona como un túnel con un motor en su extremo interior. La parte de la membrana interna, llamada AcrB, reconoce una amplia variedad de fármacos y otras moléculas tóxicas y utiliza la energía celular para expulsarlas al exterior. Cada unidad de AcrB está formada por tres partes repetidas que ciclan continuamente por tres conformaciones—ligeramente unida, fuertemente unida y abierta al exterior—creando un movimiento peristáltico que empuja los antibióticos hacia fuera antes de que puedan causar daño duradero.
Diseñando una cuña molecular más inteligente
Los desarrolladores de fármacos han intentado durante mucho tiempo bloquear esta bomba, pero la mayoría de los inhibidores anteriores se unían en un gran bolsillo grasiento que también atraía muchas otras moléculas, provocando mala solubilidad y efectos secundarios. Partiendo de trabajos previos, los autores se centraron en cambio en una familia más nueva de compuestos llamados piridilpiperazinas que se alojan en una región más especializada, profunda en la parte iniciada en la membrana de AcrB. Guiados por datos estructurales de alta resolución, rediseñaron el andamiaje químico para establecer contactos más fuertes con dos aminoácidos cargados negativamente (D408 y E947) situados a lo largo de la vía por la que la bomba normalmente mueve protones. Al añadir una cadena lateral benzilamina cuidadosamente posicionada, crearon un nuevo compuesto, BDM91531, que se une aproximadamente cincuenta veces con mayor afinidad que su predecesor y potencia la actividad de múltiples antibióticos a concentraciones muy bajas.
Congelando la bomba a mitad de ciclo
La cristalografía de rayos X y la criomicroscopía electrónica de partículas individuales mostraron exactamente cómo BDM91531 desactiva la bomba. El compuesto se sitúa en una cavidad alargada entre varias hélices transmembrana dentro de una subunidad de AcrB. Dado que BDM91531 porta dos cargas positivas, forma fuertes puentes salinos con D408, en lo profundo del bolsillo, y con E947, cerca del borde citoplasmático. Estos dos puntos de contacto suspenden el inhibidor como un puente entre la pared interna de la bomba y el interior celular. Bloqueado en esa posición, el compuesto atrapa esa subunidad en un estado intermedio entre las conformaciones abierta y la floja—el tipo de forma transitoria por la que la bomba normalmente sólo pasa brevemente. Puesto que las tres subunidades deben rotar por sus estados de forma sincronizada, congelar una de ellas detiene toda la máquina y paraliza el eflujo de fármacos.
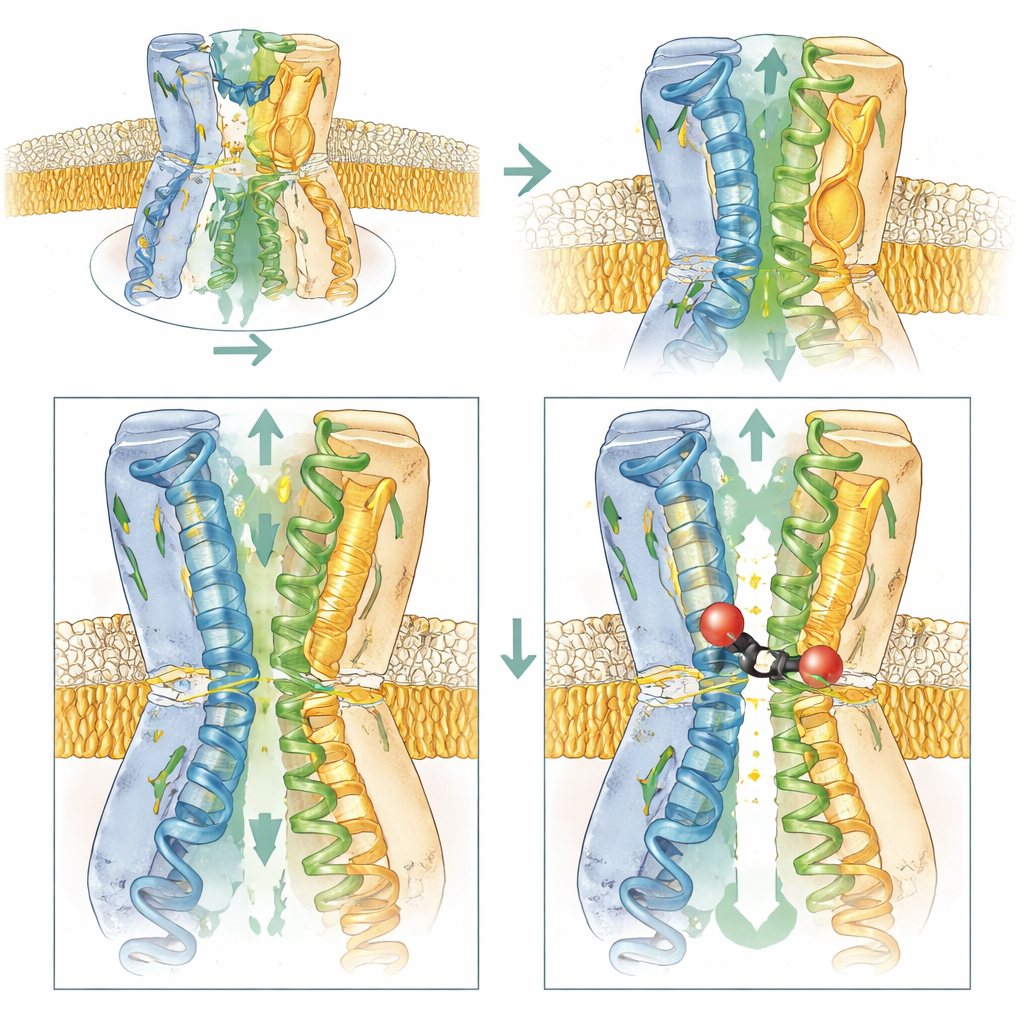
Cargando la entrada para atraer el inhibidor
El equipo combinó mediciones biofísicas, pruebas de crecimiento bacteriano y simulaciones por ordenador para sondear qué partes de AcrB son más importantes para la acción de BDM91531. Eliminar la carga negativa en D408 eliminó por completo la unión, confirmando su papel central. Alterar E947 o un residuo ácido cercano, D951, hizo a las bacterias menos sensibles al inhibidor, mientras que la reintroducción de cargas negativas en posiciones vecinas restauró o incluso aumentó la sensibilidad. Esto muestra que, además de servir como puntos de anclaje, estos residuos ácidos ayudan a atraer el inhibidor cargado positivamente desde el citoplasma hacia la ranura de entrada del bolsillo de unión. En contraste, cambios que eliminaban estas cargas o hacían la zona de entrada más neutra redujeron tanto el acceso como la unión.
Revivir los antibióticos atacando el movimiento, no el fármaco
En términos cotidianos, BDM91531 funciona atascando una pieza móvil de la bomba bacteriana en el momento justo, impidiendo que la máquina complete su ciclo y atrapando los antibióticos dentro de la célula donde pueden hacer efecto. Dado que el inhibidor no mata a las bacterias por sí mismo a las dosis necesarias para bloquear la bomba, debe verse mejor como un potenciador que se combina con fármacos existentes. Las ideas estructurales y mecanicistas derivadas de este trabajo señalan con precisión qué características de la bomba deben dirigirse para diseñar bloqueadores aún mejores, abriendo la posibilidad de nuevas terapias adyuvantes que restauren el poder de los antibióticos contra algunas de nuestras infecciones más persistentes.
Cita: Börnsen, C., Müller, R.T., Vieira Da Cruz, A. et al. Molecular mechanism of transition-state inhibitors of bacterial antibiotic efflux pumps. npj Antimicrob Resist 4, 35 (2026). https://doi.org/10.1038/s44259-026-00207-6
Palabras clave: resistencia a antibióticos, inhibidor de bomba de eflujo, AcrB, bacterias Gram negativas, diseño de fármacos basado en estructura