Clear Sky Science · nl
Moleculair mechanisme van remmers die de overgangstoestand van bacteriële antibiotica-effluxpompen blokkeren
Waarom het stoppen van bacteriële "pompen" antibiotica kan redden
Antibioticaresistentie ontstaat vaak niet omdat geneesmiddelen hun doelwit niet bereiken, maar omdat bacteriën ze actief weer naar buiten pompen. Deze studie onthult, tot op atomaire detailniveau, hoe een nieuw ontworpen verbinding een belangrijke bacteriële pomp blokkeert en bestaande antibiotica weer effectief maakt. Inzicht in hoe deze moleculaire "wig" werkt, kan de weg openen naar combinatietherapieën die medicijnen nieuw leven inblazen die we dreigen te verliezen.
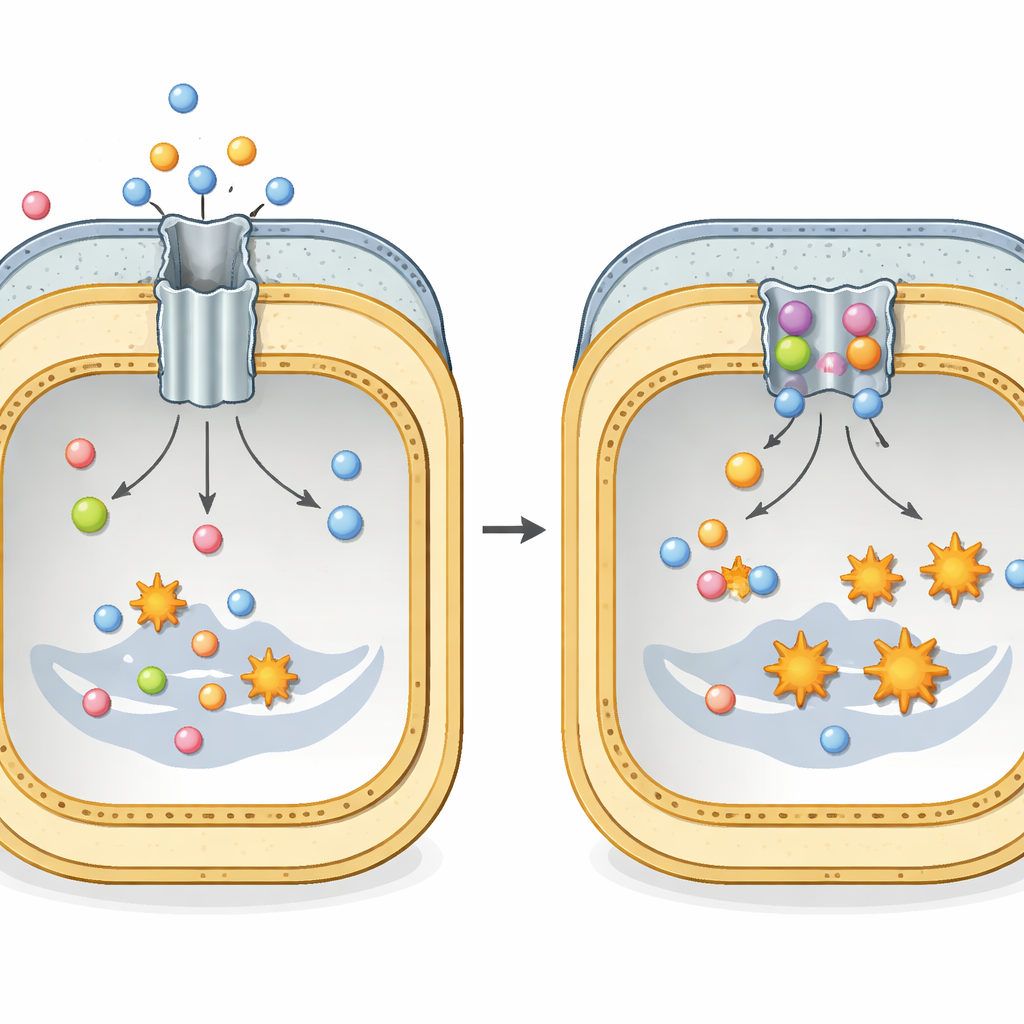
Een verborgen ontsnappingstunnel voor antibiotica
Veel gevaarlijke Gram-negatieve bacteriën, zoals Escherichia coli en Klebsiella pneumoniae, vertrouwen op een groot proteïnecomplex genaamd AcrAB–TolC om antibiotische behandeling te overleven. Dit complex overspant de volledige celomhulling en werkt als een tunnel met een motor aan de binnenkant. Het deel in het binnenmembraan, AcrB genoemd, herkent een breed scala aan geneesmiddelen en andere toxische stoffen en gebruikt cellulaire energie om ze naar buiten te werpen. Elk AcrB-eenheid is opgebouwd uit drie herhalende delen die voortdurend door drie vormen heen cycleren—losjes gebonden, strak gebonden en open naar buiten—waardoor een peristaltische beweging ontstaat die antibiotica wegduwt voordat ze blijvende schade kunnen aanrichten.
Ontwerpen van een slimmere moleculaire wig
Geneesmiddelontwikkelaars hebben al lang geprobeerd deze pomp te blokkeren, maar de meeste eerdere remmers binden in een grote vette holte die ook veel andere moleculen aantrekt, wat leidt tot slechte oplosbaarheid en bijwerkingen. Voortbouwend op eerder werk richtten de auteurs zich in plaats daarvan op een nieuwere familie verbindingen, pyridylpiperazines, die zitten in een meer gespecialiseerde regio diep in het membraanoverspannende deel van AcrB. Geleid door hoogresolutie-structurele gegevens herontwierpen ze het chemische skelet om sterkere contacten te maken met twee negatief geladen aminozuren (D408 en E947) die langs het pad liggen waarlangs de pomp normaal protonen verplaatst. Door een zorgvuldig gepositioneerde benzylamine-zijketen toe te voegen, creëerden ze een nieuwe verbinding, BDM91531, die ongeveer vijftig keer sterker bindt dan zijn voorganger en de werkzaamheid van meerdere antibiotica verhoogt bij zeer lage concentraties.
De pomp halverwege de slag bevriezen
X-ray kristallografie en single-particle cryo-elektronenmicroscopie toonden precies aan hoe BDM91531 de pomp uitschakelt. De verbinding ligt in een langwerpige holte tussen meerdere membraanoverspannende helices binnen één AcrB-subunit. Omdat BDM91531 twee positieve ladingen draagt, vormt het sterke zoutbruggen met D408 diep in de holte en E947 nabij de cytoplasmatische rand. Deze twee contactpunten hangen de remmer op als een brug tussen de binnenwand van de pomp en het celinterieur. Vastgezet op zijn plaats houdt de verbinding die subunit gevangen in een tussenstaat tussen de open en de losse conformaties—het soort tijdelijke vorm dat de pomp normaal slechts kort aanneemt. Omdat de drie subunits hun toestanden gesynchroniseerd moeten doorlopen, legt het bevriezen van één van hen de hele machine stil en stopt het de efflux van geneesmiddelen.
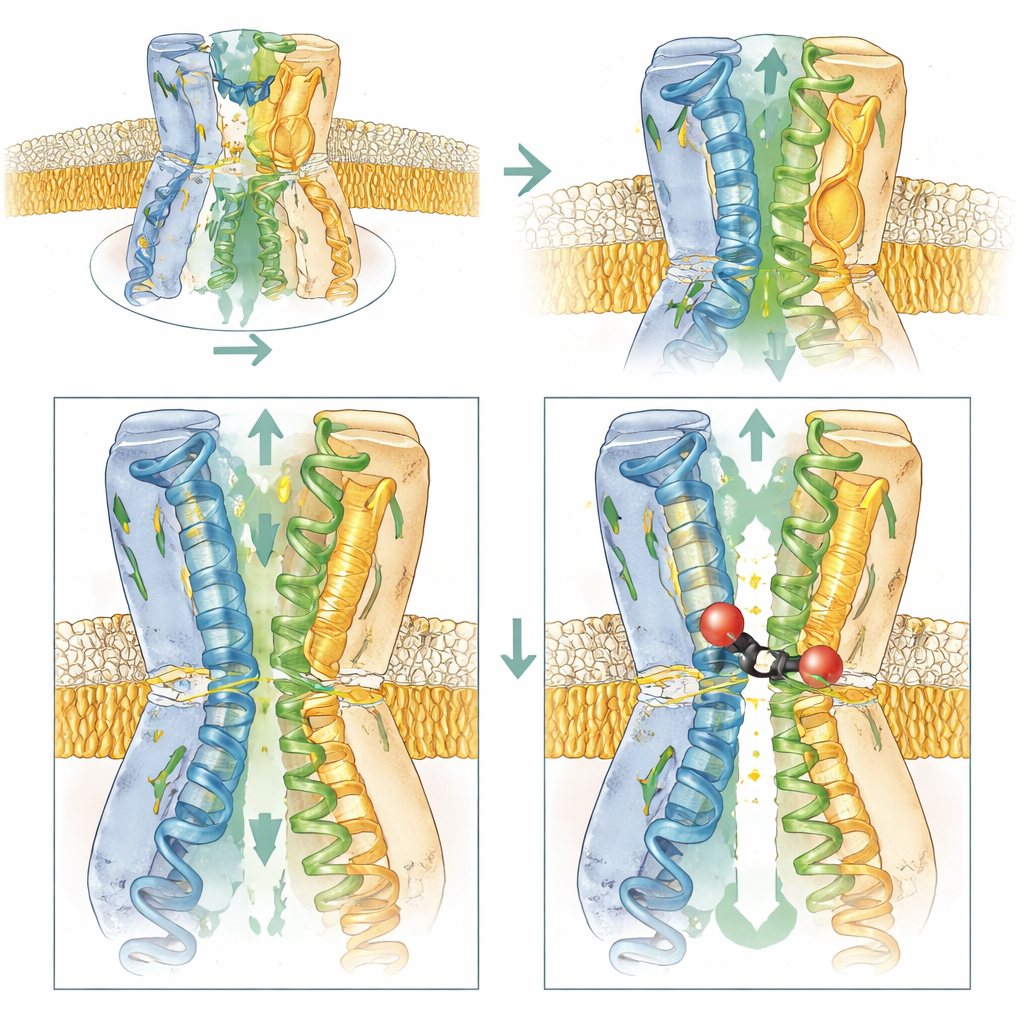
De doorgang opladen om de remmer naar binnen te trekken
Het team combineerde biofysische metingen, groeiproeven met bacteriën en computersimulaties om te onderzoeken welke delen van AcrB het belangrijkst zijn voor de werking van BDM91531. Het verwijderen van de negatieve lading bij D408 maakte binding volledig onmogelijk, wat de centrale rol daarvan bevestigt. Veranderingen aan E947 of een nabijgelegen zuur residu, D951, maakten bacteriën minder gevoelig voor de remmer, terwijl het herintroduceren van negatieve ladingen op aangrenzende posities de gevoeligheid herstelde of zelfs versterkte. Dit toont aan dat deze zure residuen, naast het dienen als ankerpunten, helpen de positief geladen remmer uit het cytoplasma naar de toegangsgroef van het bindingspocket aan te trekken. Daarentegen verminderden veranderingen die deze ladingen verwijderden of de toegangzone neutraler maakten zowel de toegang als de binding.
Antibiotica nieuw leven inblazen door beweging te richten, niet het medicijn
In gewone bewoordingen werkt BDM91531 door een bewegend onderdeel van een bacteriële pomp op precies het juiste moment vast te zetten, waardoor de machine de cyclus niet kan voltooien en antibiotica in de cel gevangen blijven waar ze effect kunnen hebben. Omdat de remmer op zichzelf de bacteriën niet doodt bij de dosis die nodig is om de pomp te blokkeren, moet hij het best worden gezien als een versterker die gecombineerd wordt met bestaande geneesmiddelen. De structurele en mechanistische inzichten uit dit werk geven precies aan welke kenmerken van de pomp moeten worden gericht om nog betere blokkers te ontwerpen, en vergroten het vooruitzicht op nieuwe adjuvante therapieën die de kracht van antibiotica herstellen tegen enkele van onze hardnekkigste infecties.
Bronvermelding: Börnsen, C., Müller, R.T., Vieira Da Cruz, A. et al. Molecular mechanism of transition-state inhibitors of bacterial antibiotic efflux pumps. npj Antimicrob Resist 4, 35 (2026). https://doi.org/10.1038/s44259-026-00207-6
Trefwoorden: antibioticaresistentie, remmer van effluxpomp, AcrB, Gram-negatieve bacteriën, structuurgebaseerde geneesmiddelontwerp