Clear Sky Science · ru
Молекулярный механизм ингибиторов переходного состояния бактериальных насосов выведения антибиотиков
Почему остановка бактериальных «насосов» может спасти антибиотики
Резистентность к антибиотикам часто возникает не потому, что препараты не достигают своих мишеней, а потому, что бактерии активно выталкивают их обратно. В этом исследовании показано с атомной точностью, как недавно разработанное соединение заклинивает крупный бактериальный насос и восстанавливает эффективность существующих антибиотиков. Понимание того, как работает эта молекулярная «клин», может открыть дорогу комбинационным терапиям, которые вернут силу лекарствам, которые мы можем потерять.
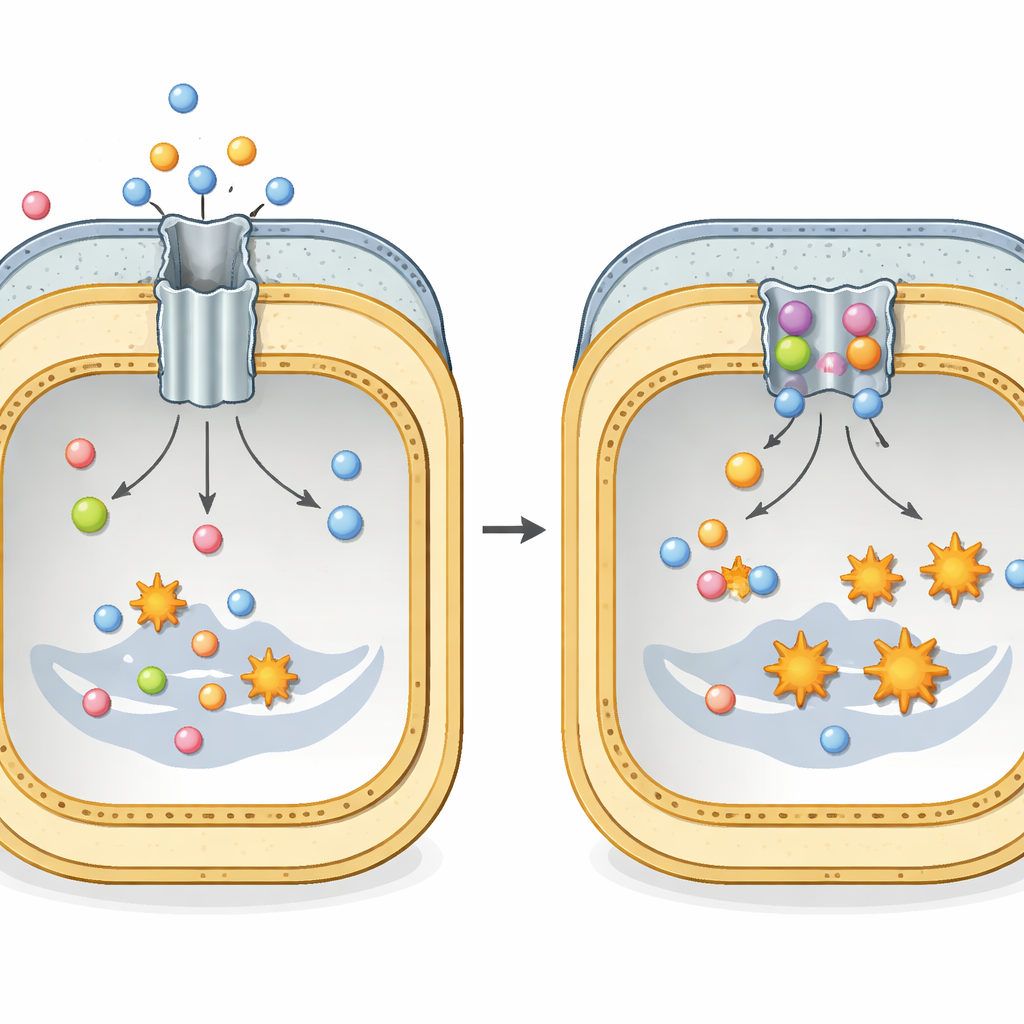
Скрытый туннель для выхода антибиотиков
Многие опасные грам-отрицательные бактерии, такие как Escherichia coli и Klebsiella pneumoniae, зависят от крупного белкового комплекса AcrAB–TolC для выживания при лечении антибиотиками. Этот комплекс проходит через всю оболочку клетки и работает как туннель с мотором на внутреннем конце. Часть во внутренней мембране, называемая AcrB, распознаёт широкий спектр препаратов и других токсичных молекул и использует энергию клетки, чтобы выталкивать их наружу. Каждая единица AcrB состоит из трёх повторяющихся частей, которые постоянно циклично меняют три формы — слабо связанная, плотно связанная и открытая наружу — создавая перистальтическое движение, которое выталкивает антибиотики прежде, чем те успеют нанести длительный вред.
Проектирование более умного молекулярного клина
Разработчики лекарств давно пытались блокировать этот насос, но большинство ранних ингибиторов связывались в большой жирной карманной области, которая также притягивает многие другие молекулы, что приводило к плохой растворимости и побочным эффектам. Опираясь на предыдущие работы, авторы сосредоточились на более новой семействе соединений — пиридилпиперазинах, которые встраиваются в более специализированную область глубоко в мембранной части AcrB. Руководствуясь данными высокоразрешающей структуры, они переработали химический остов, чтобы усилить контакты с двумя отрицательно заряженными аминокислотами (D408 и E947), расположенными вдоль пути, по которому насос обычно перемещает протоны. Добавив тщательно размещённую бензиламиновую боковую цепь, они создали новое соединение BDM91531, которое связывается примерно в пятьдесят раз сильнее предшественника и усиливает действие нескольких антибиотиков при очень низких концентрациях.
Замораживание насоса в середине хода
Рентгеноструктурный анализ и крио–электронная микроскопия отдельных частиц показали, как именно BDM91531 дезактивирует насос. Соединение располагается в удлинённой полости между несколькими спиралями, пересекающими мембрану, внутри одного субъединицы AcrB. Поскольку BDM91531 несёт два положительных заряда, оно образует прочные солевые мостики с D408 глубоко в кармане и с E947 у цитоплазматического края. Эти две точки контакта подвешивают ингибитор как мост между внутренней стенкой насоса и интерьером клетки. Закреплённый таким образом, соединение удерживает эту субъединицу в промежуточном состоянии между открытой и слабо связанной конформациями — в той кратковременной форме, через которую насос обычно проходит очень быстро. Поскольку три субъединицы должны синхронно сменять свои состояния, блокировка одной из них останавливает всю машину и прекращает выведение препаратов.
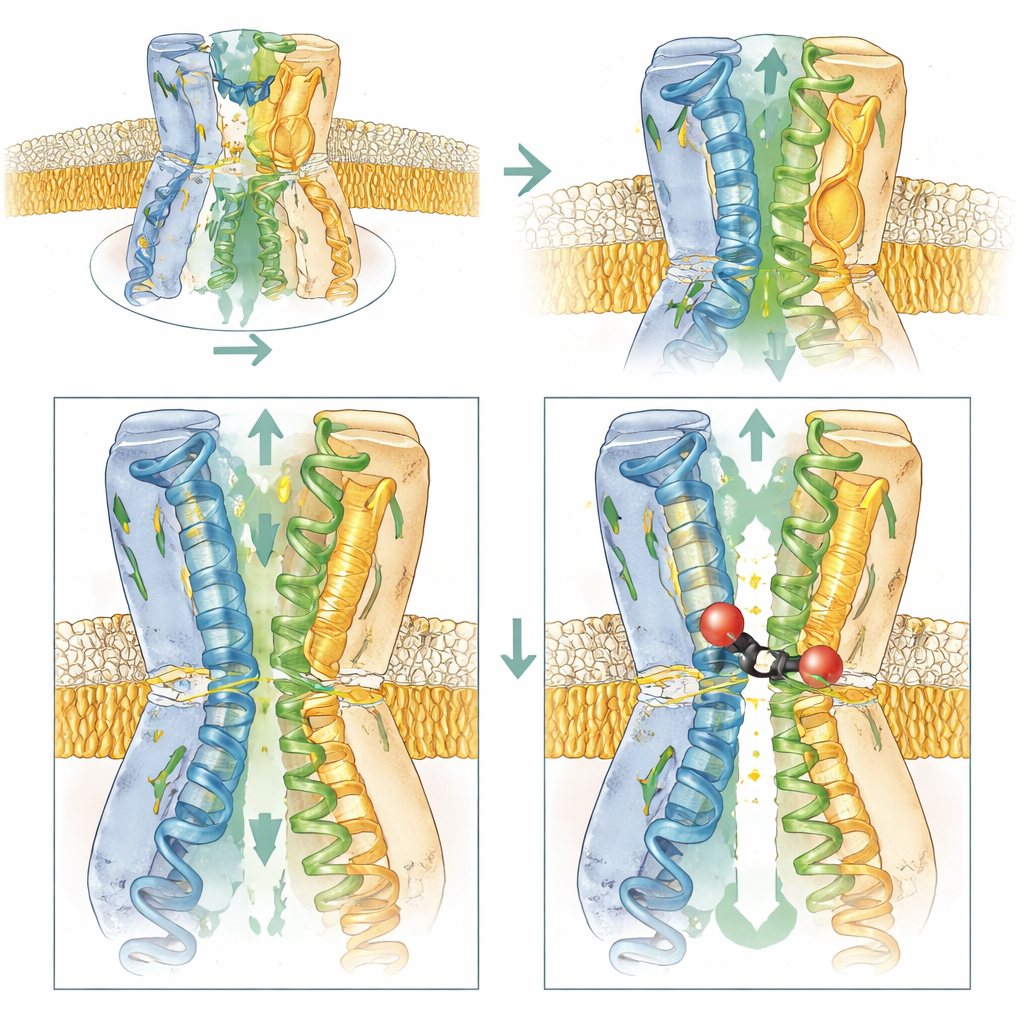
Заряжая вход, чтобы втянуть ингибитор
Команда совместила биофизические измерения, тесты роста бактерий и компьютерное моделирование, чтобы выяснить, какие части AcrB наиболее важны для действия BDM91531. Удаление отрицательного заряда в D408 полностью устраняло связывание, подтверждая его ключевую роль. Модификация E947 или соседнего кислого остатка D951 делала бактерии менее чувствительными к ингибитору, тогда как восстановление отрицательных зарядов в соседних позициях возвращало или даже усиливало чувствительность. Это показывает, что помимо роли анкеров эти кислые остатки помогают притягивать положительно заряженный ингибитор из цитоплазмы в входную борозду связывающего кармана. Напротив, изменения, убирающие эти заряды или делавшие зону входа более нейтральной, снижали как доступ, так и связывание.
Возрождение антибиотиков путём воздействия на движение, а не на препарат
Проще говоря, BDM91531 действует, заклинивая движущуюся часть бактериального насоса в нужный момент, предотвращая завершение рабочего цикла и удерживая антибиотики внутри клетки, где они могут подействовать. Поскольку ингибитор сам по себе при дозах, необходимых для блокировки насоса, не убивает бактерии, его лучше рассматривать как усилитель, который следует комбинировать с существующими препаратами. Структурные и механистические выводы этой работы указывают, какие именно особенности насоса следует целить при разработке ещё более эффективных блокаторов, создавая перспективу адъювантных терапий, которые восстановят силу антибиотиков против некоторых из самых упорных инфекций.
Цитирование: Börnsen, C., Müller, R.T., Vieira Da Cruz, A. et al. Molecular mechanism of transition-state inhibitors of bacterial antibiotic efflux pumps. npj Antimicrob Resist 4, 35 (2026). https://doi.org/10.1038/s44259-026-00207-6
Ключевые слова: резистентность к антибиотикам, ингибитор насосов выведения, AcrB, грам-отрицательные бактерии, дизайн лекарств на основе структуры