Clear Sky Science · pl
Molekularny mechanizm inhibitorów stanu przejściowego pomp wypompowujących antybiotyki u bakterii
Dlaczego zatrzymanie „pomp” bakteryjnych może uratować antybiotyki
Oporność na antybiotyki często wynika nie z tego, że leki nie trafiają w swoje cele, lecz z tego, że bakterie aktywnie je wypompowują. To badanie odsłania, z dokładnością atomową, jak nowo zaprojektowany związek blokuje dużą bakteryjną pompę i przywraca skuteczność istniejących antybiotyków. Zrozumienie, jak działa ta molekularna „klin”, może otworzyć drogę do terapii skojarzonych, które przywrócą leki, o które możemy w przeciwnym razie zostać pozbawieni.
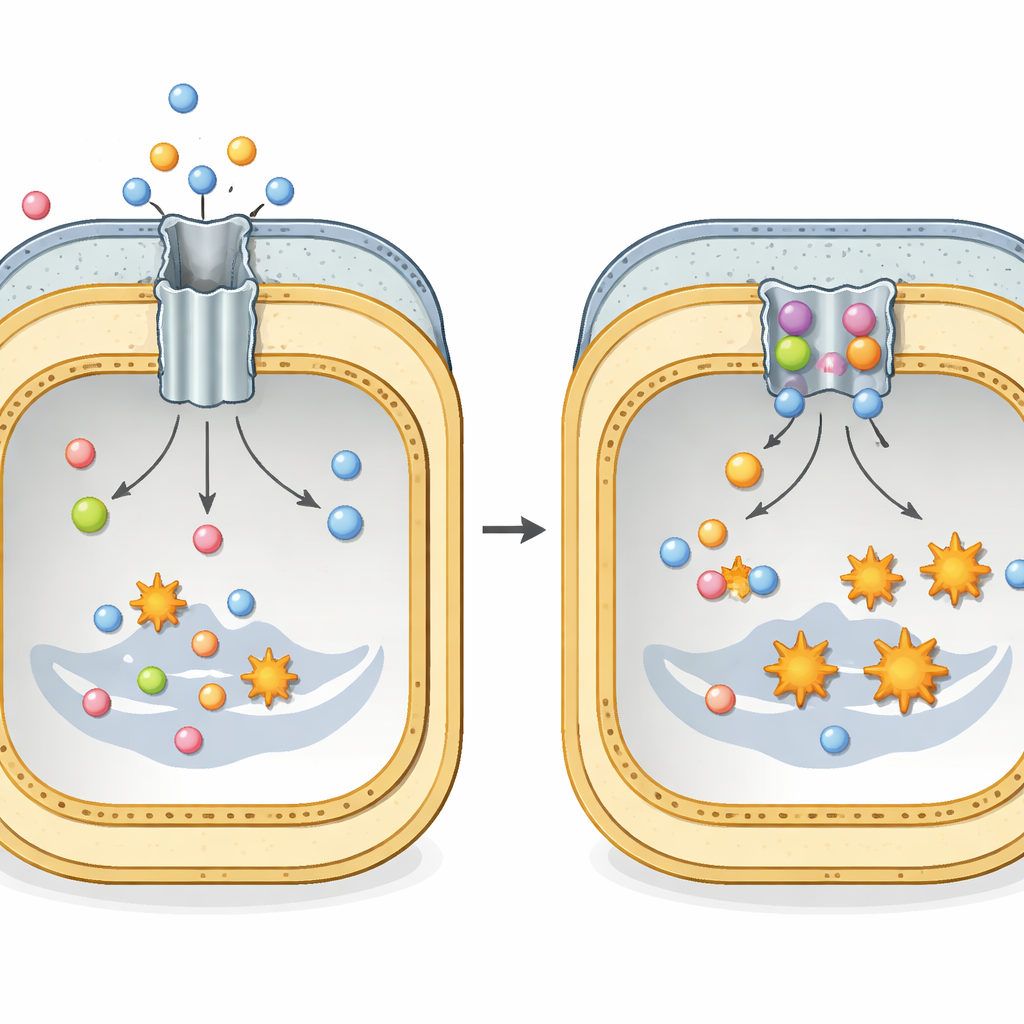
Ukryty tunel ucieczki dla antybiotyków
Wiele groźnych bakterii Gram-ujemnych, takich jak Escherichia coli i Klebsiella pneumoniae, polega na dużym kompleksie białkowym zwanym AcrAB–TolC, by przetrwać terapię antybiotykową. Kompleks ten rozciąga się przez całą otoczkę komórkową i działa jak tunel z silnikiem na jego wewnętrznym końcu. Część wewnętrznej błony, nazwana AcrB, rozpoznaje szeroką gamę leków i innych toksycznych cząsteczek oraz wykorzystuje energię komórkową do ich wyrzucenia na zewnątrz. Każda jednostka AcrB składa się z trzech powtarzających się elementów, które nieustannie przechodzą przez trzy kształty — luźne, ściśle związane i otwarte na zewnątrz — tworząc perystaltyczny ruch, który wypycha antybiotyki zanim zdążą wyrządzić trwałe szkody.
Projektowanie mądrzejszego molekularnego klina
Twórcy leków od dawna próbowali zablokować tę pompę, ale większość wcześniejszych inhibitorów wiązała się w dużym tłustym kieszeni, która przyciągała też wiele innych cząsteczek, prowadząc do słabej rozpuszczalności i skutków ubocznych. Budując na wcześniejszych pracach, autorzy skupili się zamiast tego na nowszej rodzinie związków zwanych pyridylopiperazynami, które osadzają się w bardziej wyspecjalizowanym regionie głęboko w części AcrB przechodzącej przez błonę. Kierowani danymi strukturalnymi o wysokiej rozdzielczości, przeprojektowali szkielet chemiczny, aby wzmocnić kontakty z dwoma ujemnie naładowanymi aminokwasami (D408 i E947) położonymi wzdłuż ścieżki, po której pompa zwykle przesuwa protony. Dodając starannie umieszczony łańcuch boczny benzylaminy, stworzyli nowy związek, BDM91531, który wiąże się około pięćdziesiąt razy silniej niż jego poprzednik i zwiększa aktywność wielu antybiotyków przy bardzo niskich stężeniach.
Zamrażanie pompy w połowie skoku
Kryształografia rentgenowska i krioelektronowa mikroskopia pojedynczych cząstek wykazały dokładnie, jak BDM91531 unieruchamia pompę. Związek siedzi w wydłużonej wnęce między kilkoma helisami przechodzącymi przez błonę wewnątrz jednej podjednostki AcrB. Ponieważ BDM91531 niesie ze sobą dwa ładunki dodatnie, tworzy silne mostki solne z D408 głęboko w kieszeni oraz z E947 blisko brzeżnej strony cytoplazmatycznej. Te dwa punkty kontaktu zawieszają inhibitor jak most między wewnętrzną ścianą pompy a wnętrzem komórki. Zablokowany w tym miejscu, związek unieruchamia tę podjednostkę w stanie pośrednim między konformacjami otwartą i luźną — w takim krótkotrwałym kształcie, przez który pompa normalnie przechodzi tylko na chwilę. Ponieważ trzy podjednostki muszą rotować przez swoje stany w zsynchronizowany sposób, zablokowanie jednej z nich zatrzymuje całą maszynę i przerywa wypompowywanie leków.
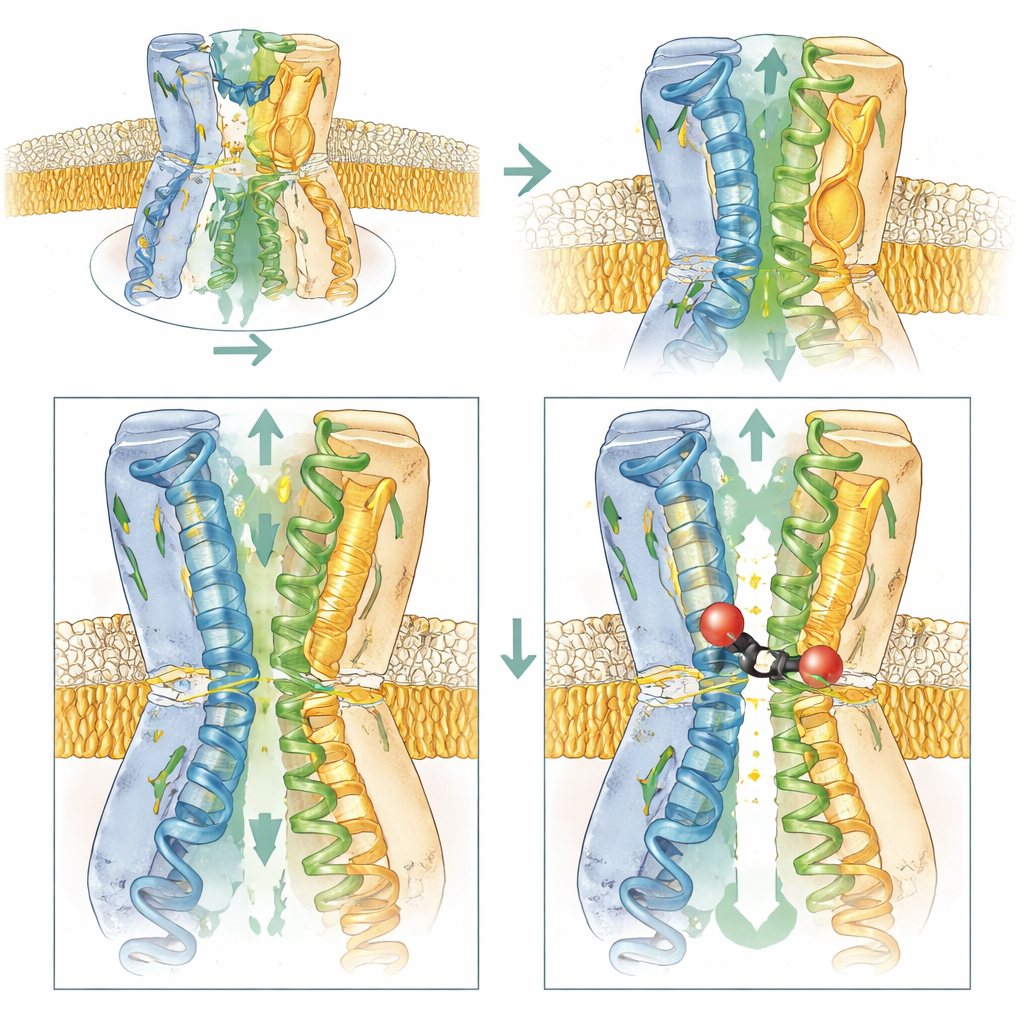
Nabicie wejścia, by wciągnąć inhibitor
Zespół połączył pomiary biofizyczne, testy wzrostu bakterii i symulacje komputerowe, aby sprawdzić, które części AcrB są najważniejsze dla działania BDM91531. Usunięcie ładunku ujemnego w D408 całkowicie eliminowało wiązanie, potwierdzając jego kluczową rolę. Zmiany w E947 lub pobliskim reszcie kwaśnej, D951, zmniejszały wrażliwość bakterii na inhibitor, podczas gdy ponowne wprowadzenie ładunków ujemnych w sąsiednich pozycjach przywracało lub nawet zwiększało wrażliwość. Pokazuje to, że poza pełnieniem roli punktów kotwiczenia, te reszty kwaśne pomagają przyciągać dodatnio naładowany inhibitor z cytoplazmy do wejściowego rowka kieszeni wiążącej. Natomiast zmiany usuwające te ładunki lub czyniące strefę wejściową bardziej obojętną zmniejszały zarówno dostęp, jak i wiązanie.
Przywracanie skuteczności antybiotyków poprzez celowanie w ruch, a nie w lek
Mówiąc obrazowo, BDM91531 działa poprzez zablokowanie ruchomej części pompy bakteryjnej w odpowiednim momencie, uniemożliwiając maszynie dokończenie cyklu i zatrzymując antybiotyki wewnątrz komórki, gdzie mogą zadziałać. Ponieważ inhibitor sam w sobie nie zabija bakterii w dawkach wymaganych do zablokowania pompy, powinien być rozumiany raczej jako wzmacniacz do stosowania w połączeniu z istniejącymi lekami. Wnikliwe informacje strukturalne i mechanistyczne z tej pracy wskazują dokładnie, które cechy pompy należy celować, aby zaprojektować jeszcze lepsze blokery, co zwiększa perspektywę nowych terapii adiuwantowych przywracających moc antybiotyków przeciwko niektórym z naszych najbardziej opornych zakażeń.
Cytowanie: Börnsen, C., Müller, R.T., Vieira Da Cruz, A. et al. Molecular mechanism of transition-state inhibitors of bacterial antibiotic efflux pumps. npj Antimicrob Resist 4, 35 (2026). https://doi.org/10.1038/s44259-026-00207-6
Słowa kluczowe: oporność na antybiotyki, inhibitor pompy wypompowującej, AcrB, bakterie Gram-ujemne, projektowanie leków w oparciu o strukturę