Clear Sky Science · tr
Bakteriyal antibiyotik dışarı atım pompalarının geçiş-durumu inhibitörlerinin moleküler mekanizması
Bakteri "pompalarını" durdurmak neden antibiyotikleri kurtarabilir?
Antibiyotik direnci sıklıkla ilaçların hedeflerini vuramamasından değil, bakterilerin ilaçları aktif olarak dışarı pompalamasından kaynaklanır. Bu çalışma, atomik ayrıntıda, yeni tasarlanmış bir bileşiğin büyük bir bakteri pompasını nasıl kilitlediğini ve mevcut antibiyotikleri yeniden etkili hâle getirdiğini ortaya koyuyor. Bu moleküler "takoz"un nasıl çalıştığını anlamak, kaybetme tehlikesiyle karşı karşıya olduğumuz ilaçları canlandıracak kombinasyon terapilerine kapı açabilir.
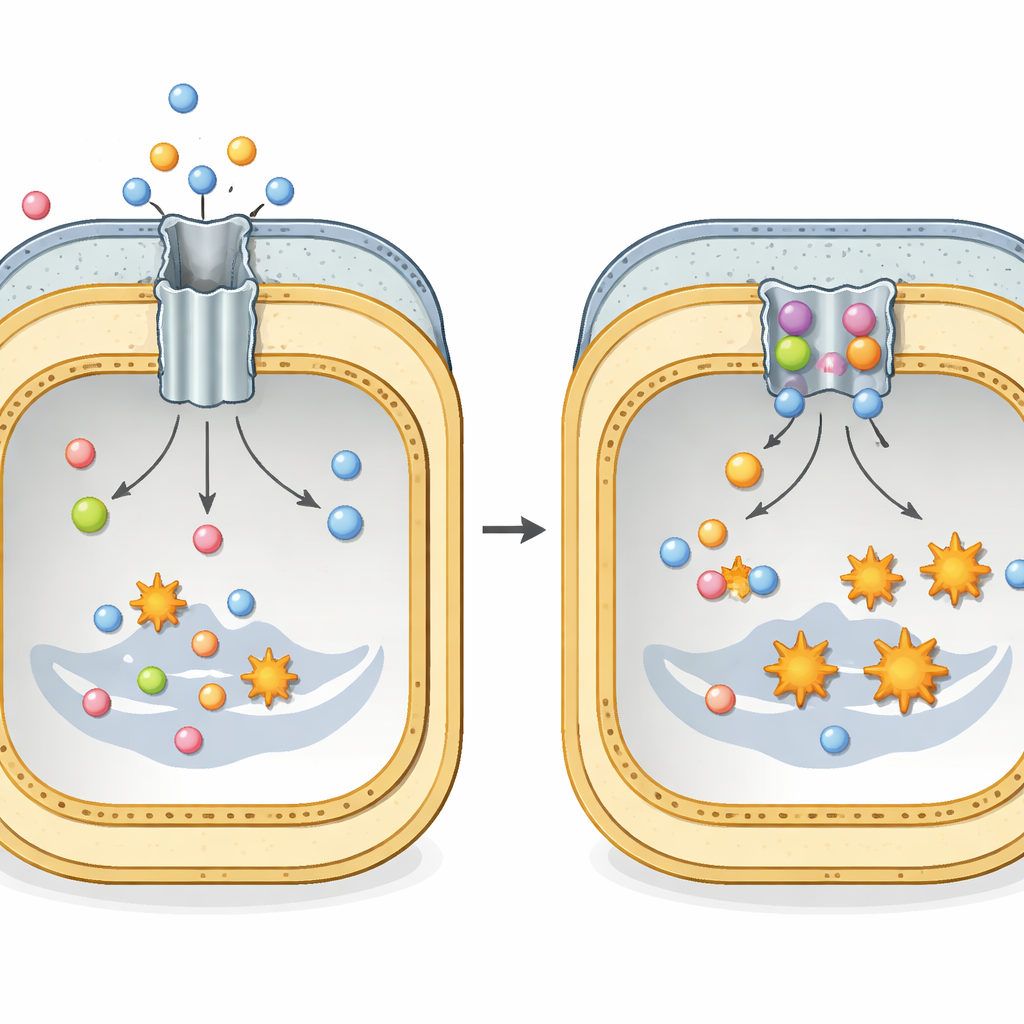
Antibiyotikler için gizli bir kaçış tüneli
Escherichia coli ve Klebsiella pneumoniae gibi birçok tehlikeli Gram-negatif bakteri, antibiyotik tedavisine direnmek için AcrAB–TolC adı verilen büyük bir protein bileşimine güvenir. Bu yapı tüm hücre zarfına yayılır ve iç ucunda bir motor bulunan bir tünel gibi çalışır. İç zar kısmı olan AcrB, çok çeşitli ilaçları ve diğer zehirli molekülleri tanır ve bunları hücresel enerji kullanarak dışarı atar. Her AcrB ünitesi, gevşek bağlanmış, sıkı bağlanmış ve dışa açık olmak üzere üç şekil arasında sürekli dönen üç tekrarlayan parçadan oluşur; bu da antibiyotikleri kalıcı zarar vermeden önce dışarı iten bir peristaltik hareket yaratır.
Daha akıllı bir moleküler takoz tasarlamak
İlaç geliştiriciler uzun zamandır bu pompayı engellemeye çalıştı, ancak önceki çoğu inhibitör, birçok başka molekülü de çeken büyük yağlı bir ceple bağlanıyordu; bu da zayıf çözünürlük ve yan etkilere yol açtı. Önceki çalışmalardan yola çıkarak yazarlar, bunun yerine AcrB'nin zar boyunca uzanan kısmının derin, daha özelleşmiş bir bölgesine yerleşen piridilpiperazinler adlı yeni bir bileşik ailesine odaklandı. Yüksek çözünürlüklü yapısal veriler yol göstericiliğinde kimyasal iskeleti, pompanın normalde protonları taşıdığı yol boyunca yer alan iki negatif yüklü amino asit (D408 ve E947) ile daha güçlü temaslar kuracak şekilde yeniden tasarladılar. Dikkatle yerleştirilmiş bir benzilamin yan zinciri ekleyerek, selefinden yaklaşık elli kat daha sıkı bağlanan ve çok düşük konsantrasyonlarda birden fazla antibiyotiğin etkinliğini artıran yeni bir bileşik, BDM91531, yarattılar.
Pompayı hareketin ortasında dondurmak
X-ışını kristalografisi ve tek parçacıklı kriyo-elektron mikroskobu, BDM91531'in pompayı nasıl devre dışı bıraktığını tam olarak gösterdi. Bileşik, bir AcrB alt biriminin içindeki birkaç zar geçiş heliksi arasında uzanan uzun bir boşlukta yer alır. BDM91531 iki pozitif yük taşıdığından, cephenin derinliklerindeki D408 ve sitoplazmik kenara yakın E947 ile güçlü tuz köprüleri oluşturur. Bu iki temas noktası inhibitörü pompanın iç duvarı ile hücre içi arasında bir köprü gibi asılı tutar. Yerine kilitlendiğinde, bileşik o alt birimi açık ve gevşek konformasyonlar arasındaki yarı yolda—pompanın normalde yalnızca kısa süreliğine geçtiği geçici bir şekil—tuzaklar. Üç alt birimin durumları senkronize biçimde dönmek zorunda olduğundan, bunlardan birini dondurmak tüm makineyi durdurur ve ilaç dışarı atımını keser.
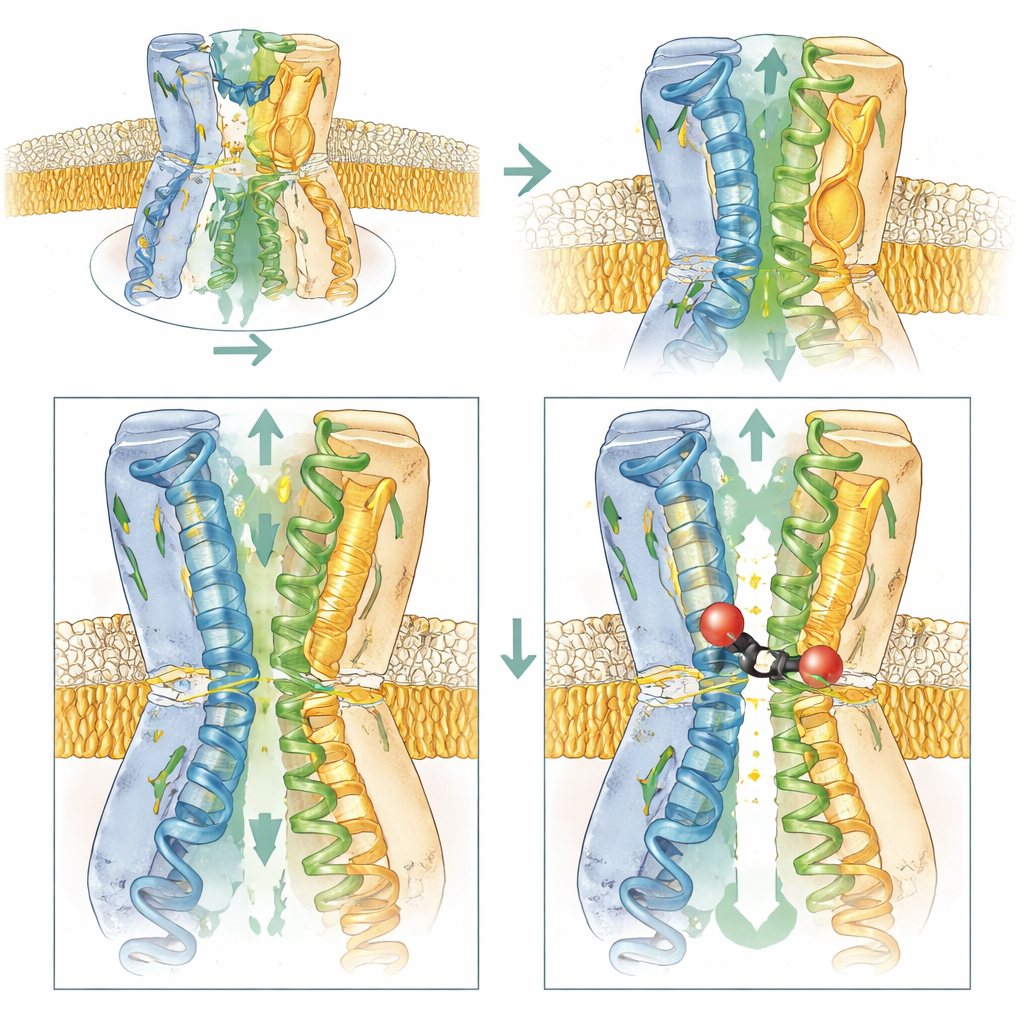
İnhibitörü çekmek için kapının şarj edilmesi
Araştırma ekibi, hangi AcrB parçalarının BDM91531’in etkisi için en önemli olduğunu araştırmak üzere biyofiziksel ölçümleri, bakteri büyüme testlerini ve bilgisayar simülasyonlarını birleştirdi. D408’deki negatif yükün kaldırılması bağlanmayı tamamen ortadan kaldırdı ve bunun merkezi rolünü doğruladı. E947 veya yakındaki asidik bir kalıntı olan D951'in değiştirilmesi bakterilerin inhibitöre duyarlılığını azalttı; komşu pozisyonlara negatif yüklerin yeniden getirilmesi ise duyarlılığı geri getirdi veya hatta artırdı. Bu, bu asidik kalıntıların bağlayıcı noktalardan öte, pozitif yüklü inhibitörü sitoplazmadan bağlanma cepleri giriş oluğuna çekmeye yardımcı olduğunu gösterir. Buna karşılık, bu yükleri kaldıran veya giriş bölgesini daha nötr hâle getiren değişiklikler hem erişimi hem de bağlanmayı azalttı.
Hareketi hedefleyerek, ilacı değil, antibiyotikleri canlandırmak
Günlük ifadeyle, BDM91531 bir bakteri pompasının hareketli parçasını tam doğru anda tıkayarak makinenin döngüsünü tamamlamasını engeller ve antibiyotikleri hücre içinde etkili olabilecekleri yerde hapseder. İnhibitör, pompayı bloke etmek için gereken dozlarda tek başına bakterileri öldürmediği için, mevcut ilaçlarla birlikte kullanılacak bir güçlendirici olarak değerlendirilmelidir. Bu çalışmadan elde edilen yapısal ve mekanistik içgörüler, pompanın hangi özelliklerinin daha iyi engelleyiciler tasarlamak için hedeflenmesi gerektiğini net biçimde ortaya koyuyor ve bazı inatçı enfeksiyonlara karşı antibiyotiklerin etkisini geri getirebilecek yeni yardımcı tedaviler olasılığını artırıyor.
Atıf: Börnsen, C., Müller, R.T., Vieira Da Cruz, A. et al. Molecular mechanism of transition-state inhibitors of bacterial antibiotic efflux pumps. npj Antimicrob Resist 4, 35 (2026). https://doi.org/10.1038/s44259-026-00207-6
Anahtar kelimeler: antibiyotik direnci, efluks pompa inhibitörü, AcrB, Gram-negatif bakteriler, yapı-temelli ilaç tasarımı