Clear Sky Science · it
Meccanismo molecolare degli inibitori dello stato di transizione delle pompe di efflusso batteriche
Perché fermare le “pompe” batteriche potrebbe salvare gli antibiotici
La resistenza agli antibiotici spesso non nasce perché i farmaci non colpiscono i loro bersagli, ma perché i batteri li espellono attivamente. Questo studio rivela, a livello atomico, come un composto di nuova concezione inceppi una pompa batterica di primo piano e renda di nuovo potenti antibiotici già esistenti. Comprendere come funziona questa “cuneo” molecolare potrebbe aprire la strada a terapie combinate in grado di rivitalizzare medicinali che rischiamo di perdere.
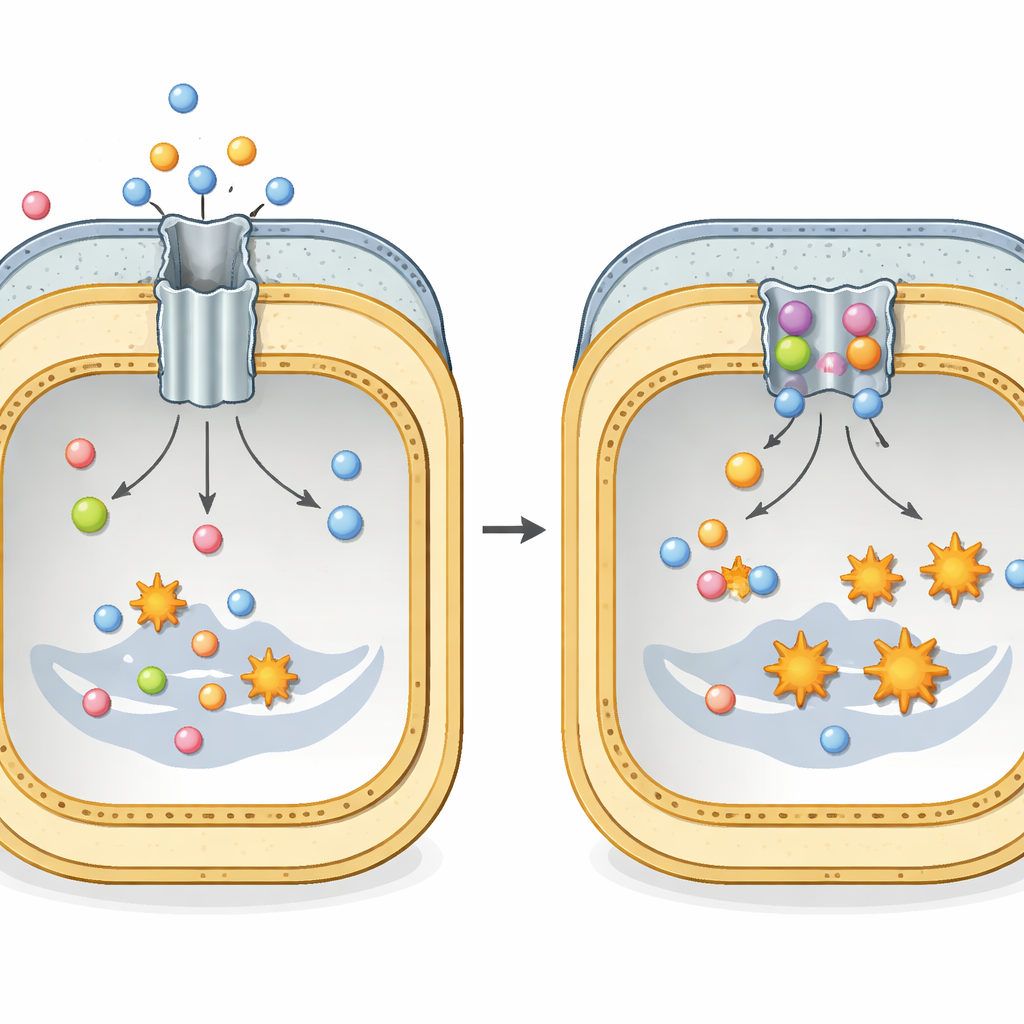
Un tunnel nascosto di fuga per gli antibiotici
Molti pericolosi batteri Gram-negativi, come Escherichia coli e Klebsiella pneumoniae, dipendono da un grande assemblaggio proteico chiamato AcrAB–TolC per sopravvivere al trattamento con antibiotici. Questo complesso attraversa tutto l’involucro cellulare e funziona come un tunnel con un motore alla sua estremità interna. La parte della membrana interna, chiamata AcrB, riconosce un’ampia varietà di farmaci e altre molecole tossiche e usa l’energia cellulare per espellerle all’esterno. Ogni unità di AcrB è costituita da tre parti ripetute che ciclicamente passano attraverso tre conformazioni—legata in modo lasco, legata in modo stretto e aperta verso l’esterno—creando un movimento peristaltico che respinge gli antibiotici prima che possano causare danni duraturi.
Progettare un cuneo molecolare più intelligente
Gli sviluppatori di farmaci hanno a lungo cercato di bloccare questa pompa, ma la maggior parte degli inibitori precedenti si legava in una grande tasca lipofila che attraeva anche molte altre molecole, causando scarsa solubilità ed effetti collaterali. Partendo da lavori precedenti, gli autori si sono concentrati invece su una famiglia più recente di composti chiamati piridilpiperazine che si inseriscono in una regione più specializzata, profonda nella parte transmembrana di AcrB. Guidati da dati strutturali ad alta risoluzione, hanno riprogettato l’impalcatura chimica per stabilire contatti più forti con due aminoacidi carichi negativamente (D408 ed E947) situati lungo il percorso dove la pompa normalmente muove protoni. Aggiungendo una catena laterale benzilamminica posizionata con cura, hanno creato un nuovo composto, BDM91531, che si lega circa cinquanta volte più forte del predecessore e potenzia l’attività di più antibiotici a concentrazioni molto basse.
Congelare la pompa a metà corsa
La cristallografia a raggi X e la microscopia crio-elettronica single-particle hanno mostrato esattamente come BDM91531 disabiliti la pompa. Il composto si trova in una cavità allungata tra diversi elicoidi transmembrana all’interno di un sottounità di AcrB. Poiché BDM91531 porta due cariche positive, forma solide interazioni ioniche con D408 in profondità nella tasca ed E947 vicino al bordo citoplasmatico. Questi due punti di contatto sospendono l’inibitore come un ponte tra la parete interna della pompa e l’interno della cellula. Bloccato in posizione, il composto intrappola quella sottounità in uno stato intermedio tra le conformazioni aperta e lasca—il tipo di forma transitoria che la pompa normalmente attraversa solo per breve tempo. Poiché le tre sottounità devono ruotare attraverso i loro stati in modo sincronizzato, il congelamento di una di esse arresta l’intera macchina e interrompe l’efflusso di farmaci.
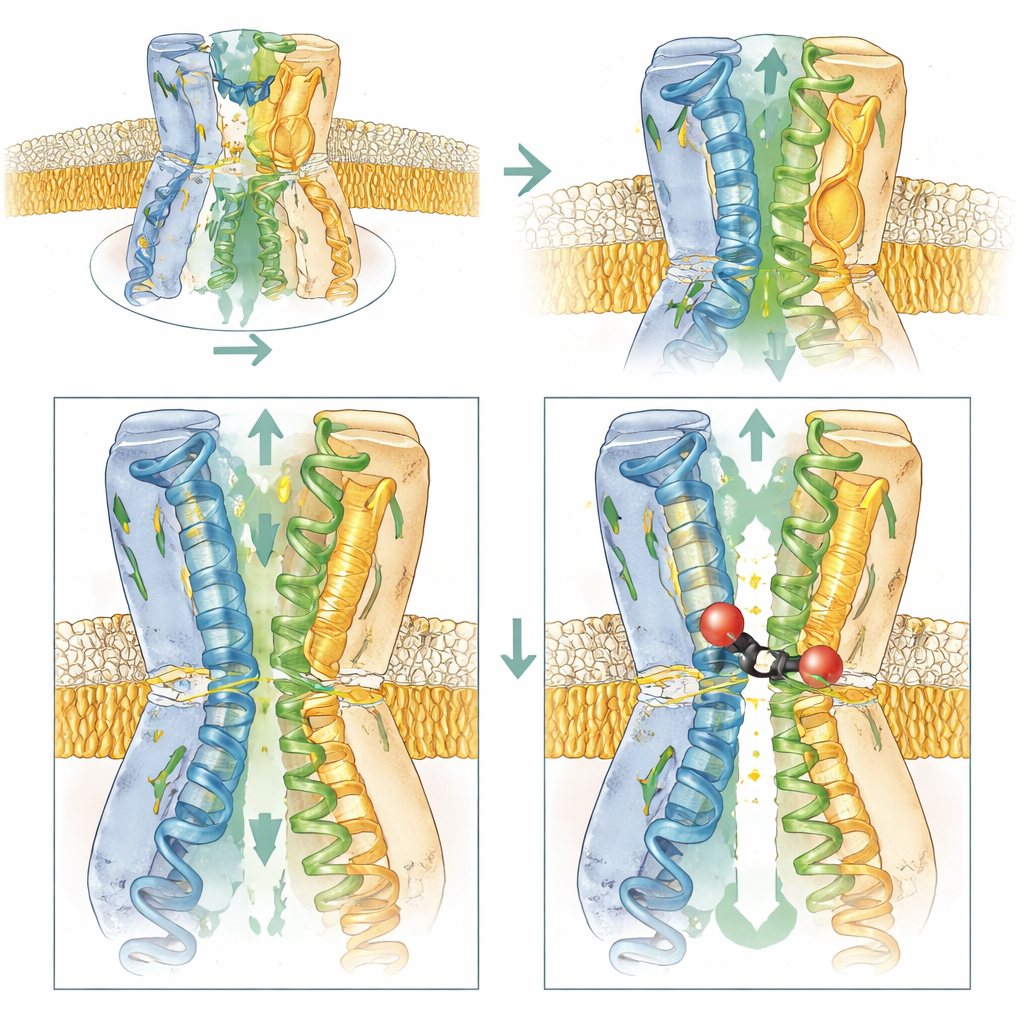
Caricare la porta per attrarre l’inibitore
Il team ha combinato misure biofisiche, test di crescita batterica e simulazioni al computer per sondare quali parti di AcrB sono più importanti per l’azione di BDM91531. L’eliminazione della carica negativa in D408 ha abolito completamente il legame, confermandone il ruolo centrale. La modifica di E947 o di un residuo acido vicino, D951, ha reso i batteri meno sensibili all’inibitore, mentre la reintroduzione di cariche negative in posizioni vicine ha ripristinato o persino aumentato la sensibilità. Questo mostra che, oltre a funzionare come punti di ancoraggio, questi residui acidi aiutano ad attrarre l’inibitore carico positivamente dal citoplasma nella gola di ingresso della tasca di legame. Al contrario, cambiamenti che rimuovono queste cariche o rendono la zona di ingresso più neutra hanno ridotto sia l’accesso sia il legame.
Rivitalizzare gli antibiotici mirando al movimento, non al farmaco
In termini pratici, BDM91531 agisce inceppando una parte mobile di una pompa batterica nel momento giusto, impedendo alla macchina di completare il suo ciclo e intrappolando gli antibiotici all’interno della cellula dove possono fare effetto. Poiché l’inibitore non uccide i batteri da solo alle dosi necessarie per bloccare la pompa, è più corretto considerarlo come un potenziatore da combinare con farmaci esistenti. Le intuizioni strutturali e meccanicistiche emerse da questo lavoro evidenziano esattamente quali caratteristiche della pompa dovrebbero essere mirate per progettare bloccanti ancora migliori, alimentando la prospettiva di nuovi adiuvanti terapeutici che riportino efficacia agli antibiotici contro alcune delle nostre infezioni più ostinate.
Citazione: Börnsen, C., Müller, R.T., Vieira Da Cruz, A. et al. Molecular mechanism of transition-state inhibitors of bacterial antibiotic efflux pumps. npj Antimicrob Resist 4, 35 (2026). https://doi.org/10.1038/s44259-026-00207-6
Parole chiave: resistenza agli antibiotici, inibitore della pompa di efflusso, AcrB, batteri Gram-negativi, progettazione di farmaci basata sulla struttura