Clear Sky Science · sv
Molekylär mekanism för transitionstillståndsinhibitorer av bakteriella antibiotika-effluxpumpar
Varför det kan rädda antibiotika att stoppa bakteriers ”pumpar”
Antibiotikaresistens uppstår ofta inte för att läkemedlen missar sina mål, utan för att bakterier aktivt pumpar ut dem igen. Denna studie visar, i atomär detalj, hur en nyligen konstruerad förening sätter igen en huvudpump hos bakterier och återställer befintliga antibiotikas effekt. Att förstå hur denna molekylära ”kil” fungerar kan öppna för kombinationsbehandlingar som återupplivar mediciner vi riskerar att förlora.
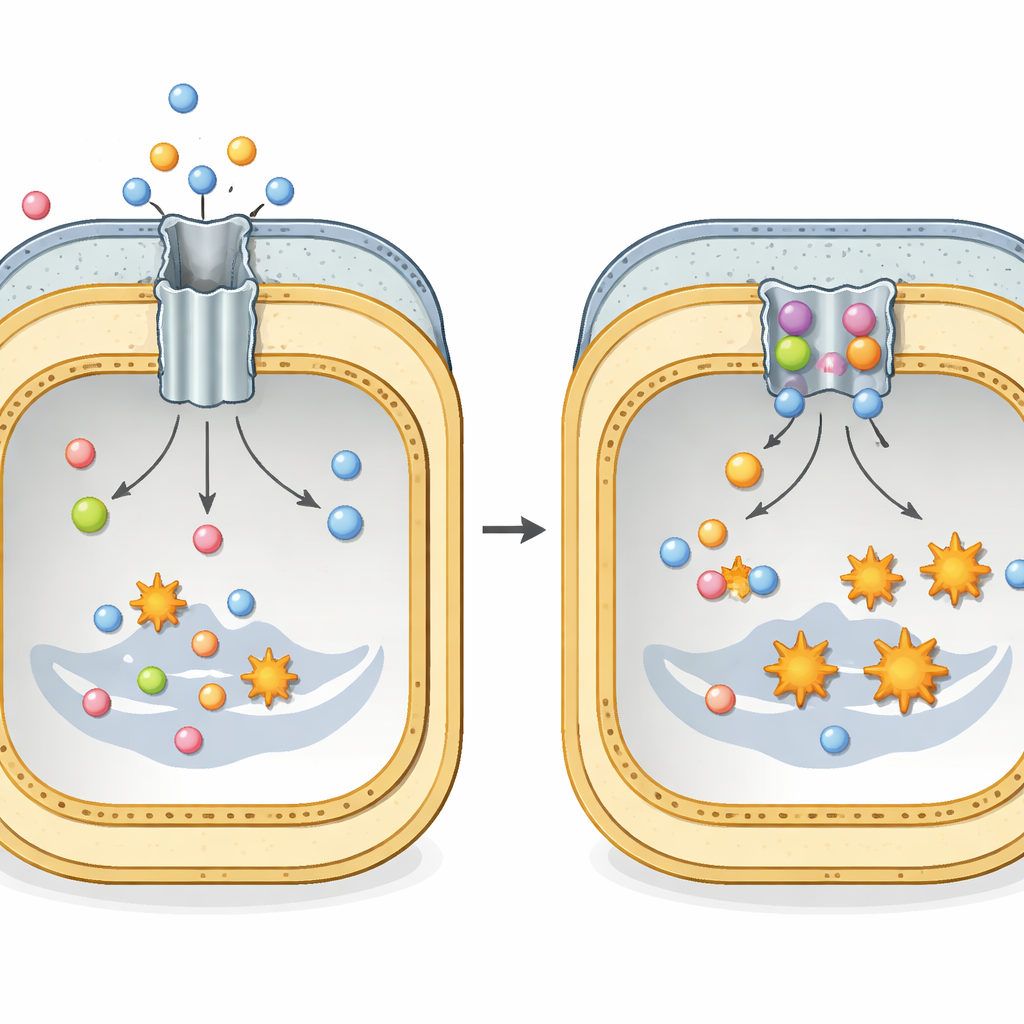
Tunneln som gömmer en flyktväg för antibiotika
Många farliga Gramnegativa bakterier, såsom Escherichia coli och Klebsiella pneumoniae, är beroende av ett stort proteinkomplex kallat AcrAB–TolC för att överleva antibiotikabehandling. Detta komplex sträcker sig över hela cellhöljet och fungerar som en tunnel med en motor vid dess inre ände. Den del som sitter i det inre membranet, kallad AcrB, känner igen ett brett spektrum av läkemedel och andra giftiga molekyler och använder cellulär energi för att stöta ut dem till utsidan. Varje AcrB-enhet består av tre upprepade delar som ständigt cyklar genom tre former—löstsittande, tättsittande och öppen mot utsidan—vilket skapar en peristaltisk rörelse som trycker ut antibiotika innan de kan orsaka bestående skada.
Att konstruera en smartare molekylär kil
Läkemedelsutvecklare har länge försökt blockera denna pump, men de flesta tidigare hämmare bundit i en stor fet ficka som också attraherar många andra molekyler, vilket leder till dålig löslighet och biverkningar. Med utgångspunkt i tidigare arbete fokuserade författarna istället på en nyare föreningsfamilj kallad pyridylpiperaziner som fäster i ett mer specialiserat område djupt i den membrangenomgående delen av AcrB. Guidad av högupplösta strukturella data omdesignade de det kemiska skelettet för att skapa starkare kontakter med två negativt laddade aminosyror (D408 och E947) som ligger längs den väg där pumpen normalt förflyttar protoner. Genom att lägga till en noggrant placerad bensylamin-sidokedja skapade de en ny förening, BDM91531, som binder ungefär femtio gånger starkare än sin föregångare och förstärker aktiviteten hos flera antibiotika vid mycket låga koncentrationer.
Att frysa pumpen mitt i slaget
Röntgenkristallografi och enkelpartikel-kryoelektronmikroskopi visade exakt hur BDM91531 inaktiverar pumpen. Föreningen ligger i en förlängd kavity mellan flera membrangenomgående helixar inne i en AcrB-underenhet. Eftersom BDM91531 bär två positiva laddningar bildar den starka saltbryggor med D408 djupt i fickan och E947 nära den cytoplasmatiska kanten. Dessa två kontaktpunkter upphänger inhibitorn som en bro mellan pumpens inre vägg och cellens insida. Låst på plats fångar föreningen den undenheten i ett mellantillstånd mellan den öppna och den lösa konformationen—en typ av övergående form som pumpen normalt bara passerar mycket kort. Eftersom de tre undenheterna måste rotera genom sina tillstånd synkront, stannar maskinen helt när en av dem fryses och drug efflux upphör.
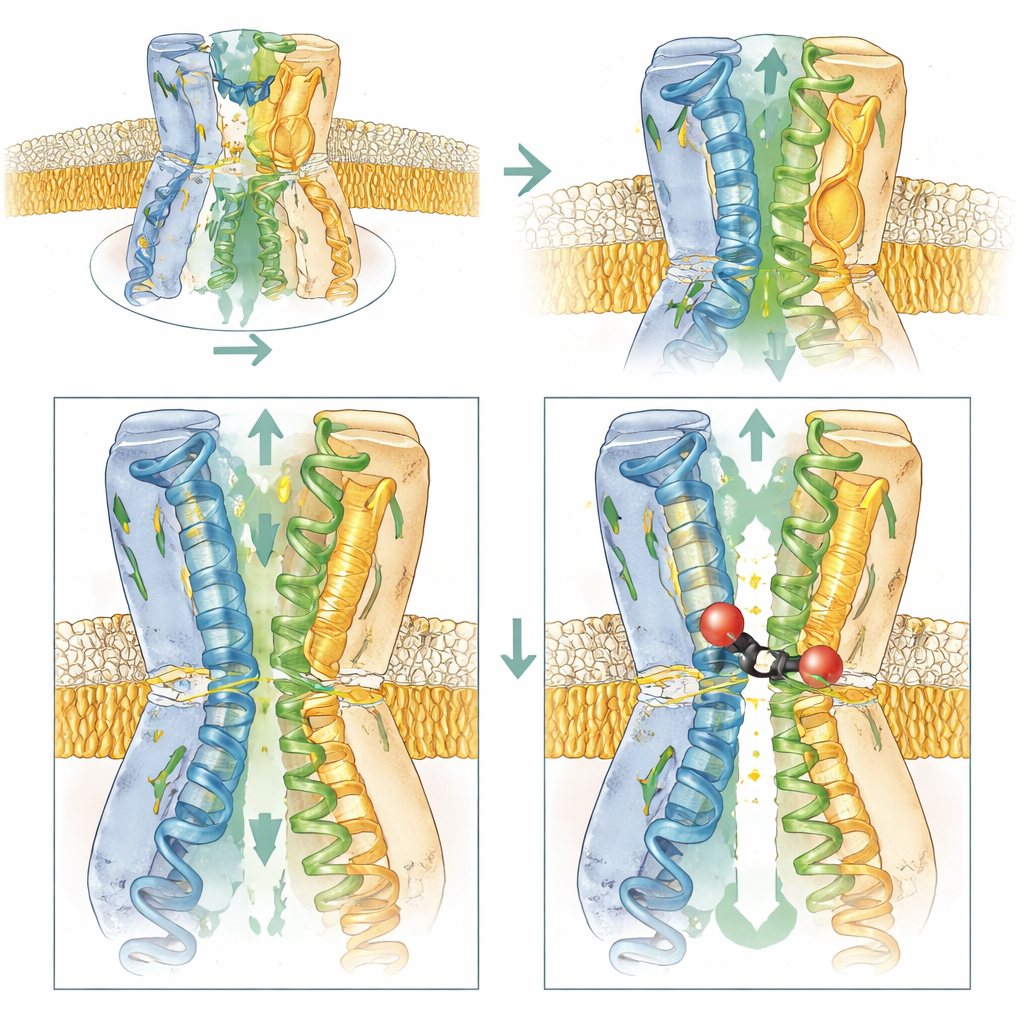
Ladda porten för att dra in inhibitorn
Teamet kombinerade biofysiska mätningar, bakterietillväxtstester och datasimuleringar för att undersöka vilka delar av AcrB som är viktigast för BDM91531:s verkan. Att ta bort den negativa laddningen vid D408 eliminerade bindningen helt, vilket bekräftar dess centrala roll. Att förändra E947 eller en närliggande sur rest, D951, gjorde bakterierna mindre känsliga för inhibitorn, medan återinförande av negativa laddningar vid intilliggande positioner återställde eller till och med ökade känsligheten. Detta visar att dessa sura rester, utöver att fungera som förankringspunkter, hjälper till att attrahera den positivt laddade inhibitorn från cytoplasman in i instegsgropen till bindningsfickan. I kontrast minskade förändringar som avlägsnade dessa laddningar eller gjorde instegsregionen mer neutral både åtkomst och bindning.
Återuppliva antibiotika genom att rikta in sig på rörelse, inte läkemedlet
I vardagliga termer fungerar BDM91531 genom att blockera en rörlig del av en bakteriepump vid precis rätt ögonblick, vilket hindrar maskinen från att fullfölja sin cykel och fångar antibiotika inne i cellen där de kan verka. Eftersom inhibitorn inte i sig dödar bakterier vid de doser som krävs för att blockera pumpen, bör den bäst ses som en förstärkare som kombineras med befintliga läkemedel. De strukturella och mekanistiska insikterna från detta arbete belyser exakt vilka egenskaper hos pumpen som bör riktas för att designa ännu bättre blockörer, vilket ökar utsikten för nya adjuvanta terapier som återställer antibiotikas effekt mot några av våra mest svårhanterliga infektioner.
Citering: Börnsen, C., Müller, R.T., Vieira Da Cruz, A. et al. Molecular mechanism of transition-state inhibitors of bacterial antibiotic efflux pumps. npj Antimicrob Resist 4, 35 (2026). https://doi.org/10.1038/s44259-026-00207-6
Nyckelord: antibiotikaresistens, effluxpumpshämmare, AcrB, Gramnegativa bakterier, strukturbaserad läkemedelsdesign