Clear Sky Science · fr
Mécanisme moléculaire des inhibiteurs d’état de transition des pompes d’efflux antibactériennes
Pourquoi arrêter les « pompes » bactériennes pourrait sauver les antibiotiques
La résistance aux antibiotiques survient souvent non pas parce que les médicaments n’atteignent pas leur cible, mais parce que les bactéries les expulsent activement. Cette étude révèle, au niveau atomique, comment un composé récemment conçu bloque une pompe bactérienne majeure et rend les antibiotiques existants efficaces de nouveau. Comprendre le fonctionnement de cette « cale » moléculaire pourrait ouvrir la voie à des thérapies combinées qui relanceraient des médicaments que nous risquons de perdre.
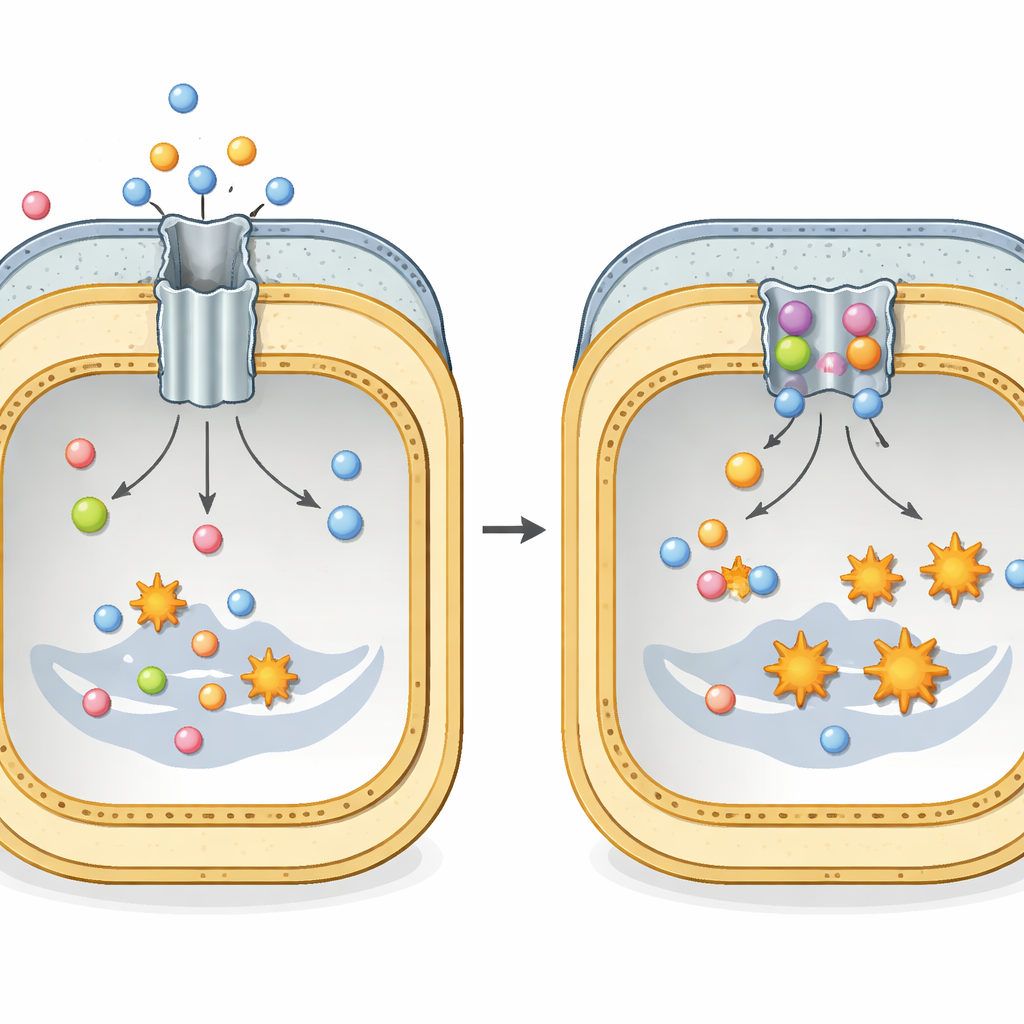
Un tunnel d’échappement caché pour les antibiotiques
De nombreuses bactéries à Gram négatif dangereuses, comme Escherichia coli et Klebsiella pneumoniae, dépendent d’un vaste assemblage protéique appelé AcrAB–TolC pour survivre au traitement antibiotique. Cet assemblage traverse l’ensemble de l’enveloppe cellulaire et fonctionne comme un tunnel doté d’un moteur à son extrémité interne. La partie de la membrane interne, nommée AcrB, reconnaît une grande variété de médicaments et d’autres molécules toxiques et utilise l’énergie cellulaire pour les expulser vers l’extérieur. Chaque unité d’AcrB est constituée de trois sous‑unités répétées qui cyclent en permanence à travers trois conformations — faiblement liée, fortement liée et ouverte vers l’extérieur — créant un mouvement péristaltique qui pousse les antibiotiques dehors avant qu’ils ne puissent causer des dommages durables.
Concevoir une cale moléculaire plus intelligente
Les développeurs de médicaments ont longtemps tenté de bloquer cette pompe, mais la plupart des inhibiteurs antérieurs se liaient dans une grande poche grasse qui attire aussi de nombreuses autres molécules, entraînant une faible solubilité et des effets indésirables. S’appuyant sur des travaux précédents, les auteurs se sont concentrés sur une nouvelle famille de composés appelés pyridylpipérazines qui se logent dans une région plus spécialisée, en profondeur dans la partie transmembranaire d’AcrB. Guidés par des données structurales à haute résolution, ils ont repensé l’échafaudage chimique pour établir des contacts plus forts avec deux acides aminés chargés négativement (D408 et E947) situés le long du chemin où la pompe déplace normalement les protons. En ajoutant une chaîne latérale benzylamine soigneusement positionnée, ils ont créé un nouveau composé, BDM91531, qui se lie environ cinquante fois plus fortement que son prédécesseur et potentialise l’activité de plusieurs antibiotiques à des concentrations très faibles.
Geler la pompe en plein mouvement
La cristallographie aux rayons X et la cryo‑microscopie électronique monocarte ont montré exactement comment BDM91531 désactive la pompe. Le composé se place dans une cavité allongée entre plusieurs hélices transmembranaires à l’intérieur d’une sous‑unité d’AcrB. Parce que BDM91531 porte deux charges positives, il forme de fortes liaisons ioniques avec D408, en profondeur dans la poche, et avec E947, près du rebord cytoplasmique. Ces deux points de contact suspendent l’inhibiteur comme un pont entre la paroi interne de la pompe et l’intérieur de la cellule. Verrouillé en place, le composé piège cette sous‑unité dans un état intermédiaire entre les conformations ouverte et lâche — le type de forme transitoire que la pompe ne prend normalement que brièvement. Puisque les trois sous‑unités doivent tourner de façon synchronisée à travers leurs états, le blocage d’une seule cale la machine entière et arrête l’efflux des médicaments.
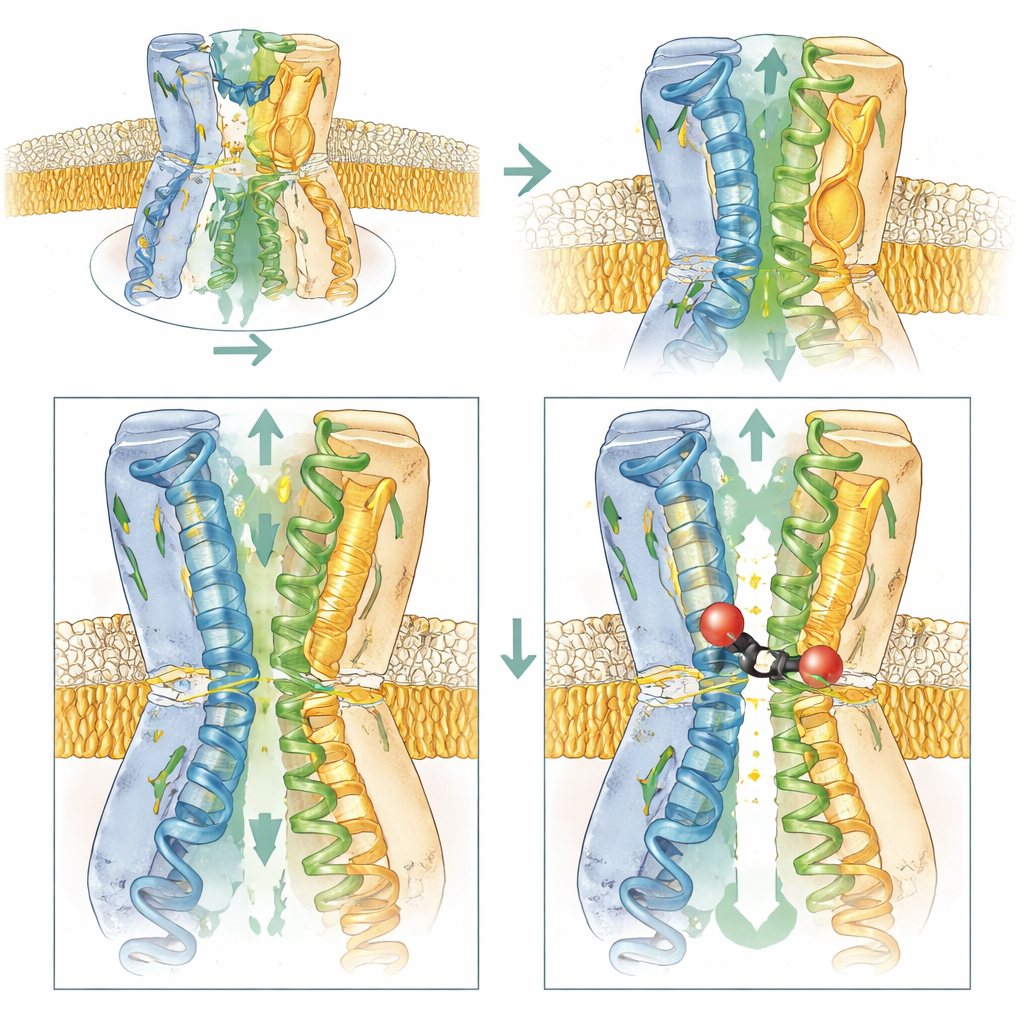
Charger l’entrée pour attirer l’inhibiteur
L’équipe a combiné mesures biophysiques, tests de croissance bactérienne et simulations informatiques pour déterminer quelles parties d’AcrB sont les plus importantes pour l’action de BDM91531. La suppression de la charge négative en D408 a éliminé totalement la liaison, confirmant son rôle central. La modification d’E947 ou d’un résidu acide voisin, D951, a rendu les bactéries moins sensibles à l’inhibiteur, tandis que la réintroduction de charges négatives à des positions voisines a restauré, voire renforcé, la sensibilité. Cela montre que, au‑delà de servir de points d’ancrage, ces résidus acides aident à attirer l’inhibiteur chargé positivement depuis le cytoplasme vers la gouttière d’entrée de la poche de liaison. En revanche, les changements qui supprimaient ces charges ou rendaient la zone d’entrée plus neutre réduisaient à la fois l’accès et la liaison.
Raviver les antibiotiques en ciblant le mouvement, pas le médicament
En termes simples, BDM91531 fonctionne en bloquant une pièce mobile de la pompe bactérienne au bon moment, empêchant la machine d’achever son cycle et retenant les antibiotiques à l’intérieur de la cellule pour qu’ils puissent agir. Parce que l’inhibiteur ne tue pas les bactéries à lui seul aux doses nécessaires pour bloquer la pompe, il est préférable de le considérer comme un amplificateur à combiner avec les médicaments existants. Les informations structurales et mécanistiques issues de ce travail mettent en évidence les caractéristiques de la pompe à cibler pour concevoir des bloqueurs encore meilleurs, ouvrant la perspective de nouveaux adjuvants thérapeutiques qui restaureraient l’efficacité des antibiotiques contre certaines de nos infections les plus tenaces.
Citation: Börnsen, C., Müller, R.T., Vieira Da Cruz, A. et al. Molecular mechanism of transition-state inhibitors of bacterial antibiotic efflux pumps. npj Antimicrob Resist 4, 35 (2026). https://doi.org/10.1038/s44259-026-00207-6
Mots-clés: résistance aux antibiotiques, inhibiteur de pompe d’efflux, AcrB, bactéries à Gram négatif, conception de médicaments basée sur la structure