Clear Sky Science · de
Molekularer Mechanismus von Übergangszustands-Inhibitoren bakterieller Antibiotika-Effluxpumpen
Warum das Stoppen bakterieller „Pumpen“ Antibiotika retten könnte
Antibiotikaresistenz entsteht häufig nicht, weil Wirkstoffe ihr Ziel nicht treffen, sondern weil Bakterien sie aktiv wieder hinauspumpen. Diese Studie zeigt bis auf atomare Ebene, wie eine neu entwickelte Verbindung eine wichtige bakterielle Pumpe blockiert und vorhandene Antibiotika wieder wirksam macht. Das Verständnis, wie dieses molekulare „Keil“-Prinzip funktioniert, könnte den Weg für Kombinationstherapien öffnen, die Medikamente reaktivieren, die wir zu verlieren drohen.
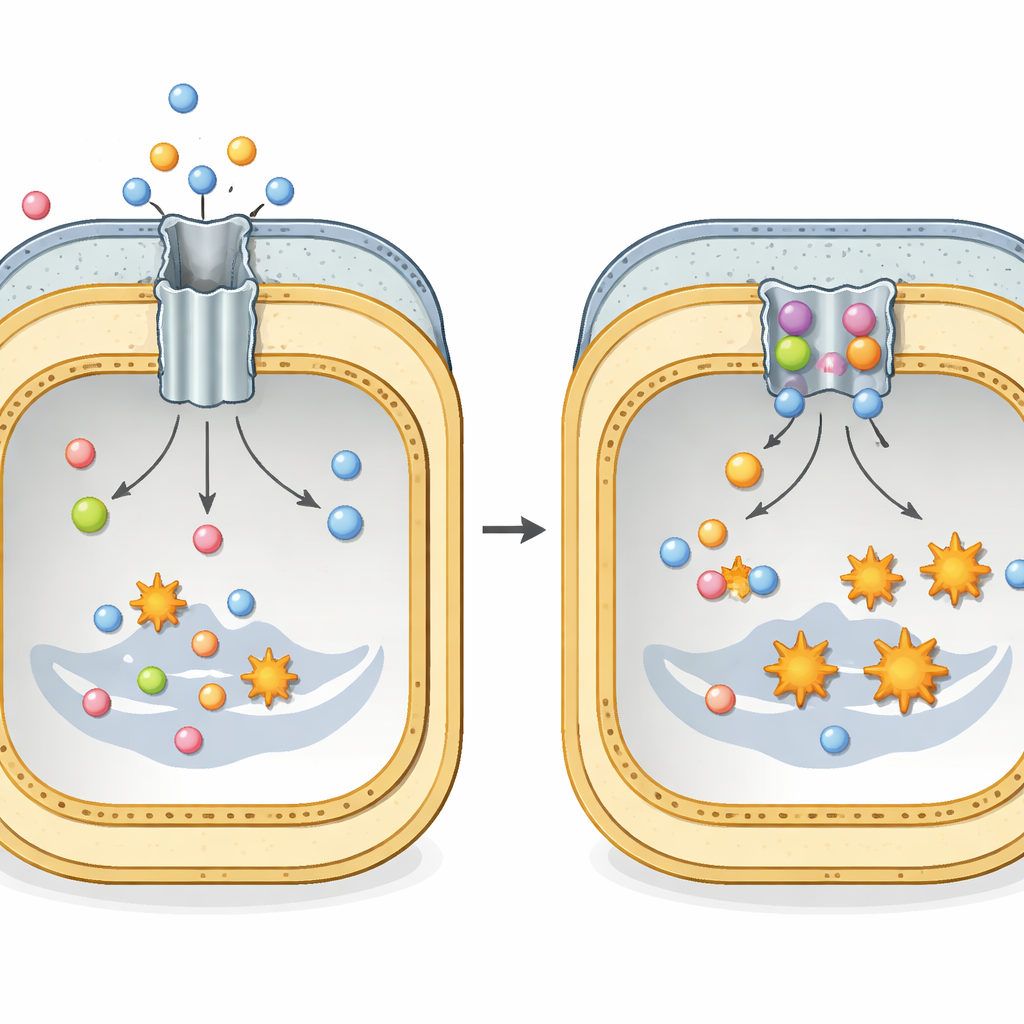
Ein versteckter Fluchtkanal für Antibiotika
Viele gefährliche Gram-negative Bakterien, etwa Escherichia coli und Klebsiella pneumoniae, sind auf einen großen Proteinkomplex namens AcrAB–TolC angewiesen, um Antibiotikabehandlungen zu überstehen. Dieser Komplex durchspannt die gesamte Zellhülle und funktioniert wie ein Tunnel mit einem Motor an seiner inneren Seite. Der innere Membranteil, AcrB genannt, erkennt eine breite Palette von Wirkstoffen und anderen toxischen Molekülen und nutzt zelluläre Energie, um sie nach außen zu befördern. Jede AcrB-Einheit besteht aus drei wiederkehrenden Untereinheiten, die fortlaufend durch drei Konformationen kreisen—locker gebunden, fest gebunden und nach außen geöffnet—und so eine peristaltische Bewegung erzeugen, die Antibiotika hinausdrückt, bevor sie dauerhaften Schaden anrichten können.
Entwurf eines intelligenteren molekularen Keils
Entwickler von Wirkstoffen haben lange versucht, diese Pumpe zu blockieren, doch die meisten früheren Inhibitoren banden in einer großen fettigen Tasche, die auch viele andere Moleküle anzieht und so zu schlechter Löslichkeit und Nebenwirkungen führt. Aufbauend auf früheren Arbeiten konzentrierten sich die Autoren stattdessen auf eine neuere Verbindungsklasse, die Pyridylpiperazine, die in einer spezialisierteren Region tief im membranüberspannenden Teil von AcrB Platz nimmt. Anhand hochauflösender Strukturdaten überarbeiteten sie das chemische Gerüst, um stärkere Kontakte zu zwei negativ geladenen Aminosäuren (D408 und E947) entlang des Pfads zu schaffen, auf dem die Pumpe normalerweise Protonen bewegt. Durch das Hinzufügen einer sorgfältig positionierten Benzylamin-Seitenkette entstand eine neue Verbindung, BDM91531, die etwa fünfzigmal stärker bindet als ihr Vorgänger und die Wirkung mehrerer Antibiotika in sehr niedrigen Konzentrationen verstärkt.
Die Pumpe mitten im Schlag einfrieren
Aufnahmen mittels Röntgenkristallographie und Einzelpartikel-Kryoelektronenmikroskopie zeigten genau, wie BDM91531 die Pumpe außer Gefecht setzt. Die Verbindung sitzt in einer langgestreckten Kavität zwischen mehreren membranüberspannenden Helices innerhalb einer AcrB-Untereinheit. Da BDM91531 zwei positive Ladungen trägt, bildet es starke Salzbrücken mit D408 tief in der Tasche und E947 nahe dem zytoplasmatischen Rand. Diese beiden Kontaktpunkte hängen den Inhibitor wie eine Brücke zwischen der Innenwand der Pumpe und dem Zellinneren auf. Fest verankert fängt die Verbindung diese Untereinheit in einem Zwischenzustand zwischen der offenen und der lockeren Konformation—eine transient Form, die die Pumpe normalerweise nur kurz durchläuft. Weil die drei Untereinheiten ihre Zustände synchron durchrotieren müssen, blockiert das Festfrieren einer Untereinheit die gesamte Maschine und stoppt den Efflux von Wirkstoffen.
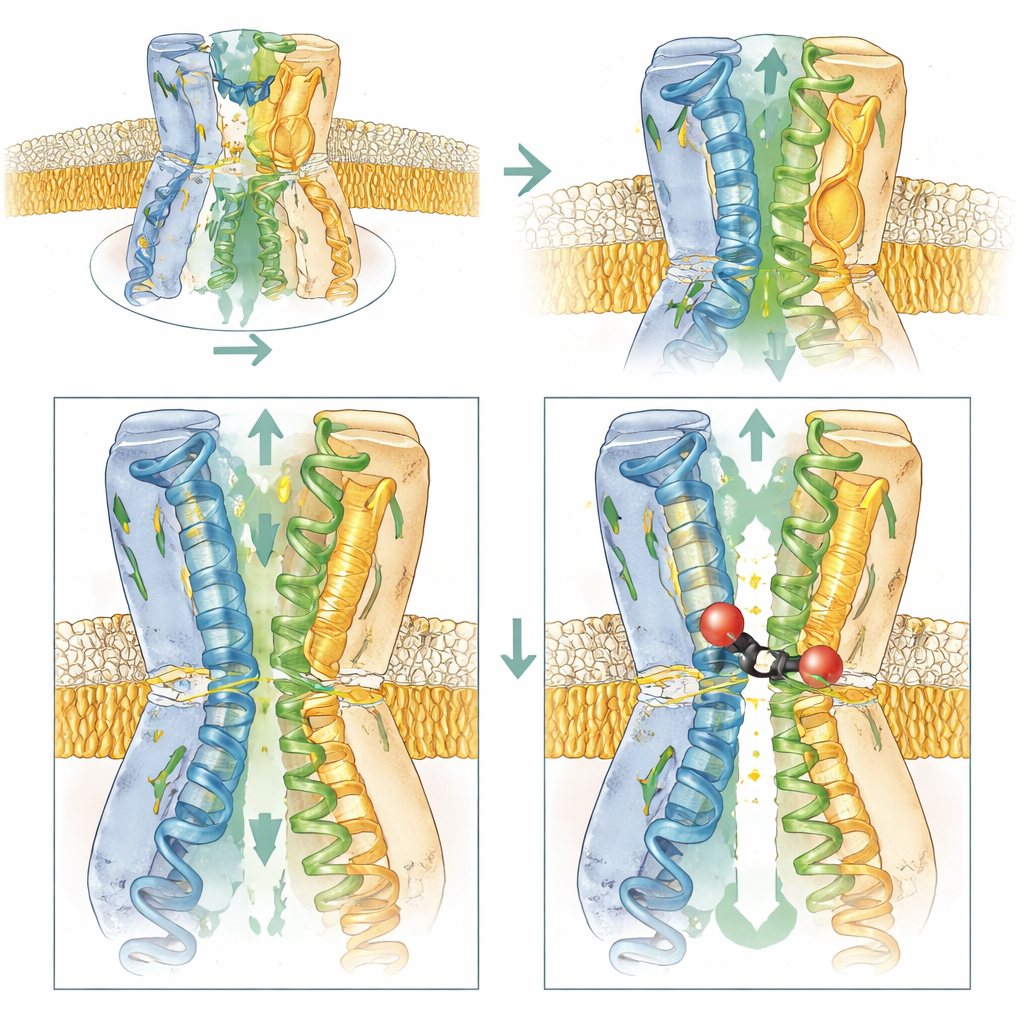
Aufladen der Türöffnung, um den Inhibitor hineinzuziehen
Das Team kombinierte biophysikalische Messungen, bakterielle Wachstumstests und Computersimulationen, um zu untersuchen, welche Teile von AcrB für die Wirkung von BDM91531 am wichtigsten sind. Die Entfernung der negativen Ladung an D408 beseitigte die Bindung vollständig und bestätigte seine zentrale Rolle. Veränderungen an E947 oder an einer benachbarten sauren Aminosäure, D951, verringerten die Empfindlichkeit der Bakterien gegenüber dem Inhibitor, während das Wiedereinführen negativer Ladungen an benachbarten Positionen die Sensitivität wiederherstellte oder sogar verstärkte. Das zeigt, dass diese sauren Reste neben ihrer Ankermfunktion auch helfen, den positiv geladenen Inhibitor aus dem Zytoplasma in die Eintrittsrille der Bindungstasche anzuziehen. Im Gegensatz dazu reduzierten Änderungen, die diese Ladungen entfernten oder die Eintrittszone neutraler machten, sowohl den Zugang als auch die Bindung.
Antibiotika wiederbeleben, indem man Bewegung statt das Medikament angreift
Anschaulich gesagt wirkt BDM91531, indem es ein bewegliches Teil einer bakteriellen Pumpe im genau richtigen Moment blockiert, sodass die Maschine ihren Zyklus nicht vollenden kann und Antibiotika im Inneren der Zelle gefangen bleiben, wo sie ihre Wirkung entfalten können. Weil der Inhibitor alleine in den für die Blockade erforderlichen Dosen die Bakterien nicht tötet, ist er am besten als Verstärker zu betrachten, der mit vorhandenen Wirkstoffen kombiniert wird. Die strukturellen und mechanistischen Einsichten aus dieser Arbeit zeigen genau, welche Merkmale der Pumpe angegriffen werden sollten, um noch bessere Blocker zu entwickeln, und eröffnen die Aussicht auf neue Adjuvans‑Therapien, die die Wirksamkeit von Antibiotika gegen einige unserer hartnäckigsten Infektionen wiederherstellen könnten.
Zitation: Börnsen, C., Müller, R.T., Vieira Da Cruz, A. et al. Molecular mechanism of transition-state inhibitors of bacterial antibiotic efflux pumps. npj Antimicrob Resist 4, 35 (2026). https://doi.org/10.1038/s44259-026-00207-6
Schlüsselwörter: Antibiotikaresistenz, Effluxpumpen-Inhibitor, AcrB, Gram-negative Bakterien, strukturbasierte Wirkstoffentwicklung