Clear Sky Science · zh
NZ2114 的分子作用——一种更强效的 plectasin 衍生物
为什么微小的真菌分子对未来抗生素很重要
随着越来越多的细菌感染对现有一线抗生素产生耐药性,科学家正在寻找新的杀菌策略,同时尽量避免快速诱导耐药。一个有前景的方向来自真菌和动物产生的小型防御分子。本研究深入解析了一种此类分子——经实验室优化的天然肽 plectasin 的变体 NZ2114——如何对抗危险细菌如金黄色葡萄球菌,包括难治的 MRSA 菌株。通过揭示其在细菌细胞壁上的逐步作用机制,这项工作为更智能的下一代抗生素设计提供了线索。
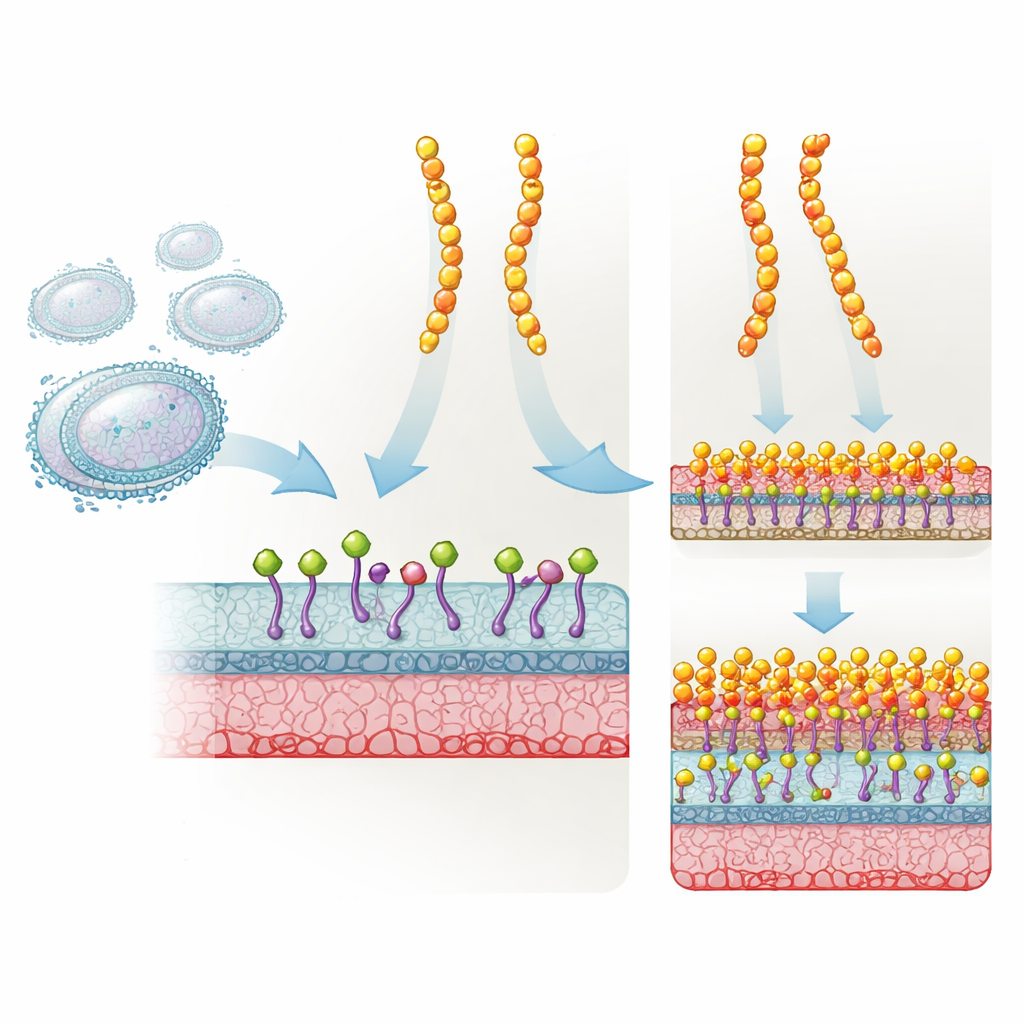
由天然盾牌变成更强的武器
Plectasin 是由真菌产生的一种短且稳固的蛋白质,天然用于抵御多种革兰氏阳性菌。它通过结合 Lipid II(一种细菌合成细胞壁所必需的关键构件)起作用。当 Lipid II 被封锁后,细胞壁无法正常合成,细菌最终死亡。药物开发者在 plectasin 的三个特定位点进行了改造,得到 NZ2114,在动物模型中对葡萄球菌和链球菌表现出更强的效力。然而,尽管 NZ2114 成功并引起临床兴趣,人们并不清楚为何这三个突变能显著提高其活性。
并非更强的抓握,而是不同的持握方式
一个简单的假设是,NZ2114 可能更紧密地结合金黄色葡萄球菌中存在的“特殊”形式的 Lipid II,而原始 plectasin 对这种改性靶标结合较差。作者通过一系列结构学和结合实验对该假说进行了直接检验。他们研究了两种肽与几种 Lipid II 变体(包括葡萄球菌典型的化学修饰)之间的相互作用,并测量了每种肽在不同膜环境中的结合强度。令人意外的结果是,plectasin 和 NZ2114 对所有 Lipid II 变体的结合都很好,且 plectasin 在某些情况下结合力甚至略强。这排除了靶标识别差异作为 NZ2114 杀菌力增强的主要原因。
微小改变如何重塑运动与协作
为探明真实原因,研究团队使用核磁共振(NMR)和计算模拟观察 NZ2114 中三个替换的氨基酸。这些突变微妙地重建了靠近一个可吸引钙和镁离子的负电斑块的氢键网络。反过来,这改变了肽的 N 端环和紧邻接触 Lipid II 的片段的形状与柔性。固态 NMR 和高速原子力显微镜进一步揭示了这些局部微调在膜表面的表现。在低钙条件下,NZ2114 在细菌膜上形成小而高度可动的簇,而 plectasin 则已扩展成更大的“地毯状”组装。当钙丰度增加时,NZ2114 发生整体重排,迅速形成与 plectasin 相似的大而有序的地毯结构。
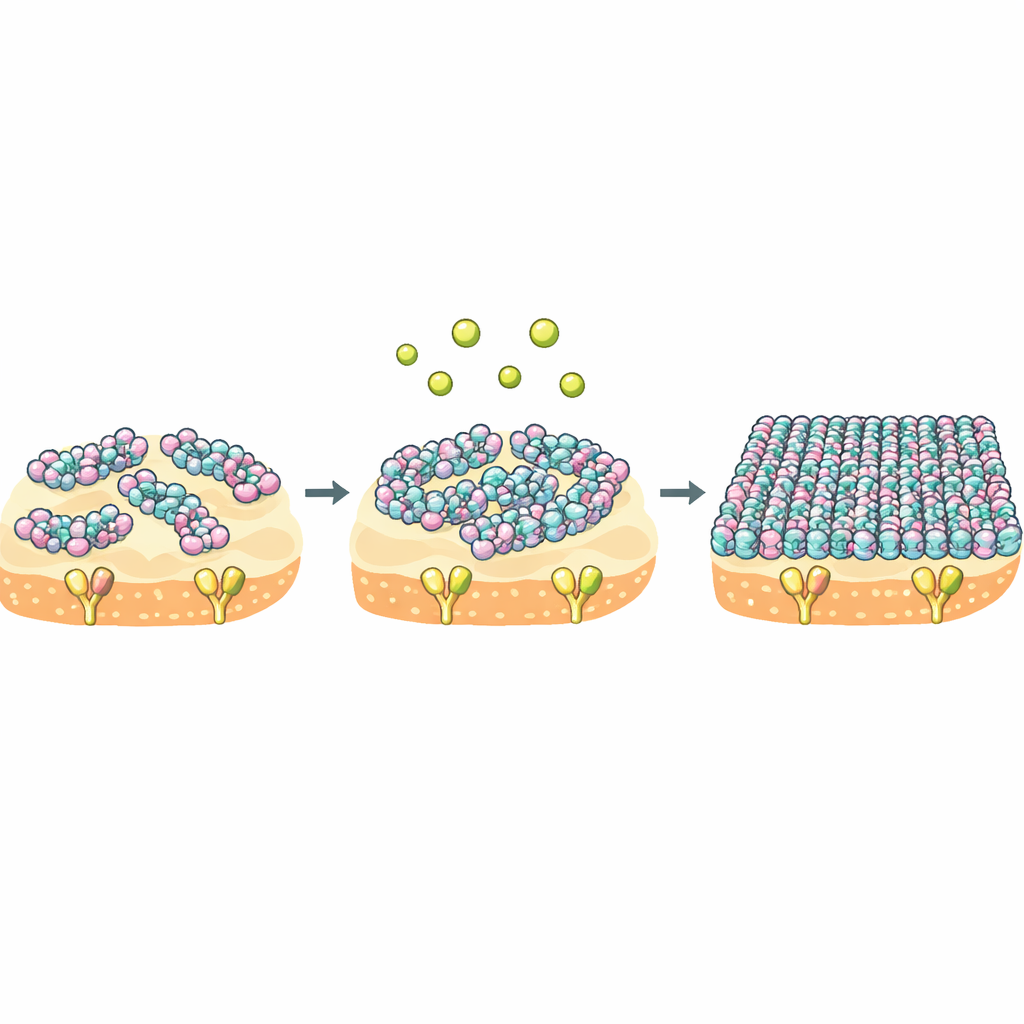
钙作为分子群行为的开关
核心洞见是,NZ2114 与 plectasin 共享相同靶标,但在到达膜面后其“群体行为”不同。对 NZ2114 而言,钙像一个强有力的开关:它将肽从松散、动态的状态切换为刚性、高度有序的层,覆盖膜面并长时间捕获 Lipid II。热力学测量显示,NZ2114 在结合靶标时付出的熵代价要小得多,这意味着结合态仍保持更多的可动性与多样性。由于结合与自组装是耦合的,这种既灵活又可被钙调控的行为可能允许 NZ2114 在细菌表面的不同环境中调整其超分子结构,从而提升其杀菌效率。
这对未来抗生素设计意味着什么
对非专业读者而言,本研究的主要信息是:NZ2114 的优势并非来自识别不同的“锁”,而是来自在同一锁孔周围形成更有效的“人群”。少量且精确定位的突变改变了肽对钙离子的响应以及与邻近分子的组织方式。研究表明,金黄色葡萄球菌中 Lipid II 的修饰并非 plectasin 性能较差的罪魁祸首,因此注意力应转向通过控制肽的构象、柔性、电荷和离子敏感性来调节其集体行为。这些见解可为设计更难被细菌回避、且对耐药菌株更具效力的肽类抗生素提供指导。
引用: Derks, M.G.N., Jekhmane, S., Maity, S. et al. Molecular action of NZ2114, a superior plectasin derivative. npj Antimicrob Resist 4, 34 (2026). https://doi.org/10.1038/s44259-026-00196-6
关键词: 抗菌肽, Lipid II, 耐甲氧西林金黄色葡萄球菌(MRSA), 钙依赖性抗生素, 超分子组装