Clear Sky Science · pt
Ação molecular de NZ2114, um derivado superior da plectasina
Por que pequenas moléculas fúngicas importam para os antibióticos do futuro
À medida que mais infecções bacterianas deixam de responder aos nossos melhores antibióticos, cientistas buscam novas maneiras de matar germes sem induzir resistência rápida. Uma pista promissora vem de pequenas moléculas defensivas produzidas por fungos e animais. Este estudo investiga como uma dessas moléculas, uma versão otimizada em laboratório do peptídeo natural plectasina chamada NZ2114, combate bactérias perigosas como Staphylococcus aureus, incluindo cepas difíceis de tratar como MRSA. Ao revelar sua ação passo a passo na parede celular bacteriana, o trabalho aponta para um design mais inteligente de antibióticos de próxima geração.
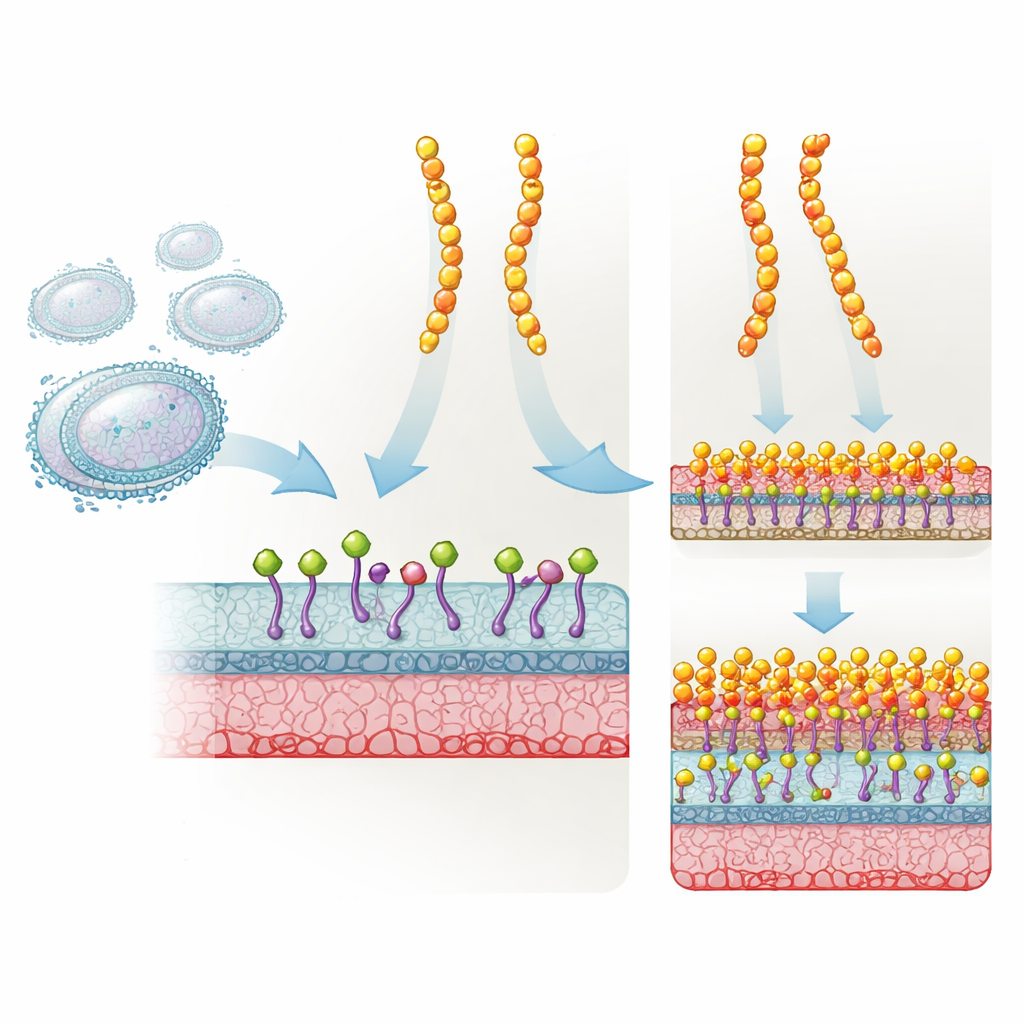
Um escudo natural transformado em arma mais potente
A plectasina é uma proteína curta e resistente produzida por um fungo que protege naturalmente contra muitas bactérias Gram‑positivas. Ela atua ao se ligar ao Lipid II, um bloco de construção crucial que as bactérias usam para fabricar sua parede celular. Quando o Lipid II fica preso, a parede celular não pode ser construída corretamente, e a bactéria acaba morrendo. Desenvolvedores de fármacos modificaram a plectasina em três posições específicas para criar a NZ2114, que se mostrou muito mais eficaz em modelos animais contra estafilococos e estreptococos. Ainda assim, apesar do sucesso e do interesse clínico, ninguém sabia exatamente por que esse tripleto mutante funcionava tão melhor que o original.
Não por segurar mais forte, mas por segurar de maneira diferente
Uma explicação simples teria sido que NZ2114 pudesse se prender com mais força a uma forma “especial” de Lipid II encontrada em Staphylococcus aureus, enquanto a plectasina se ligaria mal a esse alvo alterado. Os autores testaram essa ideia diretamente usando uma bateria de experimentos estruturais e de ligação. Eles examinaram como ambos os peptídeos interagem com várias versões de Lipid II, incluindo aquelas com modificações químicas típicas de estafilococos, e mediram a força de ligação de cada peptídeo em diferentes tipos de membranas. O resultado surpreendente foi que tanto a plectasina quanto a NZ2114 se ligaram muito bem a todas as variantes de Lipid II, muitas vezes com a plectasina ligando-se ligeiramente com mais afinidade. Isso descartou o reconhecimento do alvo como a principal razão para o poder letal superior da NZ2114.
Como pequenas mudanças remodelam movimento e cooperação
Para ver o que realmente mudou, a equipe usou ressonância magnética nuclear (RMN) e simulações computacionais para examinar os três aminoácidos substituídos na NZ2114. Essas mutações redesenharam sutilmente uma rede de ligações de hidrogênio próxima a uma área carregada negativamente que pode atrair íons cálcio e magnésio. Isso, por sua vez, alterou a forma e a flexibilidade do laço N‑terminal do peptídeo e de um segmento próximo que contata o Lipid II. RMN em estado sólido e microscopia de força atômica em alta velocidade revelaram então como esses ajustes locais se manifestam sobre a superfície da membrana. Em níveis baixos de cálcio, a NZ2114 formou pequenos aglomerados altamente móveis na membrana bacteriana, enquanto a plectasina já se espalhava em montagens maiores, em estilo ‘tapete’. Quando o cálcio era abundante, a NZ2114 passou por uma reorganização global e se converteu em grandes tapetes ordenados que se assemelhavam fortemente aos formados pela plectasina.
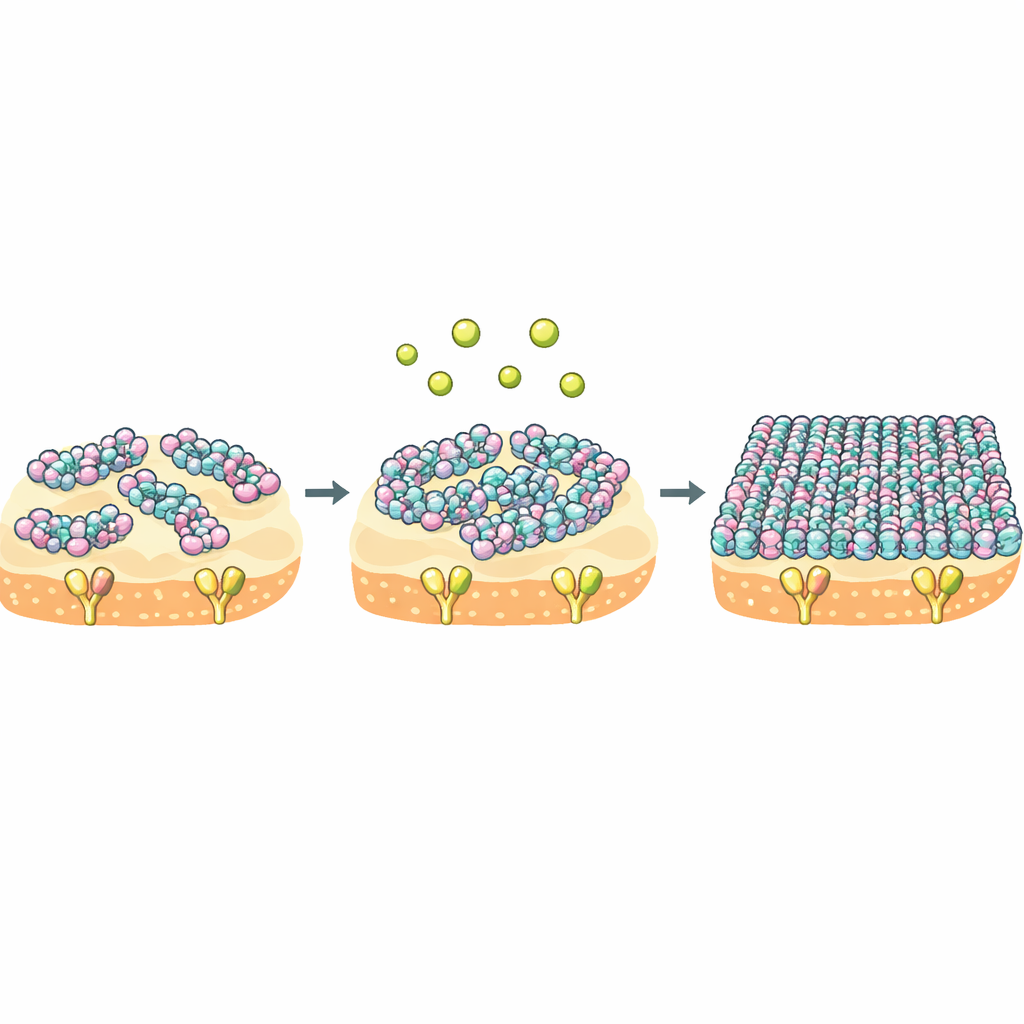
O cálcio como um interruptor para comportamento coletivo molecular
A ideia central é que NZ2114 e plectasina compartilham o mesmo alvo, mas diferem em seu “comportamento de grupo” quando alcançam a membrana. Para a NZ2114, o cálcio atua como um interruptor poderoso: ele desloca o peptídeo de um estado solto e dinâmico para uma camada rígida e altamente organizada que cobre a membrana e aprisiona o Lipid II por longos períodos. Medições termodinâmicas mostram que a NZ2114 paga um custo de entropia bem menor ao se ligar ao seu alvo, o que significa que o estado ligado permanece mais móvel e diversificado. Como a ligação e a auto‑montagem estão acopladas, esse comportamento flexível, porém ajustável pelo cálcio, pode permitir que a NZ2114 adapte sua estrutura supramolecular a diferentes ambientes na superfície bacteriana, aumentando assim sua eficiência letal.
O que isso significa para o projeto de antibióticos futuros
A principal mensagem do estudo para leigos é que a vantagem da NZ2114 não vem de agarrar uma fechadura diferente, mas de formar uma multidão mais eficaz ao redor da mesma chave. Pequenas mutações colocadas com precisão mudaram como o peptídeo responde a íons de cálcio e como se organiza com seus vizinhos na membrana bacteriana. Ao mostrar que as modificações do Lipid II em Staphylococcus aureus não são a causa do desempenho mais fraco da plectasina, o trabalho redireciona a atenção para controlar forma, flexibilidade, carga e sensibilidade a íons do peptídeo para ajustar o comportamento coletivo. Esses insights podem orientar o desenho de novos antibióticos à base de peptídeos que sejam mais difíceis de serem contornados pelas bactérias e mais potentes contra cepas resistentes.
Citação: Derks, M.G.N., Jekhmane, S., Maity, S. et al. Molecular action of NZ2114, a superior plectasin derivative. npj Antimicrob Resist 4, 34 (2026). https://doi.org/10.1038/s44259-026-00196-6
Palavras-chave: peptídeos antimicrobianos, Lipid II, MRSA, antibióticos dependentes de cálcio, assembléias supramoleculares