Clear Sky Science · it
Azione molecolare di NZ2114, un derivato superiore della plectasina
Perché piccole molecole fungine sono importanti per gli antibiotici del futuro
Con l’aumento delle infezioni batteriche che non rispondono più ai nostri migliori antibiotici, i ricercatori cercano nuovi modi per uccidere i germi senza favorire una rapida resistenza. Una pista promettente proviene da piccole molecole difensive prodotte da funghi e animali. Questo studio analizza come una di queste molecole, una versione ottimizzata in laboratorio del peptide naturale plectasina chiamata NZ2114, combatte batteri pericolosi come Staphylococcus aureus, comprese le ceppi MRSA difficili da trattare. Scoprendo la sua azione passo dopo passo sulla parete cellulare batterica, il lavoro indica come progettare in modo più intelligente gli antibiotici di nuova generazione.
Una difesa naturale trasformata in un’arma più potente
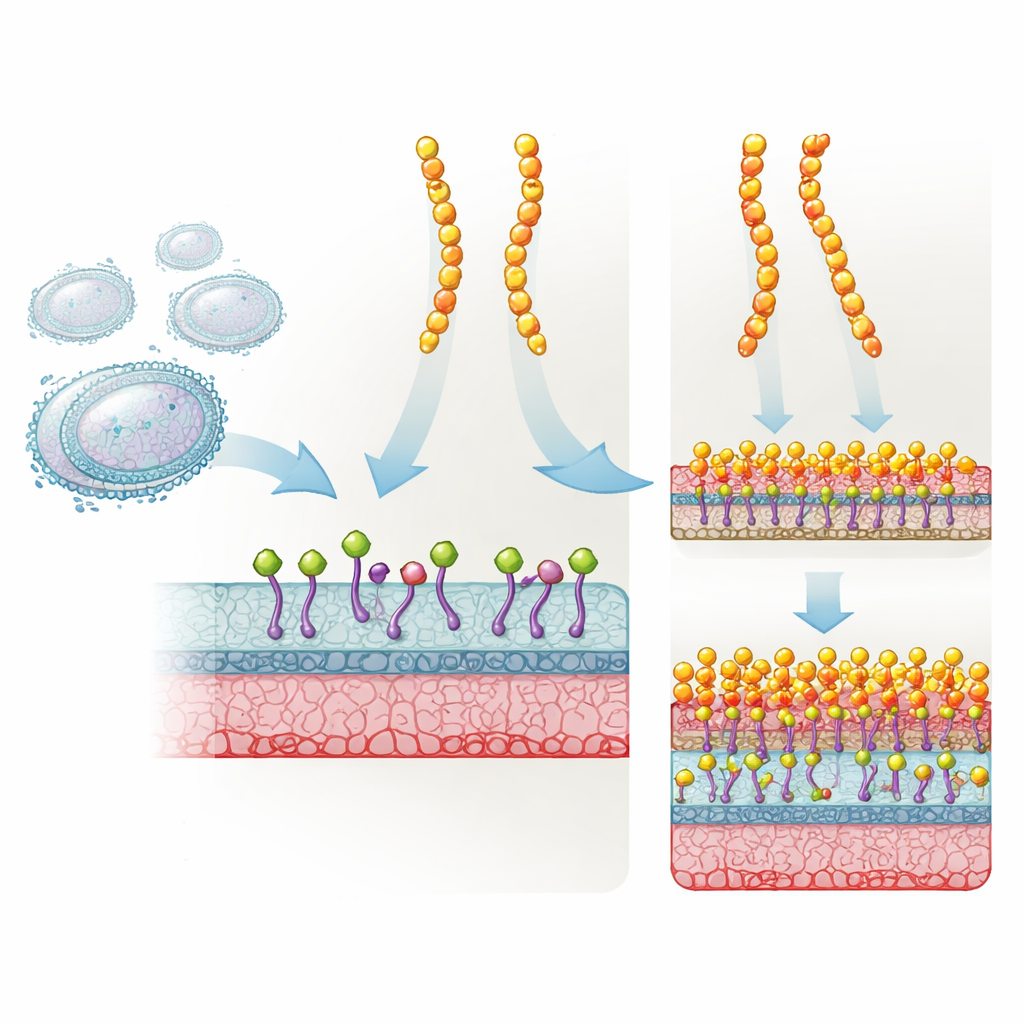
La plectasina è una proteina corta e robusta prodotta da un fungo che difende naturalmente da molti batteri Gram‑positivi. Agisce legando il Lipid II, un mattone essenziale che i batteri usano per costruire la parete cellulare. Quando il Lipid II è bloccato, la parete non può più essere costruita correttamente e il batterio muore. Gli sviluppatori di farmaci hanno modificato la plectasina in tre posizioni specifiche per ottenere NZ2114, che si è dimostrata molto più efficace nei modelli animali contro stafilococchi e streptococchi. Eppure, nonostante il successo e l’interesse clinico, non si sapeva esattamente perché questo triplo‑mutante funzionasse molto meglio dell’originale.
Non una presa più forte, ma un modo diverso di aggrapparsi
Una spiegazione semplice era che NZ2114 potesse legarsi più saldamente a una forma “speciale” di Lipid II presente in Staphylococcus aureus, mentre la plectasina lo legherebbe male. Gli autori hanno messo alla prova direttamente questa idea usando una serie di esperimenti strutturali e di legame. Hanno esaminato come entrambi i peptidi interagiscono con diverse varianti di Lipid II, comprese quelle con modifiche chimiche tipiche degli stafilococchi, e hanno misurato quanto fortemente ogni peptide si legasse in diversi tipi di membrane. L’esito sorprendente è stato che sia la plectasina sia NZ2114 legavano molto bene tutte le varianti di Lipid II, spesso con la plectasina che legava leggermente più forte. Questo ha escluso il riconoscimento del bersaglio come causa principale della maggiore efficacia di NZ2114.
Come piccoli cambiamenti rimodellano movimento e collaborazione
Per capire cosa fosse realmente cambiato, il gruppo ha usato risonanza magnetica nucleare (RMN) e simulazioni al computer per studiare i tre amminoacidi sostituiti in NZ2114. Queste mutazioni hanno rimodulato in modo sottile una rete di legami a idrogeno vicino a una regione caricata negativamente che può attrarre ioni calcio e magnesio. Ciò ha a sua volta alterato la forma e la flessibilità del loop N‑terminale del peptide e di un segmento vicino che entra in contatto con il Lipid II. RMN in stato solido e microscopia a forza atomica ad alta velocità hanno poi mostrato come queste modifiche locali si manifestano sulla superficie della membrana. A bassi livelli di calcio, NZ2114 formava piccoli ammassi altamente mobili sulla membrana batterica, mentre la plectasina si organizzava già in ammassi più grandi simili a un tappeto. Quando il calcio era abbondante, NZ2114 subiva una riorganizzazione globale e si disponeva in grandi tappeti ordinati che assomigliavano molto a quelli formati dalla plectasina.
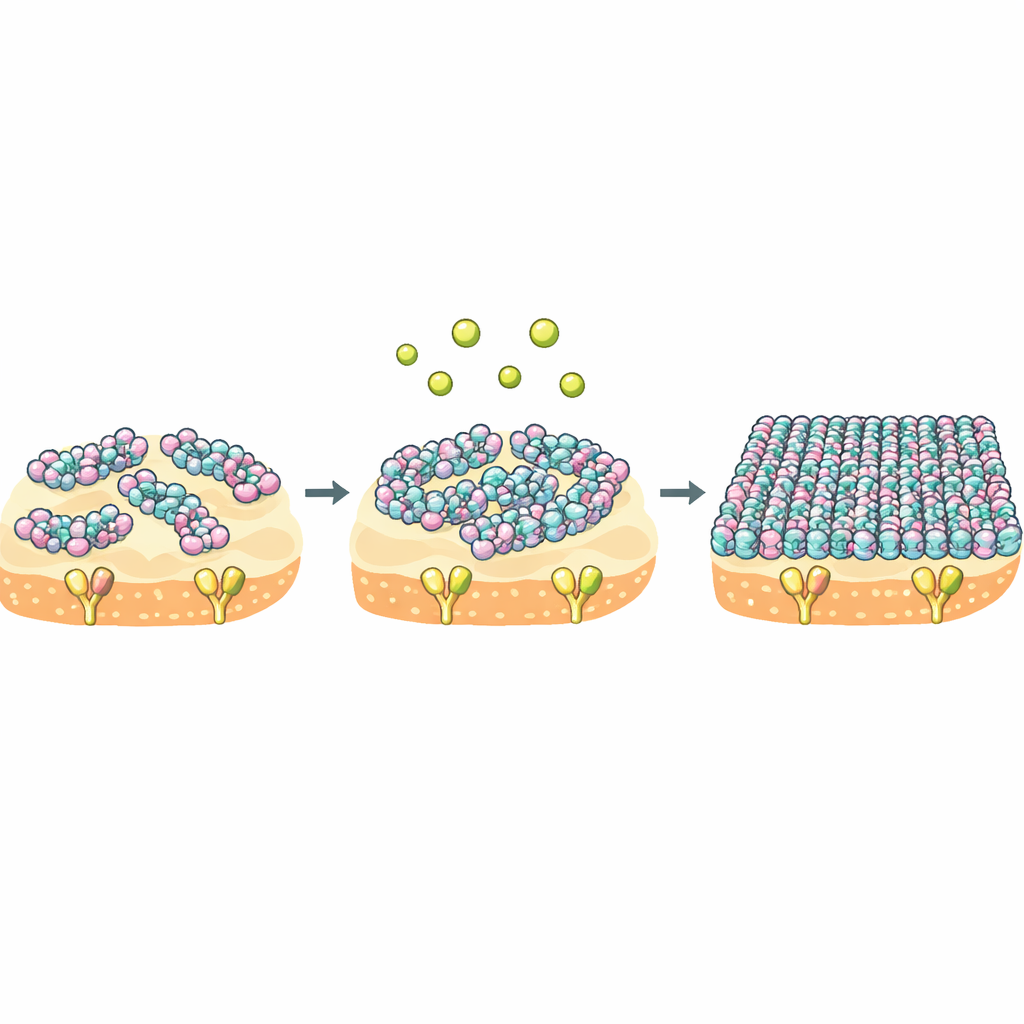
Il calcio come interruttore del comportamento collettivo molecolare
La chiave è che NZ2114 e la plectasina condividono lo stesso bersaglio ma differiscono nel loro “comportamento di massa” quando arrivano sulla membrana. Per NZ2114 il calcio funge da potente interruttore: sposta il peptide da uno stato lasco e dinamico a uno strato rigido e altamente organizzato che ricopre la membrana e intrappola il Lipid II per lungo tempo. Misure termodinamiche mostrano che NZ2114 paga un costo entropico molto minore nel legare il bersaglio, il che significa che lo stato legato resta più mobile e variegato. Poiché legame e auto‑assemblaggio sono accoppiati, questo comportamento flessibile ma regolabile dal calcio può permettere a NZ2114 di adattare la sua struttura sopramolecolare a diversi ambienti sulla superficie batterica, migliorandone così l’efficacia uccidente.
Cosa significa per la progettazione di antibiotici futuri
Il messaggio principale dello studio per un pubblico non specialistico è che il vantaggio di NZ2114 non deriva dal bloccare una serratura diversa, ma dal formare una folla più efficace intorno alla stessa serratura. Mutazioni piccole e precise hanno cambiato come il peptide risponde agli ioni calcio e come si organizza con i vicini sulla membrana batterica. Mostrando che le modifiche del Lipid II in Staphylococcus aureus non spiegano le prestazioni inferiori della plectasina, il lavoro sposta l’attenzione verso il controllo della forma del peptide, della sua flessibilità, della carica e della sensibilità agli ioni per modulare il comportamento collettivo. Queste intuizioni possono guidare la progettazione di nuovi antibiotici peptidici più difficili da eludere per i batteri e più potenti contro ceppi resistenti.
Citazione: Derks, M.G.N., Jekhmane, S., Maity, S. et al. Molecular action of NZ2114, a superior plectasin derivative. npj Antimicrob Resist 4, 34 (2026). https://doi.org/10.1038/s44259-026-00196-6
Parole chiave: peptidi antimicrobici, Lipid II, MRSA, antibiotici dipendenti dal calcio, assemblaggi sopramolecolari