Clear Sky Science · ru
Молекулярное действие NZ2114, улучшённого производного плеказина
Почему крошечные молекулы грибов важны для будущих антибиотиков
По мере того как всё больше бактериальных инфекций перестаёт реагировать на лучшие антибиотики, учёные ищут новые способы убивать микробов, не провоцируя быструю устойчивость. Многообещающий путь — небольшие защитные молекулы, которые вырабатывают грибы и животные. В этом исследовании подробно изучают, как одна из таких молекул, лабораторно улучшённая версия природного пептида плеказина под названием NZ2114, борется с опасными бактериями вроде Staphylococcus aureus, включая трудно поддающиеся лечению штаммы MRSA. Раскрывая его пошаговое действие на клеточную стенку бактерий, работа указывает на принципы более разумного проектирования антибиотиков следующего поколения.
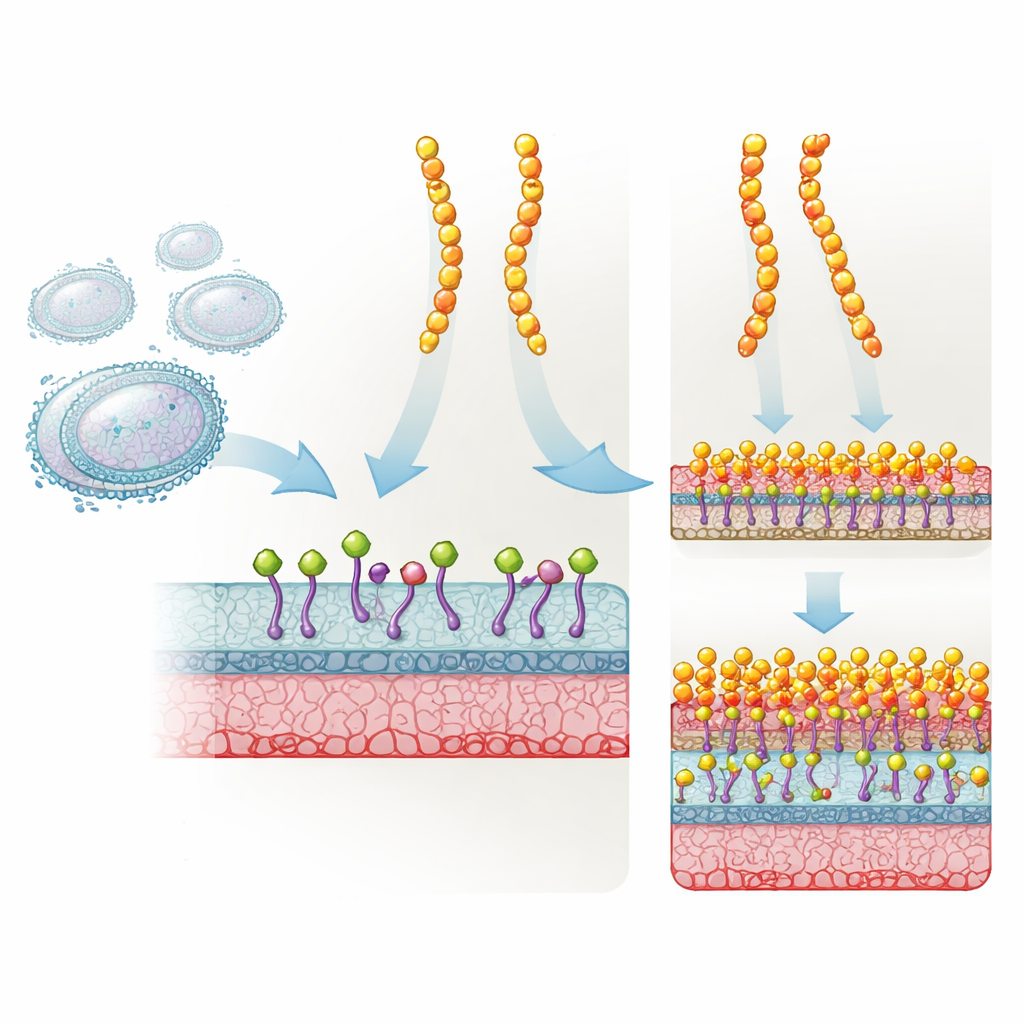
Природный щит, превращённый в более мощное оружие
Плеказин — короткий, прочный белок, который продуцирует гриб и который естественно защищает от многих грамположительных бактерий. Он действует, захватывая Липид II — ключевой строительный блок, который бактерии используют для синтеза клеточной стенки. Когда Липид II блокирован, стенку нельзя правильно построить, и бактерия в конце концов погибает. Разработчики лекарств изменили плеказин в трёх определённых положениях, получив NZ2114, который показал себя гораздо эффективнее в моделях на животных против стафилококков и стрептококков. Тем не менее, несмотря на успех и клинический интерес, долгое время не было ясно, почему именно этот тройной мутант работает заметно лучше оригинала.
Не более сильное сцепление, а другой способ удержания
Простое объяснение заключалось в том, что NZ2114 может крепче цепляться за «особую» форму Липид II, характерную для Staphylococcus aureus, тогда как плеказин плохо связывался бы с этой изменённой мишенью. Авторы проверили эту гипотезу прямыми структурными и связывающими экспериментами. Они изучали, как оба пептида взаимодействуют с несколькими вариантами Липид II, включая версии с химическими модификациями, типичными для стафилококков, и измеряли прочность связывания в разных типах мембран. Удивительный результат: и плеказин, и NZ2114 очень хорошо связывались со всеми вариантами Липид II, причём иногда плеказин связывался даже слегка сильнее. Это исключило распознавание мишени как основную причину превосходства NZ2114.
Как небольшие изменения меняют движение и командную работу
Чтобы понять реальные изменения, команда использовала ЯМР (ядерный магнитный резонанс) и компьютерное моделирование для изучения трёх заменённых аминокислот в NZ2114. Эти мутации тонко перенастроили сеть водородных связей возле отрицательно заряженной области, способной привлекать ионы кальция и магния. В результате изменилась форма и гибкость N‑концевой петли пептида и соседнего сегмента, контактирующего с Липидом II. Данные твердофазного ЯМР и высокоскоростной атомно‑силовой микроскопии показали, как эти локальные изменения проявляются на поверхности мембраны. При низком содержании кальция NZ2114 образовывал небольшие, высокоподвижные кластеры на мембране бактерии, тогда как плеказин уже расползался в большие, типа «ковровые» ансамбли. При избытке кальция NZ2114 претерпевал глобальную перестройку и переходил в крупные, упорядоченные «ковры», очень похожие на те, что формировал плеказин.
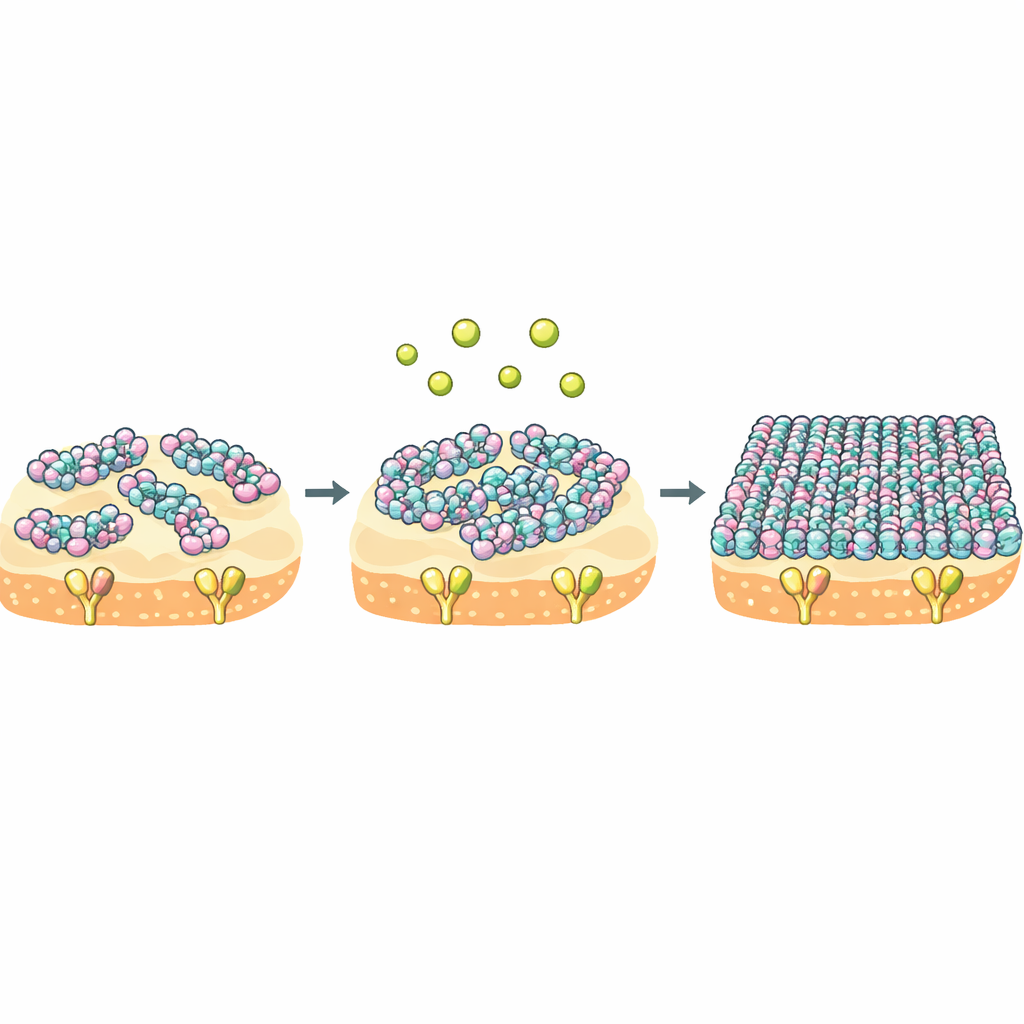
Кальций как переключатель коллективного поведения молекул
Ключевое понимание состоит в том, что NZ2114 и плеказин нацелены на один и тот же компонент, но различаются в «коллективном поведении», когда достигают мембраны. Для NZ2114 кальций действует как мощный переключатель: он переводит пептид из свободного, динамичного состояния в жёсткий, высокоорганизованный слой, который покрывает мембрану и надолго захватывает Липид II. Термодинамические измерения показывают, что NZ2114 несёт гораздо меньшие потери энтропии при связывании мишени, то есть связанное состояние остаётся более подвижным и разнообразным. Поскольку связывание и самоассамблея взаимосвязаны, это гибкое, но регулируемое кальцием поведение может позволять NZ2114 адаптировать свою супрамолекулярную структуру к разным микросредам на поверхности бактерии, тем самым повышая эффективность убийства.
Что это значит для проектирования будущих антибиотиков
Основная идея исследования для неспециалистов такова: преимущество NZ2114 вовсе не в том, что он захватывает другой «замок», а в том, что он формирует более эффективную «толпу» вокруг той же ключевой щели. Небольшие, точно расположенные мутации изменили ответ пептида на ионы кальция и его организацию с соседями на бактериальной мембране. Показав, что модификации Липид II в Staphylococcus aureus не являются причиной слабой работы плеказина, работа смещает внимание на контроль формы пептида, гибкости, заряда и чувствительности к ионам для настройки коллективного поведения. Эти выводы могут направить создание новых пептидных антибиотиков, которым бактериям труднее будет противостоять, и которые будут более эффективны против резистентных штаммов.
Цитирование: Derks, M.G.N., Jekhmane, S., Maity, S. et al. Molecular action of NZ2114, a superior plectasin derivative. npj Antimicrob Resist 4, 34 (2026). https://doi.org/10.1038/s44259-026-00196-6
Ключевые слова: антимикробные пептиды, Липид II, MRSA, кальций-зависимые антибиотики, супрамолекулярные сборки