Clear Sky Science · he
הפעולה המולקולרית של NZ2114, נגזרת משופרת של פלקטאזין
מדוע מולקולות פטרייתיות זעירות חשובות לאנטיביוטיקה העתידית
כאשר זיהומים חיידקיים מפסיקים להגיב לאנטיביוטיקות הטובות ביותר שלנו, מדענים מחפשים דרכים חדשות להרוג פתוגנים מבלי לעודד התפתחות מהירה של עמידות. כיוון מבטיח מגיע מהמולקולות ההגנתיות הקטנות שמייצרות פטריות ובעלי חיים. המחקר הזה חוקר כיצד מולקולה כזו, גרסה מותאמת במעבדה של הפפטיד הטבעי פלקטאזין הנקראת NZ2114, נלחמת בחיידקים מסוכנים כמו Staphylococcus aureus, כולל זני MRSA שקשה לטפל בהם. במיפוי הפעולה שלה שלב אחר שלב על דופן התא החיידקי, העבודה מצביעה על דרכים חכמות יותר לעיצוב אנטיביוטיקות בדור הבא.
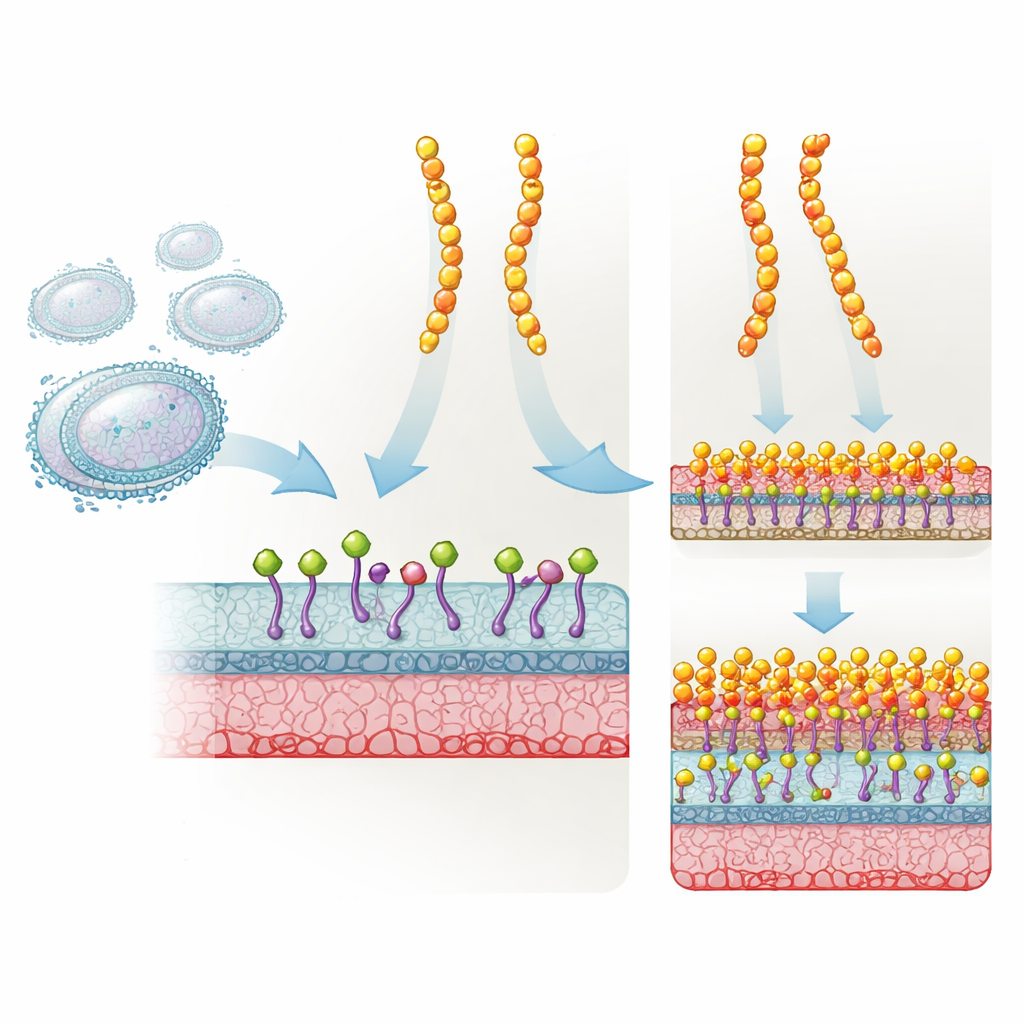
מגן טבעי שהפך לנשק חזק יותר
פלקטאזין הוא חלבון קצר וקשיח שמיוצר על ידי פטרייה ומגן באופן טבעי מפני חיידקים גרם‑חיוביים רבים. הוא פועל על ידי אחיזה ב‑Lipid II, מרכיב קריטי שבאמצעותו חיידקים בונים את דופן התא שלהם. כאשר Lipid II ננעל, דופן התא אינה נבנית כראוי והחיידק בסופו של דבר מת. מפתחי תרופות שינו את פלקטאזין בשלושה מקומות ספציפיים כדי ליצור את NZ2114, שהפגין יעילות רבה יותר במודלים של בעלי חיים נגד סטפילוקוקים וסטפטוקוקים. ועדיין, אף על פי הצלחתו והעניין הקליני בו, לא היה ברור מדוע המוטציה המשולשת עובדת טוב כל כך בהשוואה למקור.
לא אחיזה הדוקה יותר, אלא דרך שונה להיאחז
הסבר פשוט היה ש‑NZ2114 עשוי להידבק בחוזקה רבה יותר לצורת "מיוחדת" של Lipid II שנמצאת ב‑Staphylococcus aureus, בעוד שפלקטאזין ייקשור פחות היטב למטרה המותאמת הזאת. המחברים בדקו רעיון זה באמצעות מערך ניסויים מבניים ומדידות קשירה. הם בחנו כיצד שני הפפטידים מתקשרים עם מספר גרסאות של Lipid II, כולל אלה שנושאות שינויים כימיים אופייניים לסטפילוקוקים, ומדדו את חוזק הקשירה של כל פפטיד בסוגים שונים של ממברנות. התוצאה המפתיעה הייתה ששניהם — פלקטאזין ו‑NZ2114 — קושרו היטב לכל גרסאות Lipid II, לעתים פלקטאזין קשר במעט חזק יותר. זה פסל את ההנחה שזיהוי המטרה הוא הסיבה העיקרית ליעילות הגבוהה יותר של NZ2114.
כיצד שינויים קטנים מעצבים תנועה ועבודת צוות
כדי לגלות מה באמת השתנה, הצוות השתמש בNMR (תהודה מגנטית גרעינית) וסימולציות ממוחשבות כדי לבחון את שלוש חומצות האמינו שהוחלפו ב‑NZ2114. המוטציות האלה שינו בעדינות רשת של קשרי מימן בסמוך לכתם בעל מטען שלילי היכול למשוך יוני סידן ומגנזיום. זה, בתורו, שינה את צורת וגמישות הלולאה ה‑N‑טרמינלית של הפפטיד וקטע סמוך שנוגע ב‑Lipid II. NMR במצב מוצק ומיקרוסקופית כוח אטומית במהירות גבוהה חשפו כיצד התאמות מקומיות אלה באות לידי ביטוי על פני הממברנה. ברמות סידן נמוכות, NZ2114 יצר אשכולות קטנים וניידים על ממברנת החיידק, בעוד שפלקטאזין כבר התפזר לאספות רחבות ודמויי שטיח. כאשר הסידן היה בשפע, NZ2114 עבר ארגון עולמי והתארגן לשטיחים גדולים ומסודרים שהזכירו במידה רבה את אלה שהרכיב פלקטאזין.
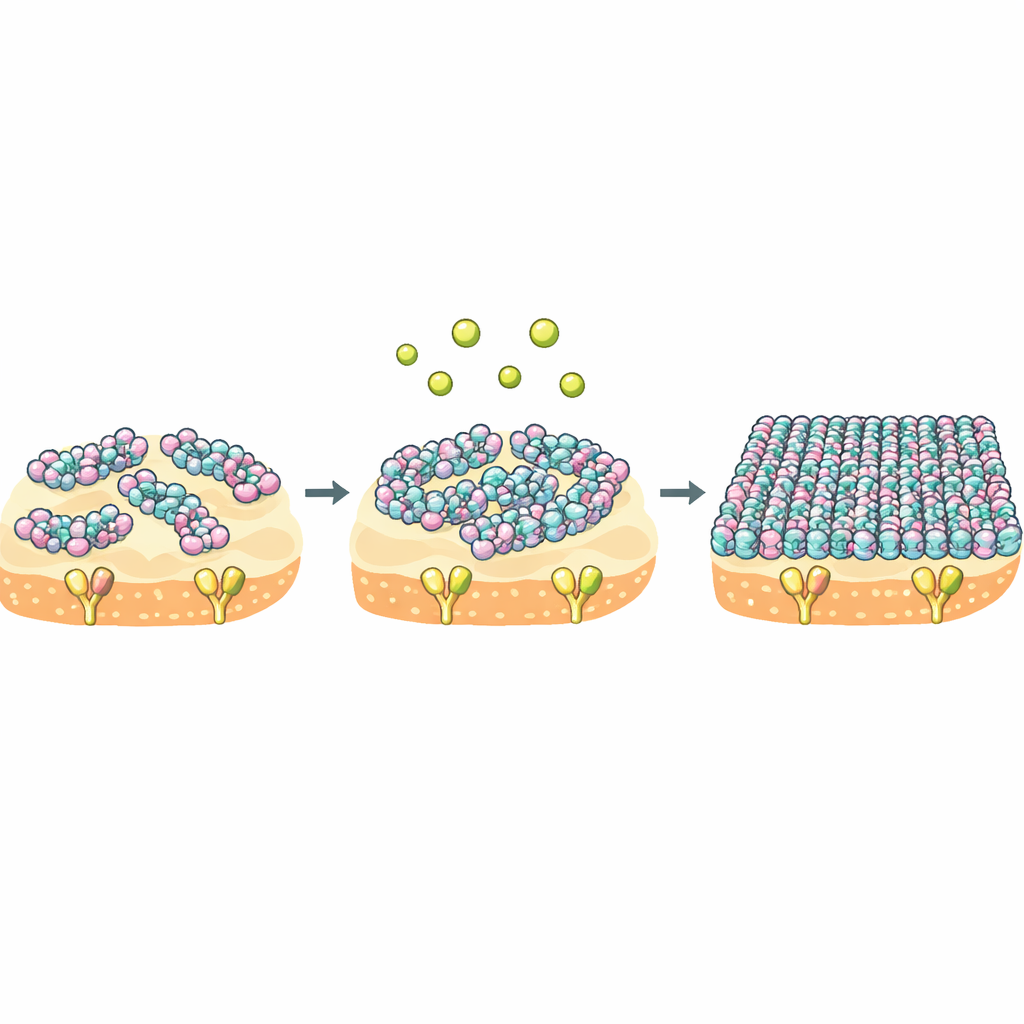
הסידן כמפסק להתנהגות המונית מולקולרית
התובנה המרכזית היא ש‑NZ2114 ופלקטאזין חולקים את אותה מטרה אך שונים בהתנהגותם הקבוצתית ברגע שהם מגיעים לממברנה. עבור NZ2114, הסידן פועל כמפסק עוצמתי: הוא מעביר את הפפטיד ממצב רפוי ודינמי לשכבה קשיחה ומאורגנת שמכסה את הממברנה ומלכדת את Lipid II לפרק זמן ממושך. מדידות תרמודינמיות מראות ש‑NZ2114 משלם עלות אנטרופית נמוכה בהרבה בעת קשירה לעומת פלקטאזין, כלומר המצב הקשור נשאר נייד ומגוון יותר. מאחר שקישור והתאספות עצמית משולבים, ההתנהגות הגמישה אך הניתנת לכוונון על‑ידי סידן עשויה לאפשר ל‑NZ2114 להתאים את המבנה הסופראמולקולרי שלו לסביבות שונות על פני השטח החיידקי ובכך לשפר את יעילות ההרג שלו.
מה משמעות הדבר לעיצוב אנטיביוטיקות עתידי
המסר העיקרי של המחקר לקהל הרחב הוא כי היתרון של NZ2114 אינו נובע מאחיזה במנעול שונה, אלא מהקמת קהל יעיל יותר סביב אותו מפתח. מוטציות קטנות וממוקדות שינו כיצד הפפטיד מגיב ליוני סידן וכיצד הוא מארגן את עצמו עם שכניו על ממברנת החיידק. בהצבעה שינויים ב‑Lipid II ב‑Staphylococcus aureus אינם הגורם לביצועי פלקטאזין החלשים יותר, העבודה מעבירה את המוקד לשליטה בצורת הפפטיד, גבישותו, מטענו ורגישותו ליונים כדי לכוונן התנהגות קולקטיבית. תובנות אלה יכולות להנחות את עיצובן של אנטיביוטיקות מבוססות פפטידים שקשה יותר לחיידקים להתחמק מהן וחזקות יותר כנגד זנים עמידים.
ציטוט: Derks, M.G.N., Jekhmane, S., Maity, S. et al. Molecular action of NZ2114, a superior plectasin derivative. npj Antimicrob Resist 4, 34 (2026). https://doi.org/10.1038/s44259-026-00196-6
מילות מפתח: פפטידים אנטימיקרוביאליים, Lipid II, MRSA, אנטיביוטיות התלויות בסידן, אספות סופראמולקולריות