Clear Sky Science · sv
Molekylär verkan av NZ2114, en överlägsen derivat av plectasin
Varför små svampmolekyler spelar roll för framtida antibiotika
När fler bakteriella infektioner slutar svara på våra bästa antibiotika söker forskare nya sätt att döda mikrober utan att snabbt framkalla resistens. Ett lovande spår kommer från små försvarsmolekyler som produceras av svampar och djur. Denna studie går på djupet i hur en sådan molekyl, en laboratorieanpassad version av det naturliga peptidet plectasin kallad NZ2114, bekämpar farliga bakterier som Staphylococcus aureus, inklusive svårbehandlade MRSA‑stammar. Genom att avslöja dess steg‑för‑steg‑verkan på bakteriers cellvägg pekar arbetet mot smartare utformning av nästa generations antibiotika.
En naturlig sköld förvandlad till ett starkare vapen
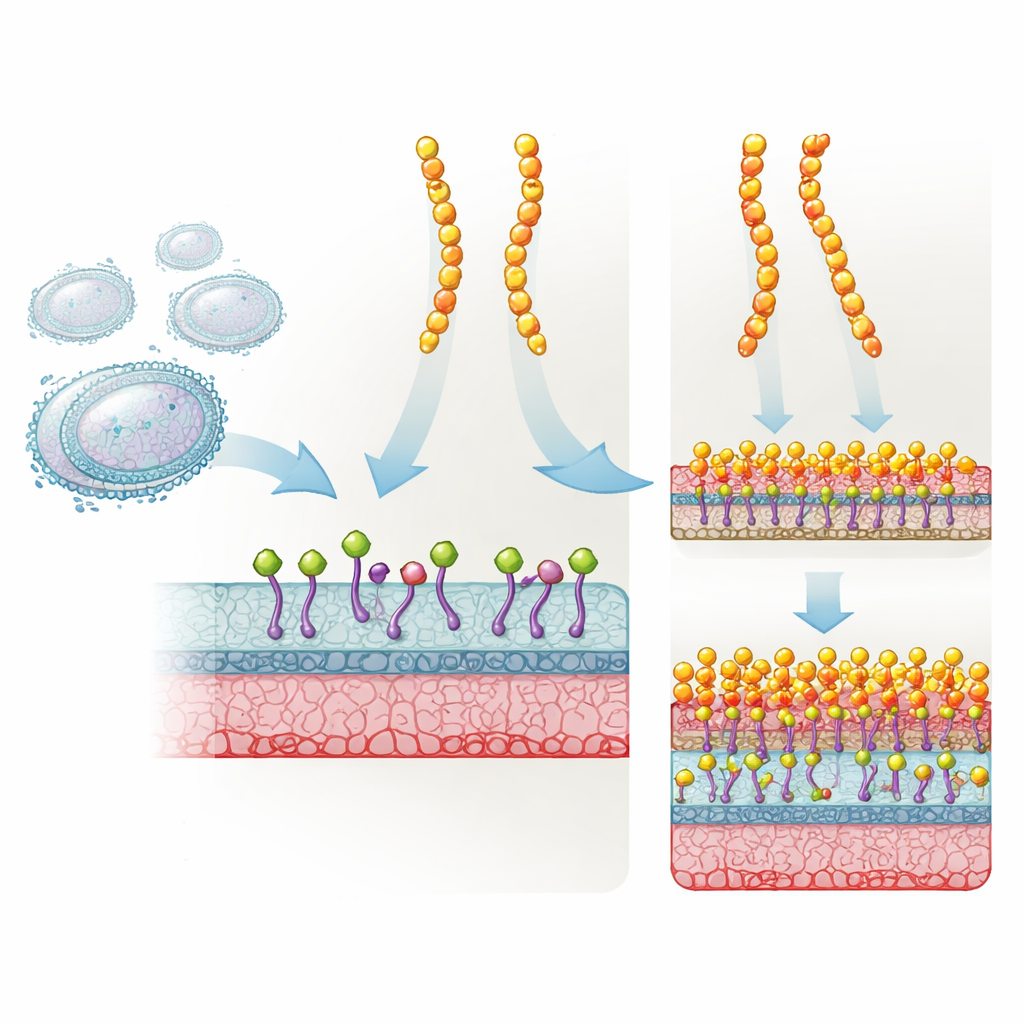
Plectasin är ett kort, stabilt peptid framställt av en svamp som naturligt försvarar mot många Gram‑positiva bakterier. Det verkar genom att binda till Lipid II, en kritisk byggsten som bakterier använder för att bygga sin cellvägg. När Lipid II blir låst kan cellväggen inte längre byggas korrekt och bakterien dör så småningom. Läkemedelsutvecklare modifierade plectasin på tre specifika positioner för att skapa NZ2114, vilket visade sig vara mycket effektivare i djurmodeller mot stafylokocker och streptokocker. Trots dess framgång och kliniska intresse var det dock oklart varför denna trippelmutant fungerade så mycket bättre än originalet.
Inte starkare grepp, utan ett annorlunda sätt att hålla i
En enkel förklaring hade varit att NZ2114 kanske fäster hårdare till en ”särskild” form av Lipid II som finns i Staphylococcus aureus, medan plectasin skulle binda dåligt till detta förändrade mål. Författarna testade denna idé direkt med en rad strukturella och bindningsmässiga experiment. De undersökte hur båda peptiderna interagerar med flera varianter av Lipid II, inklusive sådana med kemiska modifieringar typiska för stafylokocker, och mätte hur starkt varje peptid band i olika typer av membran. Det överraskande resultatet var att både plectasin och NZ2114 band alla Lipid II‑varianter mycket väl, ofta med plectasin som band något starkare. Detta uteslöt måligenkänning som huvudorsaken till NZ2114:s överlägsna dödande förmåga.
Hur små förändringar omformar rörelse och samarbete
För att se vad som verkligen förändrats använde teamet nukleär magnetisk resonans (NMR) och datorsimuleringar för att studera de tre utbytta aminosyrorna i NZ2114. Dessa mutationer omkonfigurerade subtilt ett nätverk av vätebindningar nära en negativt laddad yta som kan attrahera kalcium‑ och magnesiumjoner. Det förändrade i sin tur formen och flexibiliteten i peptidens N‑terminala loop och ett närliggande segment som tar kontakt med Lipid II. Solid‑state NMR och höghastighets atomkraftmikroskopi visade sedan hur dessa lokala justeringar slog igenom på en membranyta. Vid låga kalciumnivåer bildade NZ2114 små, mycket rörliga kluster på bakteriemembranet, medan plectasin redan spred ut sig i större, matta‑lika assembléer. När kalcium var rikligt genomgick NZ2114 en global omorganisation och vecklade ut sig till stora, ordnade mattor som starkt liknade dem som plectasin bildar.
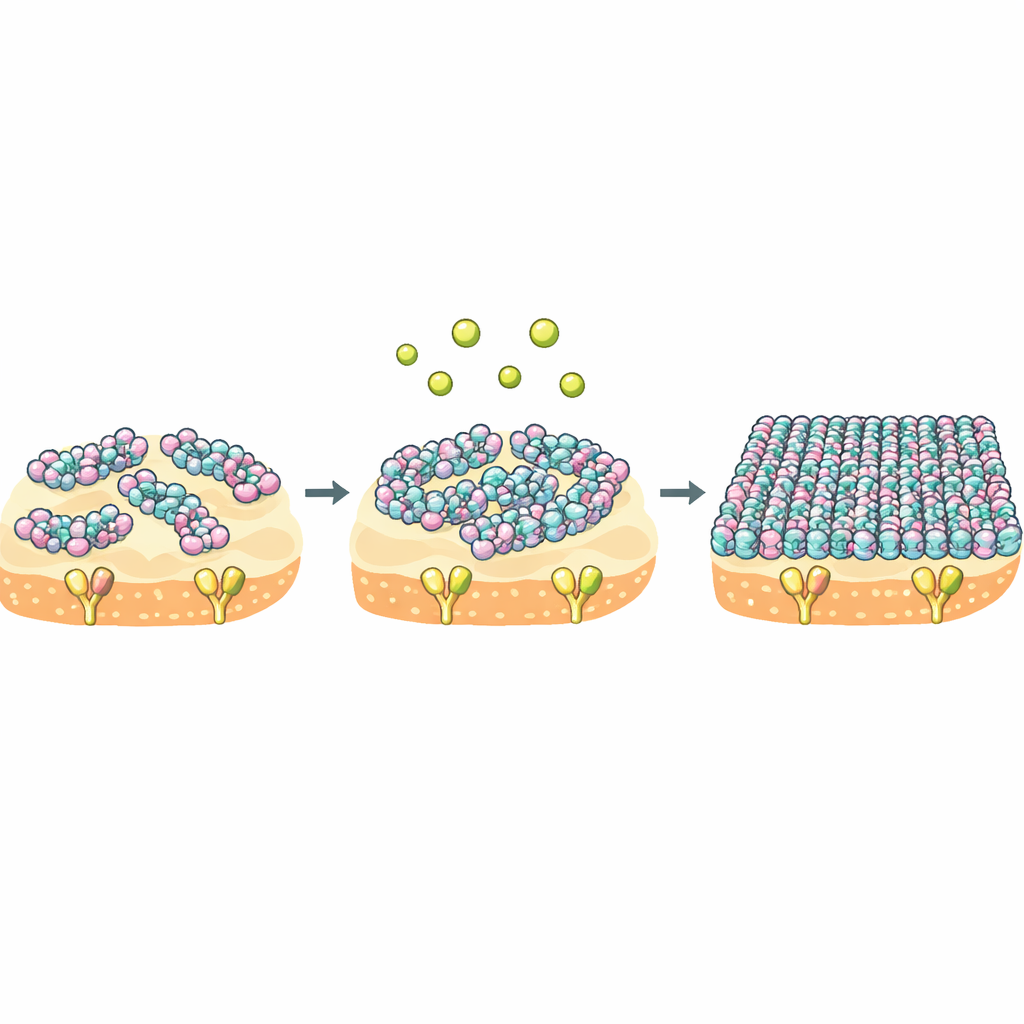
Kalcium som en omkopplare för molekylärt folkvimmelbeteende
Huvudinsikten är att NZ2114 och plectasin delar samma mål men skiljer sig i sitt ”folkvimmelbeteende” när de når membranet. För NZ2114 fungerar kalcium som en kraftfull omkopplare: det förflyttar peptiden från ett löst, dynamiskt tillstånd till ett stelt, högorganiserat skikt som täcker membranet och fångar Lipid II under lång tid. Termodynamiska mätningar visar att NZ2114 betalar mycket mindre i entropikostnad när den binder sitt mål, vilket betyder att det bundna tillståndet förblir mer rörligt och varierat. Eftersom bindning och själv‑aggregation är kopplade kan detta flexibla men kalcium‑stypbara beteende låta NZ2114 anpassa sin supramolekylära struktur till olika miljöer på bakterieytan och därigenom förbättra dess dödlighet.
Vad detta betyder för framtida antibiotikadesign
Studiens huvudbudskap för icke‑specialister är att NZ2114:s fördel inte kommer från att låsa upp ett annat hänglås, utan från att bilda en mer effektiv folkmassa runt samma nyckelhål. Små, noggrant placerade mutationer ändrade hur peptiden svarar på kalciumjoner och hur den organiserar sig med sina grannar på bakteriemembranet. Genom att visa att Lipid II‑modifieringar i Staphylococcus aureus inte är orsaken till plectasins svagare prestanda flyttas fokus mot att kontrollera peptidens form, flexibilitet, laddning och jonkänslighet för att finjustera kollektivt beteende. Dessa insikter kan vägleda utformningen av nya peptidbaserade antibiotika som är svårare för bakterier att undvika och mer potenta mot resistenta stammar.
Citering: Derks, M.G.N., Jekhmane, S., Maity, S. et al. Molecular action of NZ2114, a superior plectasin derivative. npj Antimicrob Resist 4, 34 (2026). https://doi.org/10.1038/s44259-026-00196-6
Nyckelord: antimikrobiella peptider, Lipid II, MRSA, kalciumberoende antibiotika, supramolekylära assembléer