Clear Sky Science · es
Acción molecular de NZ2114, un derivado superior de la plectasina
Por qué importan las pequeñas moléculas fúngicas para los antibióticos del futuro
A medida que más infecciones bacterianas dejan de responder a nuestros mejores antibióticos, los científicos buscan nuevas formas de matar microbios sin provocar una resistencia rápida. Una pista prometedora procede de pequeñas moléculas defensivas producidas por hongos y animales. Este estudio profundiza en cómo una de esas moléculas, una versión afinada en laboratorio del péptido natural plectasina llamada NZ2114, combate bacterias peligrosas como Staphylococcus aureus, incluidas cepas difíciles de tratar como MRSA. Al desvelar su acción paso a paso sobre la pared celular bacteriana, el trabajo apunta hacia un diseño más inteligente de antibióticos de próxima generación.
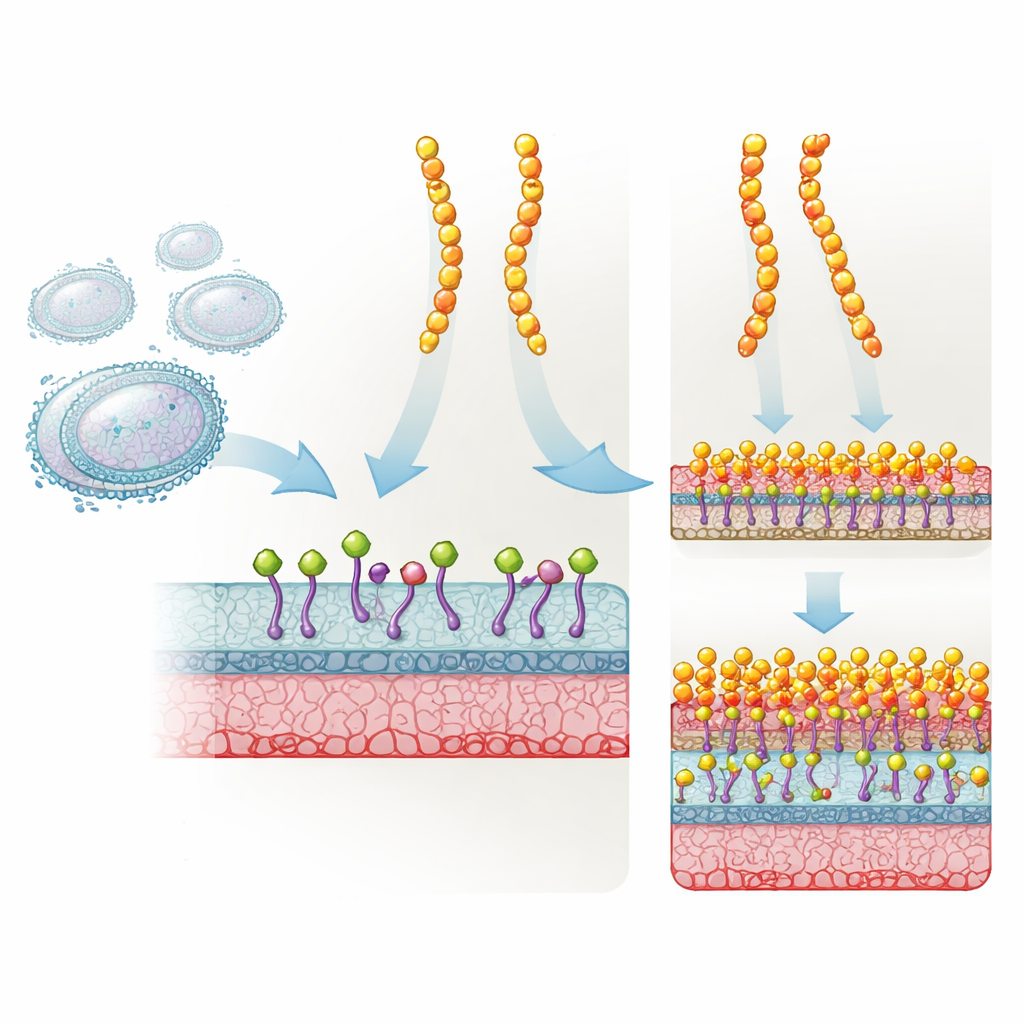
Un escudo natural convertido en arma más potente
La plectasina es una proteína corta y resistente producida por un hongo que protege de forma natural frente a muchas bacterias Gram‑positivas. Actúa capturando el Lípido II, un bloque de construcción crítico que las bacterias usan para fabricar su pared celular. Cuando el Lípido II queda secuestrado, la pared no puede formarse correctamente y la bacteria acaba muriendo. Los desarrolladores de fármacos modificaron la plectasina en tres posiciones específicas para crear NZ2114, que demostró ser mucho más eficaz en modelos animales contra estafilococos y estreptococos. Sin embargo, a pesar de su éxito e interés clínico, nadie sabía realmente por qué este triple mutante funcionaba tan mejor que la molécula original.
No una unión más fuerte, sino una forma distinta de agarrar
Una explicación simple proponía que NZ2114 podría adherirse con más fuerza a una forma “especial” de Lípido II presente en Staphylococcus aureus, mientras que la plectasina lo haría de forma deficiente. Los autores sometieron esta idea a una prueba directa usando una batería de experimentos estructurales y de afinidad. Estudiaron cómo ambos péptidos interactúan con varias versiones de Lípido II, incluidas las que presentan modificaciones químicas típicas de estafilococos, y midieron la intensidad de unión en distintos tipos de membranas. El resultado sorprendente fue que tanto la plectasina como NZ2114 se unían muy bien a todas las variantes de Lípido II, a menudo con la plectasina uniéndose ligeramente con mayor afinidad. Esto descartó el reconocimiento diferencial del objetivo como la razón principal de la mayor eficacia bactericida de NZ2114.
Cómo pequeños cambios remodelan el movimiento y el trabajo en equipo
Para ver qué había cambiado realmente, el equipo empleó resonancia magnética nuclear (RMN) y simulaciones por ordenador para examinar los tres aminoácidos sustituidos en NZ2114. Estas mutaciones reconfiguraron sutilmente una red de enlaces de hidrógeno cerca de un parche cargado negativamente que puede atraer iones calcio y magnesio. Eso, a su vez, alteró la forma y la flexibilidad del bucle N‑terminal del péptido y de un segmento cercano que contacta con el Lípido II. La RMN en estado sólido y la microscopía de fuerza atómica de alta velocidad revelaron luego cómo esos ajustes locales se traducen en la superficie de una membrana. A bajos niveles de calcio, NZ2114 formó pequeños cúmulos altamente móviles en la membrana bacteriana, mientras que la plectasina ya se disponía en ensamblajes más grandes, tipo alfombra. Cuando el calcio era abundante, NZ2114 experimentó una reorganización global y pasó a formar grandes alfombras ordenadas que se parecían mucho a las que forma la plectasina.
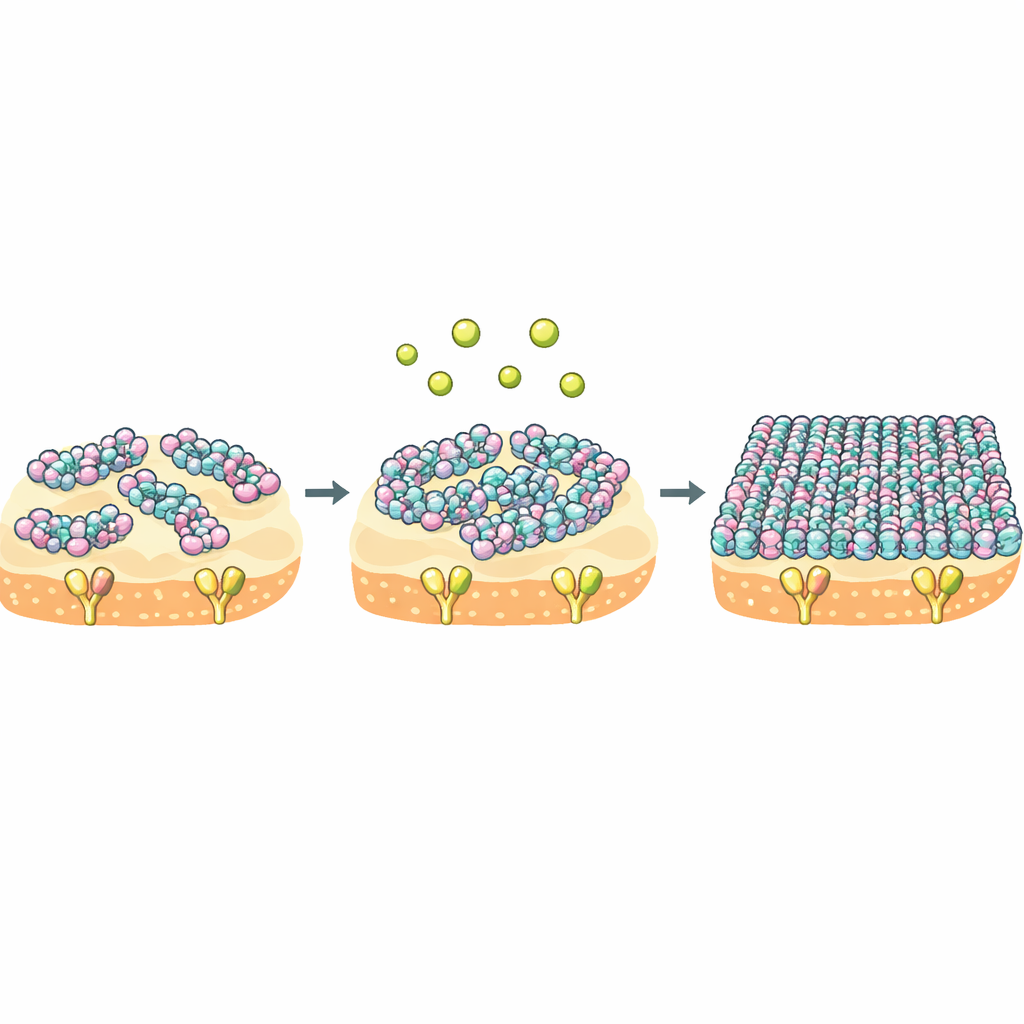
El calcio como interruptor del comportamiento colectivo molecular
La idea central es que NZ2114 y la plectasina comparten el mismo objetivo pero difieren en su “comportamiento de multitud” una vez que alcanzan la membrana. Para NZ2114, el calcio actúa como un potente interruptor: desplaza el péptido de un estado laxo y dinámico a una capa rígida y muy organizada que cubre la membrana y atrapa el Lípido II durante mucho tiempo. Mediciones termodinámicas muestran que NZ2114 paga mucho menos en coste de entropía al unirse a su objetivo, lo que significa que el estado ligado permanece más móvil y variado. Como la unión y la autoensamblaje están acoplados, este comportamiento flexible pero modulable por calcio podría permitir a NZ2114 adaptar su estructura supramolecular a diferentes entornos en la superficie bacteriana, aumentando así su eficiencia letal.
Qué implica esto para el diseño de antibióticos futuros
El mensaje principal del estudio para el público no especializado es que la ventaja de NZ2114 no proviene de abrir una cerradura distinta, sino de formar una multitud más efectiva alrededor de la misma cerradura. Pequeñas mutaciones colocadas con precisión cambiaron cómo responde el péptido a los iones de calcio y cómo se organiza con sus vecinos en la membrana bacteriana. Al mostrar que las modificaciones del Lípido II en Staphylococcus aureus no son la causa del menor rendimiento de la plectasina, el trabajo desplaza la atención hacia el control de la forma del péptido, su flexibilidad, carga y sensibilidad a iones para sintonizar el comportamiento colectivo. Estos conocimientos pueden guiar el diseño de nuevos antibióticos basados en péptidos que sean más difíciles de eludir por las bacterias y más potentes contra cepas resistentes.
Cita: Derks, M.G.N., Jekhmane, S., Maity, S. et al. Molecular action of NZ2114, a superior plectasin derivative. npj Antimicrob Resist 4, 34 (2026). https://doi.org/10.1038/s44259-026-00196-6
Palabras clave: péptidos antimicrobianos, Lípido II, MRSA, antibióticos dependientes de calcio, ensamblajes supramoleculares